11.04.2018
Basit maddelerin kimyasal özellikleri: metaller ve metal olmayanlar
Periyodik tabloda demir dördüncü periyotta, grup VIII'in ikincil bir alt grubunda yer alır.
Seri numarası 26, elektronik formülü ise 1s 2 2s 2 2p 6 3d 6 4s 2'dir.
Demir atomunun değerlik elektronları son elektron katmanında (4s 2) ve sondan bir önceki katmanda (3d 6) bulunur. Kimyasal reaksiyonlarda demir bu elektronları bağışlayabilir ve +2, +3 ve bazen +6 oksidasyon durumlarını sergileyebilir.
Demir, doğada alüminyumdan sonra en çok bulunan ikinci metaldir. En önemli doğal bileşikler: Fe2O3x3H2O - kahverengi demir cevheri; Fe2O3 - kırmızı demir cevheri; Fe3O4 (FeO Fe2O3) - manyetik demir cevheri; FeS2 - demir pirit (pirit). Demir bileşikleri canlı organizmalarda bulunur.
Demir, mükemmel işlenebilirliğe, sünekliğe ve güçlü manyetik özelliklere sahip gümüş grisi bir metaldir. Demirin yoğunluğu 7,87 g/cm3, erime noktası 1539C'dir.
Demir almak
Endüstride demir, demir cevherlerinin yüksek fırınlarda karbon (kok) ve karbon monoksit (II) ile indirgenmesiyle elde edilir.
Yüksek fırın işleminin kimyası aşağıdaki gibidir:
C + O2 = C02,
3Fe 2 O 3 + CO = 2Fe 3 O 4 + CO 2,
Fe304 + CO = 3FeO + CO2,
FeO + CO = Fe + CO2.
Tepkilerde demir indirgeyici bir maddedir. Ancak ne zaman normal sıcaklık en aktif oksitleyici maddelerle (halojenler, oksijen, kükürt) bile etkileşime girmez, ancak ısıtıldığında aktif hale gelir ve onlarla reaksiyona girer:
2Fe + 3Cl 2 = 2FeCl 3 Demir (III) klorür
3Fe + 2O 2 = Fe 3 O 4 (FeO x Fe 2 O 3) Demir (II,III) oksit
Fe + S = FeS Demir (II) sülfür
çok Yüksek sıcaklık demir karbon, silikon ve fosfor ile reaksiyona girer:
3Fe + C = Fe 3 C Demir karbür (sementit)
3Fe + Si = Fe 3 Si Demir silisit
3Fe + 2P = Fe 3 P 2 Demir (II) fosfit
Nemli havada demir hızla oksitlenir (paslanır):
4Fe + 3O2 + 6H2O = 4Fe(OH)3,
Demir, metallerin elektrokimyasal voltaj serisinin ortasında yer alır, bu nedenle orta aktivite metali. Demirin indirgeme yeteneği alkali, alkali toprak metalleri ve alüminyumdan daha azdır. Sıcak demir yalnızca yüksek sıcaklıklarda suyla reaksiyona girer:
3Fe + 4H 2 Ö = Fe 3 Ö 4 + 4H 2
Demir, seyreltik sülfürik ve hidroklorik asitlerle reaksiyona girerek asitlerdeki hidrojenin yerini alır:
Fe + 2HCl = FeCl2 + H2
Fe + H2S04 = FeS04 + H2
Normal sıcaklıkta demir, konsantre sülfürik asit tarafından pasifleştirildiği için etkileşime girmez . Isıtıldığında konsantre H2S04, demiri demir (III) sülfite oksitler:
2Fe + 6H 2 SO 4 = Fe 2 (SO 4) 3 + 3SO 2 + 6H 2 O.
Seyreltik nitrik asit, demiri demir (III) nitrata oksitler:
Fe + 4HNO3 = Fe(NO3)3 + NO + 2H2O.
Konsantre nitrik asit demiri pasifleştirir.
Tuz çözeltilerinden demir, elektrokimyasal voltaj serisinde sağında bulunan metallerin yerini alır:
Fe + CuS04 = FeS04 + Cu
Demir(II) oksit FeO- bazik oksit, asitlerle kolayca reaksiyona girerek demir(II) tuzlarının oluşmasına neden olur:
FeO + 2HCl = FeCl2 + H20
FeO + 2H + = Fe 2+ + H 2 O
Demir (II) hidroksit Fe(OH) 2 - pudra beyaz, suda çözünmez. Demir (II) tuzlarının alkalilerle reaksiyona sokulmasıyla elde edilir:
FeS04 + 2NaOH = Fe(OH)2 + Na2S04,
Fe(OH) 2 bazın özelliklerini gösterir ve asitlerle kolayca reaksiyona girer:
Fe(OH)2 + 2HCl = FeCl2 + 2H20,
Fe(OH)2 + 2H+ = Fe2+ + 2H2O.
Isıtıldığında demir (II) hidroksit ayrışır:
Fe(OH)2 = FeO + H20.
Demir +2 oksidasyon durumuna sahip bileşikler, Fe 2+ kolayca Fe +3'e oksitlendiğinden indirgeyici özellikler sergiler: Fe +2 - 1e = Fe +3
Böylece, havadaki taze elde edilen yeşilimsi Fe(OH)2 çökeltisi çok hızlı bir şekilde renk değiştirir - kahverengiye döner. Renk değişimi Fe(OH)2'nin atmosferik oksijenle Fe(OH)3'e oksidasyonu ile açıklanır:
4Fe(OH)2 + O2 + 2H20 = 4Fe(OH)3.
Demir(III) oksit Fe 2 Ö 3 - kahverengi toz, suda çözünmez.
Demir (III) oksit, demir (III) hidroksitin ayrışmasıyla elde edilir:
2Fe(OH)3 = Fe203 + 3H2O
Demir (III) oksit amfoterik özellikler sergiler:
yüksek sıcaklıklarda asitler ve katı alkaliler NaOH ve KOH'un yanı sıra sodyum ve potasyum karbonatlarla etkileşime girer:
Fe203 + 2NaOH = 2NaFeO2 + H20,
Fe203 + 2OH - = 2FeO2- + H2O,
Fe203 + Na2C03 = 2NaFeO2 + C02.
Sodyum ferrit
Demir(III) hidroksit demir (III) tuzlarının alkalilerle reaksiyona sokulmasıyla elde edilir:
FeCl3 + 3NaOH = Fe(OH)3 + 3NaCl,
Demir (III) hidroksit Fe(OH)2'den daha zayıf bir bazdır ve amfoterik özellikler (ana olanların ağırlıklı olduğu). Seyreltik asitlerle etkileşime girdiğinde Fe(OH) 3 kolayca karşılık gelen tuzları oluşturur:
Fe(OH)3 + 3HCl = FeCl3 + H20
2Fe(OH)3 + 3H2S04 = Fe2(S04)3 + 6H20
Konsantre alkali çözeltileriyle reaksiyonlar yalnızca uzun süreli ısıtmayla meydana gelir:
Fe(OH)3 + KOH = K
Demir oksidasyon durumu +3 olan bileşikler oksitleyici özellikler sergilemek çünkü indirgeyici ajanların etkisi altında Fe+3 Fe+2'ye dönüşür: Fe +3 + 1e = Fe +2.
Örneğin demir (III) klorür, potasyum iyodürü serbest iyodine oksitler:
2FeCl3 + 2KI = 2FeCl2 + 2KCl + I2 0
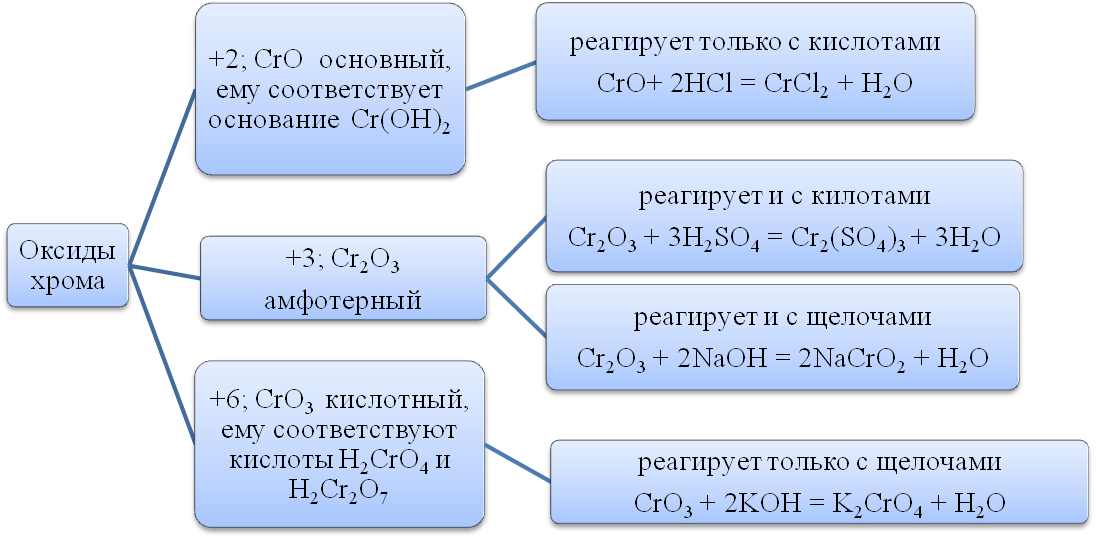
Krom.
 Krom, Periyodik tablonun VI. grubunun ikincil alt grubunda yer alır. Kromun elektron kabuğunun yapısı: Cr 3d 5 4s 1. Oksidasyon durumları +1 ila +6 arasında değişir, ancak en kararlı olanları +2, +3, +6'dır.
Krom, Periyodik tablonun VI. grubunun ikincil alt grubunda yer alır. Kromun elektron kabuğunun yapısı: Cr 3d 5 4s 1. Oksidasyon durumları +1 ila +6 arasında değişir, ancak en kararlı olanları +2, +3, +6'dır.
Kromun kütle oranı yerkabuğu%0,02'dir. Krom cevherlerini oluşturan en önemli mineraller, kromit veya krom demir cevheri ve demirin kısmen magnezyumla ve kromun alüminyumla değiştirildiği çeşitleridir.
Krom gümüş grisi bir metaldir. Saf krom oldukça yumuşaktır ve teknik krom tüm metallerin en sertidir.
Krom kimyasal olarak aktif değildir . Normal koşullar altında, yalnızca flor (metal olmayanlardan) ile reaksiyona girerek bir florür karışımı oluşturur. Yüksek sıcaklıklarda (600°C'nin üzerinde) oksijen, halojenler, nitrojen, silikon, bor, kükürt, fosfor ile etkileşime girer:
4Cr + 3O2 = 2Cr203
2Cr + 3Cl2 = 2CrCl3
2Cr + N 2 = 2CrN
2Cr + 3S = Cr2S3
Nitrik ve konsantre sülfürik asitlerde pasifleşir, koruyucu bir oksit film ile kaplanmıştır. Hidroklorik ve seyreltik sülfürik asitlerde çözünür ve asitin çözünmüş oksijenden tamamen arındırılması durumunda krom(II) tuzları elde edilir, reaksiyonun havada gerçekleşmesi durumunda krom(III) tuzları elde edilir: Cr + 2HCl = CrCl 2 + H2; 2Cr + 6HCl + O2 = 2CrCl3 + 2H20 + H2
1. Metalik olmayan özellikler basit maddeler seri olarak yoğunlaşmak
1) nitrojen → fosfor → arsenik 2) flor → klor → brom
3) selenyum → kükürt → oksijen 4) fosfor → silikon → alüminyum
2. Hem sodyum hem de bakır reaksiyona girer
1) sodyum hidroksit 2) su 3) hidrojen 4) nitrik asit
3. Hem demir hem de çinko reaksiyona girer
1) magnezyum hidroksit 2) karbon monoksit (II) 3) bakır (II) sülfat 4) su
4. Demir iki maddenin her biriyle reaksiyona girer: 1) O2 ve NaCl 2) KOH ve H2S 3) HCl ve S 4) Na2S ve K2O
5. Alüminyum tepki vermiyor çözüm ile
1) sülfürik asit 2) magnezyum sülfat 3) sodyum hidroksit 4) bakır(II) nitrat
6. Seyreltik sülfürik asit, 1) Zn 2) Ag 3) NaNO3 4) SO2 ile reaksiyona girer
7. Aşağıdaki metallerden hangisi ile reaksiyona girer? hidroklorik asit?
1) gümüş 2) altın 3) alüminyum 4) bakır
8. Hem çinko hem de bakırla reaksiyona girer
1) klor 2) karbon monoksit (II) 3) sodyum hidroksit 4) hidroklorik asit
9. Alüminyum tepki vermiyor İle
1) su 2) potasyum hidroksit 3) hidroklorik asit 4) sodyum klorür
10. İki maddenin her biri demirle reaksiyona girebilir:
1) CuSO 4 ve O 2 2) S ve NaOH (p-p) 3) MgCl 2 ve H 2 O 4) Na 2 SO 4 ve Hg(NO 3) 2
11. İki metalden her biri oda sıcaklığında suyla reaksiyona girer:
1) Zn ve Cu 2) K ve Ca 3) Zn ve K 4) Ca ve Ag
12. İki metalden her biri bir sülfürik asit çözeltisiyle reaksiyona girer:
1) Zn ve Hg 2) Ag ve Mg 3) Zn ve Mg 4) Cu ve Hg
13. 1) nitrojen lityum ile reaksiyona girer 2) sodyum oksit 3) kalsiyum 4) kalsiyum fosfat
14. Alüminyum aşağıdakilerle reaksiyona girer:
1) magnezyum 2) karbon monoksit (II) 3) demir (II) hidroksit 4) gümüş nitrat (çözelti)
15. Hem çinko hem de kalsiyum reaksiyona girer
1) su 2) brom 3) sodyum hidroksit 4) silisik asit
16. Demir, metali çözeltiden uzaklaştırır
1) alüminyum klorür 2) çinko sülfat 3) bakır(II) nitrat 4) potasyum silikat
17. Oda sıcaklığında çinko iki maddenin her biriyle reaksiyona girer:
1) hidroklorik asit ve gümüş nitrat 2) su ve sodyum hidroksit
3) kükürt(VI) oksit ve alüminyum oksit 4) bakır(II) sülfat ve su
18. Reaksiyon 1) Fe ve S 2) P ve H2 3) Cl2 ve O2 4) Fe ve K arasında mümkündür.
19. Reaksiyon sonucunda bakır oluşumu meydana gelir.
1) bakır(II) oksitli hidrojen 2) bakır(II) klorürlü hidrojen
3) bakır(II) klorürlü gümüş 4) bakır(II) sülfürlü oksijen
20. Hidroklorik asit çözeltisi ile reaksiyona girmez
1) gümüş 2) bakır(II) oksit 3) bakır(II) hidroksit 4) bakır(II) karbonat
21. Magnezyum ile tepki vermiyor 1) klor 2) kalsiyum oksit 3) hidroklorik asit 4) bakır(II) sülfat (çözelti)
22. Bakırlı tepki vermiyor 1) klor 2) oksijen 3) sülfürik asit (kons.) 4) demir(II) klorür (çözelti)
23. 1) bakır 2) kalsiyum oksit 3) sodyum hidroksit 4) nitrik asit magnezyum ile reaksiyona girer
24. 1) demir 2) çinko 3) bakır 4) magnezyum bir alkali çözeltiyle etkileşime girer
25. Alüminyum ile reaksiyona girmez
1) sülfürik asit 2) sodyum hidroksit 3) bakır(II) klorür 4) çinko hidroksit
26. 1) Na2S 2) BaCl2 3) K2CO3 4) AgNO3'ün demirle reaksiyona girdiği çözelti
27. Magnezyum aşağıdakilerle reaksiyona girer:
1) sodyum oksit 2) lityum sülfat 3) çinko klorür (çözelti) 4) potasyum hidroksit (çözelti)
28. 1) çinko 2) gümüş 3) demir 4) kalay bakır(II) sülfat çözeltisiyle reaksiyona girmez
29 Çinko aşağıdakilerle reaksiyona girer:
1) alüminyum oksit 2) hidroklorik asit 3) demir(III) hidroksit 4) demir(II) sülfit
otuz. Hem lityum hem de çinko oda sıcaklığında reaksiyona girer.
31. Bir çinko klorür çözeltisi ile arasındaki reaksiyon
1) demir 2) bakır 3) kurşun 4) alüminyum
32. Bakır(II) nitrat çözeltisiyle etkileşime girebilir
1) çinko 2) demir(III) hidroksit 3) silikon(IV) oksit 4) karbon
33. Isıtıldığında aralarında bir reaksiyon meydana gelir.
1) demir ve kükürt 2) nitrojen ve su 3) bakır ve kükürt oksit (IV) 4) fosfor ve çinko oksit
34. Alüminyum iki maddenin her biriyle reaksiyona girer
1) K 2 O ve K 2 SO 4 2) S ve LiCl 3) Cl 2 ve H 2 SO 4 4) H 2 O ve Cu(OH) 2
35. Lityum ve demirin her ikisi de reaksiyona girer
1) sodyum hidroksit 2) su 3) kükürt 4) hidroklorik asit
36. Hem magnezyum hem de alüminyum ile reaksiyona girer
1) sodyum klorür 2) baryum oksit 3) potasyum hidroksit 4) sülfürik asit
37. Demir, 1) bromin 2) sodyum oksit 3) kalsiyum klorür 4) sodyum hidroksit ile reaksiyona girer
38. Su ile etkileşime girdiğinde alkali ve hidrojen oluşur.
1) silikon 2) potasyum 3) çinko 4) alüminyum
39. Potasyum iki maddenin her biriyle etkileşime girer
1) H 2 O ve S 2) O 2 ve Ba 3) Cu ve N 2 4) HCl ve NaOH
40. Demir tepki vermiyor çözüm ile
1) hidroklorik asit 2) sülfürik asit 3) baryum klorür 4) gümüş nitrat
41. Magnezyum normal koşullar altında iki maddenin her biriyle reaksiyona girer:
1) su ve hidroklorik asit 2) su ve sodyum hidroksit
3) hidroklorik asit ve sodyum hidroksit 4) hidroklorik asit ve bakır(II) sülfat çözeltisi
42. Demir, metali çözeltiden uzaklaştırır 1) Zn(NO3)2 2) CuSO4 3) AlCl3 4) Ba(OH)2
43. Fosforik asit çözeltisindeki hidrojen, yerini alabilir
1) demir 2) bakır 3) altın 4) gümüş
44. Potasyum iki maddenin her biriyle etkileşime girer: 1) Ca ve O 2 2) Cu ve N 2 3 HCl ve S 4) H 2 O ve NaOH
45. Metalleri oksitlerinden geri kazanmak için 1) CO 2 2) CO 3) SO 3 4) HAYIR kullanın
46. Alüminyum iki maddenin her biriyle etkileşime girer:
1) Cl 2 ve H 2 SO 4 2) S ve NaCl 3) H 2 O ve Cu(OH) 2 4) K 2 O ve Na 2 SO 4
47. Aşağıdaki metallerden hangisi hidrojeni hidroklorik asit çözeltisinden uzaklaştırır?
1) cıva 2) bakır 3) demir 4) gümüş
48. 1) bakır 2) altın 3) çinko 4) gümüş seyreltik sülfürik asitle reaksiyona girer
49. Hem klor hem de oksijen reaksiyona girer
1) hidroklorik asit 2) sodyum hidroksit 3) su 4) demir
50. Normal koşullar altında demir iki maddenin her biriyle reaksiyona girer
1) kükürt oksit (VI) ve oksijen 2) hidrojen ve karbon
3) oksijen ve klor 4) su ve demir
51. 52. Reaksiyonlardaki flor 1) yalnızca bir indirgeyici maddenin özelliklerini gösterir
2) yalnızca oksitleyici bir maddenin özelliklerini sergiler
3) hem oksitleyici bir maddenin hem de bir indirgeyici maddenin özelliklerini sergileyebilir
4) redoks özelliği göstermez
51. Hem magnezyum hem de sodyum güçlü bir şekilde reaksiyona girer.
1) su 2) hidroklorik asit 3) baryum hidroksit 4) kalsiyum karbonat
52. Kurşun nitrat ile ikame reaksiyonuna girer.
1) hidrojen 2) demir 3) bakır 4) gümüş
53. Azot 1) su 2) hidroklorik asit 3) oksijen 4) fosfor ile reaksiyona girer
54. Bakır, 1) AgNO3 2) FeSO4 3) Al2(SO4)3 4) NaOH çözeltisiyle reaksiyona girer
55. Oda sıcaklığında iki metalin her biri suyla reaksiyona girer:
1) Ba ve Fe 2) Ag ve Al 3) Na ve Ba 4) Pb ve K
56. Çinko 1) sodyum klorür 2) bakır(II) klorür ile reaksiyona girer
3) silikon oksit (IV) 4) fosfor oksit (V)
57. Çinko, metali çözeltiden uzaklaştırır
1) potasyum nitrat 2) kalsiyum nitrat 3) bakır(II) sülfat 4) magnezyum sülfat
58. 1) sodyum 2) nitrojen 3) gümüş 4) klor ısıtmadan oksijenle reaksiyona girer
59. Hem kalsiyum hem de beyaz fosfor reaksiyona girer
1) hidroklorik asit 2) potasyum hidroksit 3) oksijen 4) Su
60. İki metalden her biri hidroklorik asitle reaksiyona girer:
1) Ca ve Ag 2) Hg ve Na 3) Cu ve Zn 4) Mg ve Zn
61. Oksijen normal koşullar altında aşağıdaki maddelerden hangisiyle reaksiyona girer?
1) nitrojen) sodyum 3) alüminyum oksit 4) karbon monoksit (IV)
62. 1) bakır oksijenle reaksiyona girer 2) karbon monoksit (IV) 3) sodyum hidroksit 4) sülfürik asit
63. 1) hidrojen karbonla reaksiyona girer 2) magnezyum hidroksit 3) kalsiyum klorür 4) fosforik asit
64. Hidrojen 1) bakır 2) bakır(II) oksit 3) bakır(II) hidroksit 4) bakır(II) sülfat ile reaksiyona girer
65. Kükürt, 1) magnezyum 2) oksijen 3) hidrojen 4) demir ile reaksiyona giren bir indirgeyici maddedir
66. İki metalden her biri hidroklorik asitle reaksiyona girer:
1) Zn ve Cu 2) Ag ve Mg 3) Zn ve Mg 4) Cu ve Ag
67. 1) klor 2) bakır 3) potasyum hidroksit 4) hidroklorik asit hidrojenle reaksiyona girer
68. 1) flor 2) nitrojen 3) kükürt 4) demir ısıtmadan hidrojenle reaksiyona girer
69. 1) oksijen 2) demir 3) karbon 4) silikon seyreltik sülfürik asitle reaksiyona girer
70.Cevap vermiyorlar birlikte
1) klor ve hidrojen 2) oksijen ve kalsiyum
o 3) nitrojen ve su 4) demir ve kükürt
71. 1) Ag 2) Mg 3) Fe 4) Al, sodyum hidroksit ve hidroklorik asit çözeltileriyle reaksiyona girer
72. Fosfor 1) NaCl 2) O2 3) KBr 4) H2 ile reaksiyona girer
73. Brom, başka bir halojeni çözeltiden uzaklaştırır
1) sodyum klorür 2) potasyum iyodür 3) sodyum florür 4) hidrojen florür
74. Hem magnezyum hem de kükürt aşağıdakilerle reaksiyona girer:
1) alkaliler 2) seyreltik sülfürik asit 3) nitrojen 4) oksijen
75. Hidrojen 1) CuO 2) NaOH 3) NH3 4) K 2 O ile reaksiyona girer
76. Hem oksijen hem de hidrojen 1) FeO 2) CuO 3) NH 3 4) H 2 S ile reaksiyona girer
77. Hem demir hem de fosfor 1) hidrojen 2) klor 3) alkaliler 4) hidroklorik asit ile reaksiyona girer
78. 1) demir(III) oksit 2) sodyum hidroksit 3 hidroklorik asit 4) bakır karbonla reaksiyona girer
79. Baryum bromür çözeltisiyle reaksiyona girer: 1) ZnCl 2 2) KI 3) FeO 4) Cl 2
80. Hidrojen 1) bakır(II) oksit 2) klor 3) sodyum hidroksit 4) oksijen ile reaksiyona girmez
81. Isıtıldığında hidrojen girer Kimyasal reaksiyonİle
1) su 2) bakır (II) oksit 3) sodyum klorür 4) amonyak
82. Hidrojen asit çözeltilerinden çıkarılabilir
1) platin 2) bakır 3) magnezyum 4) gümüş
83. Potasyum hidroksit çözeltisi 1) bakır 2) magnezyum 3) karbon 4) alüminyumu çözebilir
84. İki maddenin her biri oda sıcaklığında suyla reaksiyona girer:
1) magnezyum ve kükürt 2) alüminyum ve fosfor 3) sodyum ve kalsiyum 4) oksijen ve karbon
85. 1) gümüş 2) cıva 3) kükürt 4) magnezyum, bakır(II) sülfat çözeltisiyle reaksiyona girer
86. Seyreltik sülfürik asit ile tepki vermiyor
1) demir 2) çinko 3) bakır 4) magnezyum
87. Kükürt iki maddenin her biriyle reaksiyona girer:
1) nitrojen ve çinko 2) oksijen ve magnezyum oksit 3) sodyum hidroksit ve amonyak 4) hidrojen ve cıva
88. Oksijen 1) NaOH 2) SO2 3) FeCl3 4) CO2 ile reaksiyona girer
89. Oksijen iki maddenin her biriyle reaksiyona girer:
1) CO ve Mg 2) CO 2 ve Mg 3) MgO ve C 4) SiO 2 ve P
90. Hem magnezyum hem de hidrojen ile reaksiyona girer
1) klor 2) fosfor oksit (V) 3) kalsiyum hidroksit 4) hidrosülfit asit
91. Hidrojenle reaksiyona girer
1) amonyak 2) sodyum hidroksit 3) kükürt 4) fosforik asit
92. Azot, hafif bir ısıtmayla kimyasal reaksiyona girebilir.
1) kükürt 2) magnezyum 3) karbon 4) demir
93. Klor 1) N 2 2) KF 3) NaI 4) O 2 ile reaksiyona girer
94. Karbonla reaksiyona girmez
1) sodyum 2) hidrojen 3) karbon monoksit (II) 4) sülfürik asit (kons.)
95. Hidrojen, bir sülfürik asit çözeltisinin etkileşimi sonucu oluşur ve
1) sodyum oksit 2) sodyum karbonat 3) bakır 4) demir
96. Karbon ile reaksiyona girmez
1) demir(II) oksit 2) oksijen 3) hidrojen 4) sodyum klorür
97. Klor 1) oksijen2) nitrik asit 3) kalsiyum bromit4) alüminyum sülfat ile reaksiyona girer
98. Maddelerin her biri – KOH, HCl, AgNO 3 – 1) Cu 2) Mg 3) Al 4) Fe ile etkileşime girer.
99. Hem klor hem de nitrojen reaksiyona girer
1) hidroklorik asit 2) sodyum hidroksit 3) hidrojen 4) magnezyum
100. Normal koşullar altında 1) klor 2) kalsiyum 3) flor 4) kükürt suyla reaksiyona girmez
101. Hidrojen kimyasal olarak reaksiyona girebilir
1) argon 2) klor 3) silikon 4) demir
102. Karbon, etkileşime girdiğinde oksitleyici özellikler sergiler
1) O 2 2) Ca 3) Fe 2 O 3 4) CuO
103. Hidrojen iki maddenin her biriyle reaksiyona girer:
1) H2S ve O2 2) CuO ve SO2 3) FeO ve N2 4) NH3 ve S
104. Klor Olumsuz yer değiştirir çözeltiden halojen
1) sodyum florür 2) sodyum bromür 3) sodyum iyodür 4) hidrojen bromür
105. Bakır(II) sülfat ve çinko reaksiyona girdiğinde,
1) kükürt ve çinko oksit2) bakır ve çinko sülfat 3) su ve çinko sülfür4) çinko oksit ve bakır sülfür
106. 1) su oksijenle reaksiyona girer 2) karbon monoksit (II) 3) alüminyum oksit 4) sodyum nitrat
107. Oda sıcaklığındaki magnezyum ile reaksiyona girer
1) bakır(II) hidroksit 2) kalsiyum oksit 3) çinko klorür 4) su
108. Seyreltik alkali solüsyonla reaksiyona girer
1) bakır 2) alüminyum 3) karbon 4) demir
109. Aşağıdaki metallerden hangisi en büyük değeri sergiler? kimyasal aktivite suyla reaksiyona giriyor mu?
1) sodyum 2) potasyum 3) çinko 4) magnezyum
110. Hem oksijen hem de hidrojen ile reaksiyona girer
1) fosfor oksit (V) 2) kükürt 3) su 4) alüminyum oksit
111. Hidrojenin evrimi Olmuyorçinko çözeltisi ile etkileşime girdiğinde
GAÜ DPO (PC) "Bryansk Bölge Eğitim Kalitesi Değerlendirme Merkezi" ile
Demo sürümü
Bryansk bölgesindeki öğretim ve yönetim çalışanlarının, tutulan pozisyona uygunluğunu doğrulamak için sertifikalandırılması için
Kimya
Bryansk
A1. Parçacık bir kripton atomunun elektronik konfigürasyonuna sahip
1) Br − 2) Cl 5+ 3) Rb o 4) Se 4+
A2. Kimyasal element atomunun elektronik konfigürasyonu 1s 2 2s 2 2p 1'e karşılık gelir Genel formül daha yüksek oksit
1) R 2 O 3 2)RO 2 3)R 2 O 4)RO 3
A3. Polar kovalent bağa sahip bir madde aşağıdaki formüle sahiptir:
1) S 8 2) NaCl 3) MgO 4) HCl
A4. Kükürt bileşikte en yüksek oksidasyon derecesini sergiler
1) SO 2 2) K 2 SO 3 3) Na 2 SO 4 4) K 2 S
A5. moleküler kristal kafes Var
1) sofra tuzu 2) soda 3) elmas 4) glikoz
A6. Formülleri olan maddeler listesinde
A) S 5 H 10 B) S 4 H 8 C) S 4 H 6 D) S 3 H 6 D) S 3 H 4 E) S 5 H 8
asetilen hidrokarbonlar şunları içerebilir
1) AVE 2) GD 3) NEREDE 4) NEREDE
A7. Demir ile ilgili aşağıdaki ifadeler doğru mudur?
A. Demirin oksidasyon durumu +8'dir.
B. Demir, bakırı bakır (II) sülfat çözeltisinden uzaklaştırır
A8. Nitrik asit, formülü şu şekilde olan bir okside karşılık gelir:
1) HAYIR 2)N 2 O 3 3) HAYIR 2 4) N 2 O 5
A9. Demir çözeltiyle reaksiyona girer
1) Hg(NO 3) 2 2) Mg(NO 3) 2 3) K 2 SO 4 4) ZnCl 2
A10. Kükürt (VI) oksit iki maddenin her biriyle reaksiyona girer
1) P 2 O 5 ve KOH 2) MgO ve SO 2 3) NaOH ve H 2 O 4) CO 2 ve Ba(OH) 2
A11. Hidroklorik asit iki maddenin her biriyle reaksiyona girer:
1) Cu(OH)2 ve Ag 2) NH3 ve CO 3) CaC03 ve Fe203 4) NaOH ve Hg
A12. Karbonik asit tuzları ile ilgili aşağıdaki ifadeler doğru mudur?
A. Alkali aşırı karbondioksitle reaksiyona girdiğinde karbonatlar oluşur.
B. Hidrokarbonların ısıtılması karbonatlar üretir.
1) yalnızca A doğrudur 2) yalnızca B doğrudur 3) her iki yargı da doğrudur 4) her iki yargı da yanlış
A13. Dönüşüm şemasında “X” ve “Y” maddeleri
1) X -HCl ve Y - Ca(OH)2
2) X - H2S04 ve Y - CaHPO 4
3) X - H2O ve Y - Ca(OH)2
4) X - Ca(OH)2 ve Y - CaH2
A14. Dimetil eterin izomeri:
1) metanal 2) metan 3) etanol 4) etilen
A15. Bir karbon tetraklorür molekülündeki σ bağlarının sayısı eşittir
1)1 2) 2 3) 3 4) 4
A16. Taze çökeltilmiş bakır (II) hidroksit aşağıdakilerle reaksiyona girer:
1) benzen 2) etanol 3) stiren 4) gliserin
A17. Hem formik hem de propiyonik asit aşağıdakilerle reaksiyona girer:
1) fenol 2) etanal 3) etanol 4) etil asetat
A18. Dönüşüm şemasında
"X" maddesi
1) 1,2-dibromoetan 2) bromoetan 3) 1,1-dibromoetan 4) asetilen
A19. Kimyasal reaksiyon türleriyle ilgili aşağıdaki ifadeler doğru mudur?
A. Sülfür (IV) oksidin oksijenle etkileşimi endotermik reaksiyon olarak sınıflandırılır.
B. Metanın ayrışması ekzotermik bir reaksiyon olarak sınıflandırılır
1) yalnızca A doğrudur 2) yalnızca B doğrudur 3) her iki yargı da doğrudur 4) her iki yargı da yanlış
A20. En hızlı reaksiyon hidroklorik asit ve
1) CaCO3 2) Zn 3) NaOH (çözelti) 4) Fe(OH) 3
A21. Sistemdeki denge değişimine ilişkin yargılar doğru mu: 2 NO (g) + O 2 (g) ⇄ 2 NO 2 (g) + Q?
A. Basınç arttıkça bu sistemdeki kimyasal denge reaksiyon ürününe doğru kayacaktır.
B. Nitrik oksit (II) konsantrasyonunun artmasıyla sistemin dengesi reaksiyon ürününe doğru kayacaktır.
1) yalnızca A doğrudur 2) yalnızca B doğrudur 3) her iki yargı da doğrudur 4) her iki yargı da yanlış
A22. Bir elektrolit iki maddenin her biridir:
1) baryum klorür, sodyum asetat
2) etanol, asetik asit
3) aseton, perklorik asit
4) brom, benzen
A23. İyon değişim reaksiyonları şunları içerir:
1) CH4 + Cl2 = CH3Cl + HC1
2) Zn + 2 HC1 = ZnCl 2 + H 2
3) KOH + HCl = KCl + H20
4) Cu(OH)2 = CuO + H20
A24. Redoks reaksiyonu aşağıdakiler arasındaki bir reaksiyondur:
1) Ca ve H 2 O 2) P 2 O 3 ve BaO 3) Cl 2 O 7 ve H 2 O 4) Al 2 O 3 ve Na 2 O
A25. tam hidrolize uğrar
1) alüminyum sülfür 2) sodyum sülfat 3) bakır (II) klorür 4) demir (III) nitrat
A26. Propan formülü aşağıdaki gibi olan bir maddeyle reaksiyona girer:
1) H 2 O 2) HCl 3) Cl 2 4) H 2
A27. Propanol-1 aşağıdaki etkileşimle oluşur:
1) Alkali (sulu çözelti) ile 1-kloropropan
2) alkali ile propen (sulu çözelti)
3) su ile propanal
4) su ile dikloropropan
A28. Bir kaptaki karbondioksit kullanılarak tespit edilebilir
1) hidroklorik asitle ıslatılmış çubuklar
2) yanan bir kıymık
3) ıslak fenolftalein kağıdı
4) kuru fenolftalein kağıdı
A29. Endüstride yalnızca erimiş tuzun elektrolizi ile elde edilebilir.
1) sodyum 2) çinko 3) krom 4) gümüş
A30. 1 mol amonyak gazının nitrojen oluşturmak üzere tamamen yanması için gereken oksijen hacmi (n.o.) eşittir
1) 12 l 2) 16,8 l 3) 18,4 l 4) 25,2 l
A31. Hem asit çözeltisiyle hem de alkali çözeltisiyle reaksiyona giren bir hidroksit
1) Mg(OH) 2 2) Cr(OH) 3 3) Ba(OH) 2 4) Ca(OH) 2
A32. Hem nitrik asit çözeltisi hem de sodyum hidroksit çözeltisi ile etkileşime girer.
1) magnezyum sülfat 2) amonyum sülfür 3) potasyum klorür 4) kurşun (II) bromür
A33. Dönüşüm şemasında “Y” maddesi
1) demir (III) sülfit 2) demir (II) sülfat 3) demir (III) sülfit 4) demir (III) sülfat
A34. Dietil eterin izomeri:
1) propanol-2 2) butanol-1 3) pentanol-2 4) heksanol-3
A35. Fenol molekülündeki oksijen atomu oluşur
1) iki σ bağı 2) bir σ bağı 3) bir σ ve bir π bağı 4) iki π bağı
A36. Kükürt iki maddenin her biriyle reaksiyona girer
1) O 2 ve SiO 2 2) Cl 2 ve NaCl 3) HCl ve N2 4) Fe ve H 2
Anahtar


