21.08.2020
При лечении бронхиальной астмы применяют ингаляционный глюкокортикостероид. Ингаляционные глюкокортикостероиды – наиболее эффективные и безопасные противовоспалительные препараты для лечения астмы
Согласно обзорным данным, по оценкам врачей, считается, что приблизительно 7 % американцев страдают бронхиальной астмой , , болезнь поражает людей всех рас и этнических групп во всем мире, от младенчества до старости, с небольшим преобладанием среди мальчиков а, после половой зрелости, среди женщин. Трагическое увеличение распространенности атопии и астмы, произошло за последние несколько десятилетий в Западных странах , а позднее в развивающихся , предполагают, что во всем мире астмой страдают около 300 миллионов человек
В 1970-ых и 1980-ых, в Соединенных Штатах, резко повысилось количество тяжелых обострений астмы (что отражено ростом посещаемости отделений экстренной помощи и госпитализаций по поводу астмы) и связанная с астмой смертность. Все же несмотря на постоянно высокую распространенность болезни, самые последние доступные данные указывают на улучшение показателей, и уменьшение количества ежегодных госпитализаций по поводу астматических приступов, и связанных с астмой смертельных случаев. Одно из возможных объяснений этих благоприятных тенденций - более широкое распространение профилактического использования ингаляционных кортикостероидов и внедрения за последние 10 - 15 лет новых, очень эффективных препаратов и улучшенных протоколов лечения астмы.
Обструкция дыхательных путей при астме и последующие симптомы в виде кашля, одышки, стеснения в груди, и хрипов вызваны несколькими факторами: спазмом гладкой мускулатуры дыхательных путей и воспалением бронхов. Спазм может быть тяжелым и приводить к опасному для жизни сужению и закрытию дыхательных путей, даже в отсутствие слизистого компонента. Этому может способствовать как ненормальное гладкомышечное сокращение , так и увеличение гладкомышечной массы . Воспаление дыхательных путей при астме включает слизистый, подслизистый и интерстициальный отек; клеточную инфильтрацию, особенно эозинофилами (и в некоторых случаях, нейтрофилами) и активированными лимфоцитами T-хелперами , а так же мастоцитами, которые (в отличие от мастоцитов при других эозинофильных болезнях дыхательных путей) инфильтрируют гладкомышечные пучки ; увеличение секреции в дыхательных путях, включая секретированную мокроту, слущеный эпителий, и внутрилюминальные эозинофилы; застой в капиллярах; гиперплазия гладких мышц; и оседание избыточного коллагена, особенно непосредственно под базальной мембраной эпителия ,
Традиционно, препараты, используемые для лечения астмы, были классифицированы по категориям согласно их преобладающему эффекту - расслабление гладких мышц дыхательных путей (бронходилататоры) и подавление воспаления дыхательных путей(противовоспалительные препараты). Более новые лекарства (например, модификаторы лейкотриена) и сочетания лекарств (например, ингаляционные кортикостероиды, комбинированные с b-агонистами пролонгированного действия), имеют двойной эффект, в противовес такой традиционной дихотомии. Теперь, лекарства от астмы классифицированы согласно их ролям в целостном контроле над астмой (короткого и пролонгированного действия), эта модель особенно полезна, при обсуждении с пациентами их лекарств от астмы.
У всех пациентов с астмой должен быть доступный бронходилататор короткого действия для использования по необходимости. Общепринято, что, когда быстро действующие бронходилататоры необходимы для облегчения симптомов больше чем 2 раза в неделю (или более двух раз месяц при ночных пробуждениях вызванных астматическими симптомами), должны быть назначены контролирующие препараты. ,
Препараты короткого действия.
b-агонисты короткого действия, применяемые ингаляционно, являются самой эффективной терапией для быстрого купирования обструкции дыхательных путей и облегчения астматических проявлений. Наиболее широко используемые препараты короткого действия, b2-селективные адреномиметики: альбутерол (обычно известный как вне Соединенных Штатов), левальбутерол, и пирбутерол ). Метапротеренол, поставляемый в ДАИ (дозированный аэрозольный ингалятор (eng. metered-dose inhaler (MDI)), был недавно снят с производства.
Табл. 1. b - Адреномиметики короткого действия.
Все быстродействующие b-агонисты, начинают действовать через 5 минут или меньше, с пиковым эффектом через 30 - 60 минут, продолжительность действия 4 - 6 часов . При регулярном использовании бронходилататоров (четыре и более раз ежедневно), потенциальная эффективность (измеряемая увеличением максимального выдыхаемого потока) не уменьшается, но продолжительность действия несколько сокращается , . Поскольку регулярный график приема четыре раза в день не улучшает результаты, в сравнении с приемом по необходимости (и у пациентов с определенным генотипическим вариантом b-рецепторов, может иметь вредный эффект), , b -агонисты короткого действия рекомендуются для использования только при необходимости для облегчения симптомов (или перед ожидаемым воздействием известных астмогенных факторов). Практика введения b-агонистов короткого действия прежде, чем использовать ингаляционные кортикостероиды, чтобы улучшить доставку кортикостероида к более низким дыхательным путям была отбракована как несостоятельная . Точно так же нет никакой необходимости пациенту ждать больше чем 10 - 15 секунд между ингаляциями, когда необходима доза в две и более ингаляции
У пациентов с умеренной и тяжелой обструкцией дыхательных путей, на лог-линейной кривой зависимости «доза-ответ», можно продемонстрировать, необходимость больших доз, для бронходилатации b-агонистами короткого действия (до 4000 µg альбутерола из ДАИ). Приходится часто сталкиваться с дозозависимыми побочными эффектами симпатомиметиков, такими как тремор, беспокойство, сердцебиение, и тахикардия (без гипертензии), также может быть выявлено небольшое зависимое от дозы уменьшение уровня калия и магния в сыворотке крови. Однако, при обычной дозе (две ингаляции за один раз), неприятные побочные эффекты встречаются редко. Но и их эффективность может быть снижена, в тех случаях, когда пациенты одновременно принимают бетта-блокаторы. ,
Решение, о том, какой из b-агонистов короткого действия использовать базируется в значительной степени на стоимости и предпочтении пациента и врача. Пирбутерол доступен в активируемом вдохом дозированном аэрозольном ингаляторе (ДАИ-АВ) - устройстве созданном для оптимизации доставки препарата, путем впрыскивания препарата только в момент инициализации вдоха. Левальбутерол, очищенный D-вращающий изомер альбутерола, был создан с целью устранения побочных эффектов, которые, по некоторым данным, свойственны только S-вращающим изомерам . Однако, при использовании левальбутерола в ДАИ профиль эффективность и побочных эффектов, неотличим от такового у рацемической смеси молекул в альбутероле. Сейчас альбутерол стал доступен в ДАИ, и не содержит хлорофторокарбон (CFCs), а CFC-содержащие альбутерол ингаляторы были сняты с производства 31 декабря, 2008. Как и CFC, альтернативный пропилент, гидрофтороалкан (HFA), инертен в дыхательных путях человека, но в отличие от CFC не способствует истощению стратосферного озонового слоя. Ингаляторы HFA - эквивалентны с CFC-содержащими ингаляторами, и могут использоваться со спейсерами у пациентов с плохой техникой ингаляции. Они обеспечивают бронходилатацию, сопоставимую с альбутеролом в небулайзере, если необходимое число вдохов регламентировано, и техника ингаляций довольно хорошая.
b-агонисты короткого действия для перорального приема в таблетках или в жидкой форме нежелательны, несмотря на их кажущееся удобство (особенно для маленьких детей). Они начинают действовать позже, являются более слабыми, и чаще, чем ингаляционные формы, вызывают побочные эффекты. Точно так же, антихолинергические бронходилататоры, такие как ипратропиум не рекомендованы (и не одобрены Управлением по контролю за продуктами и лекарствами ) для быстрого купирования симптомов астмы. Они позже (через 20 - 30 минут) начинают действовать и вызывают более слабую бронходилатацию, чем ингаляционные b - бронходилататоры Антихолинергические бронходилататоры должны использоваться только в редких случаях у пациентов с непереносимостью ко всем b – миметикам, или для лечения тяжелого астматического приступа , или астматических приступов, вызванных бетта-блокаторами.
Новый подход к лечению астмы, еще не принятый в Соединенных Штатах, предлагает комбинировать b - агонисты с ингаляционными кортикостероидами в одном флаконе, для купирования симптомов по мере необходимости. Использование такой комбинации приводило к более благоприятным последствиям у пациентов с умеренной астмой, по сравнению с использованием монотерапии альбутеролом по необходимости. Точно так же пролонгированный b-агонист с быстрым началом действия () используется в комбинации с ингаляционным кортикостероидом в одном ингаляторе для поддерживающей и экстренной терапии одновременно , безопасность этого подхода в широкой и разнородной группе населения ждет своего доказательства.
Долгосрочный Контроль.
Достижение хорошего долгосрочного контроля над астмой (нечастые астматические симптомы, неограниченный уровень деятельности, нормальная или почти нормальная функция легких, и редкие астматические приступы, требующие неотложной помощи), требует многогранного подхода: ограничение экологических факторов, которые могут вызвать бронхоконстрикцию, и острое или хроническое воспаление дыхательных путей; контроль изменений в активности болезни; в некоторых случаях, иммунотерапия; и медикаментозное лечение. Использование контролирующих препаратов должно быть расширено, пока не будет достигнут хороший контроль над астмой, включая сокращение числа астматических приступов, требующих системных кортикостероидов до одного в год максимум. Ингаляционные кортикостероиды составляют класс наиболее эффективных препаратов, позволяющих пациентам достигнуть хорошего уровня контроля над астмой.
Ингаляционные кортикостероиды.
Кортикостероиды оказались эффективными при лечении астмы, поскольку они эффективны при многих других воспалительных болезнях, из-за разнообразного противовоспалительного действия, включая множественный эффект на транскрипцию (как усиление, так и ослабление) многих генов , . В биоптатах дыхательных путей астматиков, у которых проводилась длительная терапия ингаляционными кортикостероидами, гистологические отклонения, типичные для астмы, оказались менее выражены. Изменения включают уменьшение количества мастоцитов, эозинофилов, T-лимфоцитов, и дендритных клеток в слизистом и подслизистом слоях ; уменьшение гиперплазии бокаловидных клеток и повреждения эпителиальных клеток ; уменьшение васкуляризации.
Наряду с подавлением воспаления дыхательных путей, неспецифическая бронхиальная гиперреактивность обычно уменьшается . Положительные клинические результаты включают уменьшение астматических симптомов, увеличение функции легких, улучшение астма - специфичного качества жизни, и сокращение астматических приступов, включая тяжелые, приводящие к госпитализации или смерти . Наряду с оптимистическими предсказаниями, надежных свидетельств указывающих на возможность предотвратить, при долгосрочном применении ингаляционных кортикостероидов, прогрессивное снижение функции легких, наблюдаемое у некоторых пациентов с астмой, по большей части недостает , . Ингаляционные стероиды подавляют, но не излечивают астматическое воспаление: в фазе стабилизации болезни, маркеры воспаления дыхательных путей(например, концентрация выдыхаемого оксида азота и эозинофилов в мокроте), и бронхиальная гиперреактивность возвращаются к исходному уровню спустя приблизительно 2 недели после того, как использование ингаляционных кортикостероидов было прекращено. ,
Не всем пациентам одинаково помогают ингаляционные кортикостероиды. Например, курильщики, менее вероятно, получат тот же самый антиастматический эффект, что и некурящие . Нейтрофильное воспаление дыхательных путей менее вероятно ответит на лечение так же, как эозинофильное воспаление. Генетические различия у людей с астмой могут также стать причиной невосприимчивости к кортикостероидам.
Большинство доступных в настоящее время ингаляционных кортикостероидов, после проглатывания и системного всасывания в желудочно-кишечном трактате, подвергается обширной первичной метаболической инактивации в печени прежде, чем достигнет системного кровотока . К тому же, из-за того, что менее 20 % поступившей дозы сохраняется в дыхательных путях, только небольшое количество может всасываться через слизистую оболочку дыхательных путей. С использованием изменений в гипоталамическо-гипофизарно-надпочечной функции в качестве испытания, системный эффект может быть отмечен при введении ингаляционного кортикостероида в таких дозах как 88 µg флутикозона в день . Однако, фактически никакие клинически важные, долгосрочные неблагоприятные системные эффекты не наблюдаются среди взрослых, принимающих низкие и средние дозы этих препаратов. При больших дозах (обычно > 1000 µg беклометазона или его эквивалента в день), риск поражения кожи, катаракты , повышения внутриглазного давления, и ускорения потери костной массы увеличивается. У детей отмечается замедление роста. Ожидаемая задержка роста в среднем приблизительно на 1 см за первый год после назначения ребенку ингаляционных кортикостероидов, , , но данные исследований у детей в препубертатном и школьном возрасте свидетельствуют, что, даже когда эти дети продолжают длительно получать ингаляционные кортикостероиды, они в конечном счете достигают своего нормального предполагаемого роста , .
Глоточные и гортанные побочные эффекты ингаляционных кортикостероидов включают изъязвление гортани, кашель при ингаляции препаратов, слабый или хриплый голос, и кандидоз. Полоскание рта после каждого применения препарата и использование спейсера с ДАИ - это методы, которые помогают минимизировать риск развития кандидоза в полости рта. (Использование спейсера с ДАИ также уменьшает количество препарата, который может всосаться в ротоглотке.) Кашель обычно можно преодолеть, изменив кортикостероид или ингаляционную систему. Дисфония, вообще неустойчивый симптом, как полагают, возникает из-за отёка гортани и утолщения слизистой оболочки или, возможно, миопатии 57 . Это обычно проходит с временным прекращением лечения или после изменения поколения аэрозоля и образца доставки (например, переключаясь от ингалятора сухого порошка до ДАИ со спейсером).
Когда для лечения астмы в середине 1970-ых, был впервые представлен, ингаляционный кортикостероид , он назначался четыре раза в день, и каждый вдох препарата из ДАИ, проданного в Соединенных Штатах, содержал только 42 µg гормона. С тех пор, стали доступны и другие кортикостероиды, включая более мощные, доставляющие большую дозу за ингаляцию, и назначаемые один – два раза в день, что способствовало улучшению эффективности и удобству ).
Табл. 2. Ингаляционные кортикостероиды.
У каждого из ингаляционных кортикостероидов есть свои особенности , . По большей части, выбор основан на удобстве приема (один – два раза в день) и методе доставки (ДАИ, ингалятор сухого порошка, или раствор для небулайзера), стартовой дозы и гибкости в контроле дозы, стоимости препарата, и имеющихся побочных эффектов. Однако в терапевтическом действии были найдены лишь незначительные различия.
Использование ингаляционных кортикостероидов в больших дозах оказалось эффективным в лечении тяжелой персистирующей астмы . Однако, кривая «доза – ответ» (на основе потока выдоха), для ингалированных кортикостероидов является относительно пологой, тогда как кривая системного поглощения дозы, оказалась, более линейной . В результате, более приемлемыми оказались стратегии, при которых можно достигнуть контроля над астмой, не используя большие дозы ингаляционных кортикостероидов, и сокращая их дозы у пациентов с хорошо управляемой астмой (так называемое "понижение" терапии) может часто быть достигнуто, без уменьшения контроля над астмой .
Ингаляционные b-адреномиметики пролонгированного действия.
Ингаляционные b-адреномиметики пролонгированного действия, сальметерол и формотерол ( и ), в значительной степени заменили более ранние бронходилататоры длительного действия - пероральные, медленно высвобождающиеся альбутерол и теофиллин. b-Адреномиметики пролонгированного действия - мощные бронходилататоры (с бронходилатирующим эффектом как у b-агонистов короткого действия), сохраняют активность более 12 часов, и из-за их высокой b-2 адреноселективности, обладают малым количеством побочных эффектов (в основном мягкие симпатомиметические эффекты, такие как единичные миоклонии и тахикардия). . Они не взаимодействуют с пищей и другими препаратами, в отличие от теофиллина, что усложняет его использование, и токсичность при передозировании препарата чрезвычайно редка, в отличие от таковой у теофиллина.
Табл. 3. Ингаляционные b-адреномиметики пролонгированного действия.
Как у b-агонистов с коротким действием, регулярное использование b-адреномиметиков пролонгированного действия - проявляется только в умеренной тахифилаксии и максимальном бронходилатирующем эффекте с более длительным сохранением активности этих препаратов . Напротив, бронхопротективный эффект при использовании b-адреномиметиков пролонгированного действия (то есть, предотвращение бронхоконстрикции вызванной физической нагрузкой) быстро уменьшается при регулярном использовании, , противоположный фармакологический эффект, который не был полностью объяснен. За редким исключением быстрое купирование приступов, обеспечиваемое b-адреномиметиками с коротким действием не тормозится у b-адреномиметиков длительного действия при регулярном их использовании. Вариации структуры b - адренергических рецепторов, обусловленные генетическим полиморфизмом, которые распространены в американском населении (15 - 20 %), может снизить эффективность b - агонистов длительного действия у некоторых пациентов .
Факт, что b-адреномиметики пролонгированного действия могут обеспечить улучшение функции легких, может заставить клиницистов использовать их в качестве долгосрочного лечения без совместного использования ингаляционного кортикостероида с противовоспалительным действием. Однако эта стратегия приводит к персистированию воспаления дыхательных путей и неприемлемо высокой частоте астматических приступов . Ингаляционные b-адреномиметики пролонгированного действия не должны использоваться без соответствующей противовоспалительной терапии для лечения астмы.
Как дополнительная или комбинированная терапия с ингаляционными кортикостероидами, b-адреномиметики пролонгированного действия оказались эффективными для сокращения дневных и особенно ночных симптомов, улучшения функции легких, сокращения риска приступов, и уменьшения необходимой дозы ингаляционных кортикостероидов . Сравнение использования ингаляционных кортикостероидов в комбинации с b-адреномиметиками пролонгированного действия и использования более высоких доз одних только ингаляционных кортикостероидов показывает, что комбинированная терапия дает более благоприятные результаты (на фоне более низкой дозы кортикостероидов). , Фармакологические данные подбивают теоретическую основу для благоприятного взаимодействия между этими двумя классами препаратов: лабораторные исследования показали, что кортикостероиды улучшают b – рецептор - опосредованную передачу сигналов в легких, и b-агонисты увеличивают транскрипцию генов под влиянием кортикостероидов . Комбинированная терапия (b-адреномиметики пролонгированного действия, объединенные с кортикостероидом в одном ингаляторе) () гарантирует совместное использование противовоспалительного препарата и оптимизирует комплаентность из-за большего удобства. Её главное неудобство – в том, что, регулируя дозу ингаляционных кортикостероидов, не изменяя дозу b – миметиков (например, увеличение дозы кортикостероида во время астматического приступа) требует смены устройства или наличия отдельного ингаляционного кортикостероида.
Жизненно важная выгода, которую многие пациенты с умеренной или тяжелой персистирующей астмой почувствовали при использовании b-адреномиметика пролонгированного действия вместе с ингаляционным кортикостероидом, должна быть противопоставлена результатам мультицентрового исследования применения сальметерола при астме (Salmeterol Multicenter Asthma Research Trial - SMART) , по результатам которого добавление b-адреномиметика пролонгированного действия к "обычной терапии" может вызывать увеличение риска фатальных или почти фатальных астматических приступов, по сравнению с "обычной терапией". Было показано, что в большинстве случаев при SMART не использовали ингаляционные кортикостероиды, а среди пациентов, принимающих b-адреномиметики пролонгированного действия и ингаляционные кортикостероиды , ни о каком увеличении связанной с астмой смертности ни разу не сообщалось. Тем не менее, механизм, благодаря которому сальметерол вызывал увеличение числа связанных с астмой смертельных случаев, как среди черных, так и белых исследуемых, остается неясным, и поэтому везде в аннотациях и на коробках всех препаратов содержащих сальметерол или формотерол содержится предупреждение. Кроме того, национальные и международные экспертные группы, рекомендовали использование b-адреномиметиков пролонгированного действия только у пациентов, у которых ингаляционные кортикостероиды сами по себе либо не позволяют достигнуть хорошего контроля над астмой, либо для начальной терапии, если не ожидается, что она даст хороший результат. Будущие руководящие принципы в лечении астмы должны взять на вооружение соответствующее заключение по недавним наблюдениям, что прием b-адреномиметиков пролонгированного действия в комбинации с ингаляционным кортикостероидом один раз в день, обеспечивает хороший контроль у пациентов с легкой персистирующей астмой .
Оба b-адреномиметика пролонгированного действия отличаются свойствами, как в практическом, так и теоретическом плане , начало действия формотерола через 5 минут, также, как у b-агонистов короткого действия, тогда как у сальметерола начало действия более медленное (15 - 20 минут). Поэтому в некоторых странах, кроме Соединенных Штатов, комбинация формотерол – ингаляционный кортикостероид в одном ингаляторе рекомендуется и для быстрого купирования приступа и, для регулярного использования, при долгосрочном контроле . Формотерол - полный агонист b - адренорецепторов, тогда как сальметерол - частичный агонист (и частичный антагонист). Значение этого фармакологического различия, особенно в отношении риска фатальных астматических приступов, сомнительно.
Модификаторы Лейкотриена.
Антагонисты рецепторов цистеинил лейкотриенов: , и пранлукаст (последний, не доступен в Соединенных Штатах) ), блокируют действие лейкотриена C4, D4, и E4 в рецепторах цистеинил лейкотриена 1 типа . Бронходилатация происходит в течение нескольких часов после первой дозы, а максимальный эффект проявляется в течение первых нескольких дней после начала применения , . Уровень циркулирующих в крови эозинофилов при лечении антагонистами рецепторов лейкотриенов уменьшается , . . Однако, при использовании косвенных показателей воспаления дыхательных путей(например, количество эозинофилов в мокроте и уровень выдыхаемого оксида азота) для определения результатов, эффект антагонистов рецепторов лейкотриенов на воспаление дыхательных путей, по сравнению с плацебо, оказался вариабельным , , .
Табл. 4. Модификаторы Лейкотриена.
Антагонисты рецепторов лейкотриенов можно принимать в таблетках однократно (в случае монтелукаста) или дважды (в случае зафирлукаста) в день. Монтелукаст доступен в жевательных таблетках и пероральных гранулах (для подмешивания в пищу) для маленьких детей. Рекомендация принимать монтелукаст один раз в день вечером была основана на выборе времени его применения в оригинальных испытаниях, представленных FDA во время заявки на одобрение препарата. Однако никакие данные не указывают на большую выгоду при приеме вечером, по сравнению с приемом в любое другое время дня .
Зилеутон тормозит продукцию цистеинил лейкотриенов (и лейкотриена B4, мощного хемокина для нейтрофилов), так как является антогонистом 5-липооксигеназы. Сейчас широко распространено мнение, что принимать его нужно два раза в день. Не проводилось клинических испытаний, непосредственно сравнивающих эффективность зилеутона по сравнению с антагонистами лейкотриеновых рецепторов или эффективности их совместного использования. Некоторые клиницисты находят зилеутон более предпочтительным, чем антагонисты лейкотриеновых рецепторов при астматической триаде (астма, непереносимость аспирина, и носовой полипоз), и для контроля астмы и с точки зрения сокращения носовых полипов .
Зилеутон вызывает обратимый токсический гепатит в 2 - 4 % случаев. Функция печени должна контролироваться ежемесячно в течение первых 3 месяцев терапии, каждые 3 месяцах до конца первого года, и периодически после того. Сообщения о появлении синдрома Чарга-Стросса (эозинофильный васкулит и грануломатоз осложняющий течение астмы) у пациентов недавно начавших антагонисты лейкотриеновых рецепторов (часто с сопутствующим уменьшением оральных кортикостероидов) , , может отражать усугубление уже существовавшего ранее синдрома- Чарга-Стросса , , хотя возможность причинной связи остается спорной . Вообще, антагонисты лейкотриеновых рецепторов считали фактически свободными от побочных эффектов, а один (монтелукаст) был даже одобрен для применения при астме у детей до года. В недавних постмаркетинговых сообщениях описаны несколько случаев, когда монтелукаст вызывал у детей депрессию и суицидальные наклонности. Но никакого тому подтверждения установлено не было, и при просмотре всех доступных данных плацебо-контролируемых клинических испытаний, FDA не нашел увеличения риска суицидальных наклонностей или самоубийства у какого-либо из лейкотриеновых модификаторов. Возможность изменений настроения и поведения под действием этих препаратов изучается.
Из-за осознания их безопасности и удобства, антагонисты лейкотриеновых рецепторов в значительной степени заменили кромогликаты (кромолин и недокромил) как некортикостероидные препараты выбора, особенно у маленьких детей, у которых лечение аэрозолем часто затруднено. Кромолин требует четырех разового применения ежедневно при помощи ДАИ или небулайзера, обеспечивая достаточно ограниченный долгосрочный контроль за астмой и, в отличие от антагонистов лейкотриеновых рецепторов, дополнительной выгоды от его использования в комбинации с ингаляционными кортикостероидами замечено не было.
Краткосрочные, двойные слепые, плацебо контролируемые исследования выявили улучшение функции легких, улучшение, в анкетных опросах, связанного с астмой качества жизни, и уменьшение астматических приступов у пациентов принимающих модификаторы лейкотриена. , , , Особенно выгодным лечение лейкотриеновыми модификаторами может быть у людей с ожирением , курильщиков , и при повышенной чувствительности к аспирину , , . В будущем идентификация определенных индивидуальных особенностей генов кодирующих ферменты метаболического пути лейкотриена может оказаться клинически полезной для предсказания эффективности лечения у конкретного пациента. В настоящее время, часто используется терапевтическое испытание; если имеет место улучшение симптоматики и объективных данных, то обычно это наблюдается в течение первого месяца после начала терапии.
В целом, ингаляционные кортикостероиды обеспечивают лучший контроль над астмой чем лейкотриеновые модификаторы , , , , . В результате, ингаляционные кортикостероиды рекомендуются как препараты первого выбора в лечении пациентов с персистирующей астмой, включая детей всех возрастов. Антагонисты лейкотриеновых рецепторов являются альтернативой в лечении легкой персистирующей астмы. Пациентам любого возраста, у которых не достигнут хороший контроль над астмой от использования лейкотриеновых модификаторов, показан переход к ингаляционным кортикостероидам. У пациентов с более тяжелой астмой добавление антагониста лейкотриеновых рецепторов к низкой дозе ингаляционного кортикостероида может улучшить контроль над астмой, , но другие терапевтические комбинации (а именно, ингаляционные кортикостероиды плюс b - агонисты длительного действия) более эффективны ,
Терапия Anti-IgE.
Anti-IgE моноклональные антитела, омализумаб, являются первыми биологическими иммунорегулирующими агентами, доступными, для лечения астмы. Они связывают ту часть IgE, к которой имеют высокое сродство рецепторы (Fc R1) на поверхности тучных клеток и базофилов. При внутривенном введении, омализумаб уменьшает уровень циркулирующего IgE на 95 %, а уровень свободного IgE, может привести к 10 IU на миллилитр или меньше, целевая идея - клинически значимое торможение аллергических реакций в дыхательных путях . Его использование также приводит к снижению экспрессии рецепторов (Fc R1) на поверхности мастоцитов и других иммунорегулирующих клеток (базофилы, моноциты, и дендритные клетки). В отличие от гипосенсибилизирующей иммунотерапии, лечение омализумабом не ограничивается действием на какой-то определенный аллерген или группу аллергенов.
Омализумаб назначается подкожно каждые 2 или 4 недели, в зависимости от дозы. Доза рассчитывается в зависимости от веса пациента и уровня IgE в крови. Местные аллергические реакции (по типу крапивницы), встречаются редко, а системные аллергические реакции (то есть, анафилаксия) возможны у 1 - 2 пациентов из 1000. Большинство, но не все, системные реакции отмечаются в течение 2 часов после введения первых нескольких доз. Пациентов просят остаться под медицинским наблюдением в течение 2 часов после каждой из их первых трех инъекций и в течение 30 минут после каждой последующей инъекции и в течение последующих 24 часов, носить с собой предварительно заполненный адреналин - содержащий автоинжектор для самоприменения при необходимости.
Омализумаб показан для лечения умеренной и тяжелой персистирующей астмы, если ингаляционные кортикостероиды, b-агонисты длительного действия и лейкотриеновые модификаторы не обеспечили адекватный контроль, или не могут использоваться из-за невыносимых побочных эффектов. В настоящее время одобряемый диапазон дозирования для омализумаба ограничен применением у пациентов с уровнем IgE в крови от 30 до 700 IU на миллилитр; зарегистрированное повышение чувствительности к постоянному аэроаллергену (например, пыль, перхоть животных, плесень, тараканы) является дополнительным критерием выбора.
Омализумаб был одобрен для использования у взрослых и детей старше 12 лет. Для пациентов в этом возрастном диапазоне препарат, как оказалось, не изменяет болезни, в том смысле, что не предотвращает отдаленные изменения в функции легких и не приводит к ремиссии заболевания (что означает приостановление без повторения астматических симптомов). Лечение омализумабом, как выяснилось, уменьшало частоту астматических приступов, даже среди пациентов, уже принимающих много других препаратов. У пациентов, принимающих только ингаляционный кортикостероид, добавление омализумаба, по сравнению с плацебо, позволяло значительно снизить дозу кортикостероида, с сохранением или некоторым улучшением легочной функции и уменьшением потребности в спасательном бронходилататоре , .
Один из самых больших недостатков, для более широко распространения использования омализумаба это стоимость, примерно от 10 000$ до 30 000$ ежегодно только за один препарат. Фармакогенетические маркеры, прогнозирующие благоприятное действие препарата, были бы очень желательны, учитывая большую стоимость терапевтического испытания, длящегося 4 - 6 месяцев. Наблюдения до настоящего времени показывают, что традиционные клинические данные в исходной точке не могут достоверно предсказать, у каких пациентов будет ответ на anti-IgE терапию.
Заключение.
Если бронхиальная астма проявляется нечастыми, кратковременными и легкими симптомами, эпизодическое применение быстро действующего бронходилататора, чтобы снять спазм гладкой мускулатуры дыхательных путей, является вполне приемлемым подходом. Однако когда симптомы становятся более частыми и более тяжелыми, акцент делается на предотвращение симптомов (и астматических приступов) ). Для подавления воспаления дыхательных путей, назначаются ингаляционные кортикостероиды, используемые один или два раза в день, и уменьшающие частоту эпизодов бронхоконстрикции и риск астматических приступов. В низких и средних дозах ингаляционные кортикостероиды, безопасны при долгосрочном использовании, даже у маленьких детей. Альтернатива кортикостероидам при легкой астме - антагонисты лейкотриеновых рецепторов, которые направлены на блокирование специфического для астмы воспалительного медиатора. Противогриппозная, и возможно, противопневмококковая вакцины показаны пациентам, на фоне регулярной антиастматической терапии. ,
Рисунок 1. Ступенчатый подход к терапии астмы.
Этот упрощенный ступенчатый подход к лечению астмы, разработан на основе центральной роли ингаляционных кортикостероидов. Для каждой из наложившихся ступеней доза ингаляционного кортикостероида может быть подогнана до необходимой для достижения хорошего управления астмой, на фоне минимизации долгосрочных рисков, связанных с большими дозами. LABA означает b-агонист длительного действия (long-acting b-agonist), LTM - лейкотриеновый модификатор, LTRA - антагонист лейкотриеновых рецепторов, и SABA - b-агонисты короткого действия (short-acting b-agonist).
Когда симптомы сохраняются, несмотря на лечение, комплаентность и хорошую технику ингаляции, использование b-агонистов длительного действия в комбинации с ингаляционными кортикостероидами, показало себя самым эффективным следующим шагом, поскольку воздействует на оба аспекта сужения дыхательных путей при астме: бронхоконстрикцию и воспаление дыхательных путей. Новая возможность для пациентов с рефрактерной аллергической астмой - терапия моноклональными anti-IgE антителами.
Контроль за астмой может часто достигаться при увеличении дозы ингаляционных кортикостероидов. Однако при больших дозах и долгосрочном воздействии возрастает потенциальный риск побочных эффектов. Таким образом, как только контроль за астмой был достигнут на период от 3 до 6 месяцев, должны быть предприняты усилия, чтобы уменьшить дозу ингаляционных кортикостероидов до средней или низкой. Использование b-агонистов длительного действия, лейкотриеновых модификаторов, и anti-IgE терапия может облегчить снижение дозы ингаляционных кортикостероидов, на фоне надлежащего контроля над астмой.
References
- The state of asthma in America: Asthma in America survey. (Accessed February 9, 2009)
- Expert panel report 3: guidelines for the diagnosis and management of asthma. Bethesda, MD: National Heart, Lung, and Blood Institute, August 2007. (NIH publication no. 07-4051.) (Accessed February 9, 2009,)
- Wilson DH, Adams RJ, Tucker G, Appleton S, Taylor AW, Ruffin RE. Trends in asthma prevalence and population changes in South Australia, 1990-2003. Med J Aust 2006;184:226-229.
- Pearce N, Aït-Khaled N, Beasley R, et al. Worldwide trends in the prevalence of asthma symptoms: phase III of the International Study of Asthma and Allergies in Childhood (ISAAC). Thorax 2007;62:758-766.
- Beasley R. The Global Burden of Asthma Report. In: Global Initiative for Asthma (GINA). 2004. (Accessed February 9, 2009)
- Epidemiology and Statistics Unit. Trends in asthma morbidity and mortality. New York: American Lung Association, August 2007. (Accessed February 9, 2009)
- Shore SA. Airway smooth muscle in asthma -- not just more of the same. N Engl J Med 2004;351:531-532.
- Johnson PR, Roth M, Tamm M, et al. Airway smooth muscle cell proliferation is increased in asthma. Am J Respir Crit Care Med 2001;164:474-477.
- Azzawi M, Bradley B, Jeffery PK, et al. Identification of activated T lymphocytes and eosinophils in bronchial biopsies in stable atopic asthma. Am Rev Respir Dis 1990;142:1407-1413.
- Brightling CE, Bradding P, Symon FA, Holgate ST, Wardlaw AJ, Pavord ID. Mast-cell infiltration of airway smooth muscle in asthma. N Engl J Med 2002;346:1699-1705.
- Elias JA, Zhu Z, Chupp G, Homer RJ. Airway remodeling in asthma. J Clin Invest 1999;104:1001-1006.
- James AL, Wenzel S. Clinical relevance of airway remodelling in airway diseases. Eur Respir J 2007;30:134-155.
- Global strategy for asthma management and prevention. Global Initiative for Asthma (GINA), 2007. (Accessed February 9, 2009)
- Nelson HS. b-Adrenergic bronchodilators. N Engl J Med 1995;333:499-506.
- Lipworth BJ, Struthers AD, McDevitt DG. Tachyphylaxis to systemic but not to airway responses during prolonged therapy with high dose inhaled salbutamol in asthmatics. Am Rev Respir Dis 1989;140:586-592.
- Repsher LH, Anderson JA, Bush RK, et al. Assessment of tachyphylaxis following prolonged therapy of asthma with inhaled albuterol aerosol. Chest 1984;85:34-38.
- Drazen JM, Israel E, Boushey HA, et al. Comparison of regularly scheduled with as-needed use of albuterol in mild asthma. N Engl J Med 1996;335:841-847.
- Israel E, Drazen JM, Liggett SB, et al. The effect of polymorphisms of the beta(2)-adrenergic receptor on the response to regular use of albuterol in asthma. Am J Respir Crit Care Med 2000;162:75-80.
- Israel E, Chinchilli VM, Ford JG, et al. Use of regularly scheduled albuterol treatment in asthma: genotype-stratified, randomised, placebo-controlled cross-over trial. Lancet 2004;364:1505-1512.
- Mackay AD, Dyson AJ. How important is the sequence of administration of inhaled beclomethasone dipropionate and salbutamol in asthma? Br J Dis Chest 1981;75:273-276.
- Lawford P, McKenzie D. Pressurized aerosol inhaler technique: how important are inhalation from residual volume, inspiratory flow rate and the time interval between puffs? Br J Dis Chest 1983;77:276-281.
- Salpeter SR, Ormiston TM, Salpeter EE. Cardioselective beta-blockers in patients with reactive airway disease: a meta-analysis. Ann Intern Med 2002;137:715-725.
- Doshan HD, Rosenthal RR, Brown R, Slutsky A, Applin WJ, Caruso FS. Celiprolol, atenolol and propranolol: a comparison of pulmonary effects in asthmatic patients. J Cardiovasc Pharmacol 1986;8:Suppl 4:S105-S108.
- Henderson WR Jr, Banerjee ER, Chi EY. Differential effects of (S)- and (R)-enantiomers of albuterol in a mouse asthma model. J Allergy Clin Immunol 2005;116:332-340.
- Berger WE, Milgrom H, Skoner DP, et al. Evaluation of levalbuterol metered dose inhaler in pediatric patients with asthma: a double-blind, randomized, placebo- and active-controlled trial. Curr Med Res Opin 2006;22:1217-1226.
- Hendeles L, Colice GL, Meyer RJ. Withdrawal of albuterol inhalers containing chlorofluorocarbon propellants. N Engl J Med 2007;356:1344-1351.
- Ramsdell JW, Colice GL, Ekholm BP, Klinger NM. Cumulative dose response study comparing HFA-134a albuterol sulfate and conventional CFC albuterol in patients with asthma. Ann Allergy Asthma Immunol 1998;81:593-599.
- Newman SP. Spacer devices for metered dose inhalers. Clin Pharmacokinet 2004;43:349-360.
- Cates CJ, Crilly JA, Rowe BH. Holding chambers (spacers) versus nebulizers for beta-agonist treatment of acute asthma. Cochrane Database Syst Rev 2006;2:CD000052-CD000052.
- Nathan RA. Beta 2 agonist therapy: oral versus inhaled delivery. J Asthma 1992;29:49-54.
- Rebuck AS, Chapman KR, Abboud R, et al. Nebulized anticholinergic and sympathomimetic treatment of asthma and chronic obstructive airways disease in the emergency room. Am J Med 1987;82:59-64.
- Rodrigo GJ, Castro-Rodriguez JA. Anticholinergics in the treatment of children and adults with acute asthma: a systematic review with meta-analysis. Thorax 2005;60:740-746.
- Papi A, Canonica GW, Maestrelli P, et al. Rescue use of beclomethasone and albuterol in a single inhaler for mild asthma. N Engl J Med 2007;356:2040-2052.
- O"Byrne PM, Bisgaard H, Godard PP, et al. Budesonide/formoterol combination therapy as both maintenance and reliever medication in asthma. Am J Respir Crit Care Med 2005;171:129-136.
- Rabe KF, Atienza T, Magyar P, Larsson P, Jorup C, Lalloo UG. Effect of budesonide in combination with formoterol for reliever therapy in asthma exacerbations: a randomised controlled, double-blind study. Lancet 2006;368:744-753.
- Barnes PJ. How corticosteroids control inflammation: Quintiles Prize Lecture 2005. Br J Pharmacol 2006;148:245-254.
- van der Velden VH. Glucocorticoids: mechanisms of action and anti-inflammatory potential in asthma. Mediators Inflamm 1998;7:229-237.
- Chanez P, Bourdin A, Vachier I, Godard P, Bousquet J, Vignola AM. Effects of inhaled corticosteroids on pathology in asthma and chronic obstructive pulmonary disease. Proc Am Thorac Soc 2004;1:184-190.
- Lundgren R, Söderberg M, Hörstedt P, Stenling R. Morphological studies of bronchial mucosal biopsies from asthmatics before and after ten years of treatment with inhaled steroids. Eur Respir J 1988;1:883-889.
- Feltis BN, Wignarajah D, Reid DW, Ward C, Harding R, Walters EH. Effects of inhaled fluticasone on angiogenesis and vascular endothelial growth factor in asthma. Thorax 2007;62:314-319.
- Haahtela T, Järvinen M, Kava T, et al. Comparison of a b 2 -agonist, terbutaline, with an inhaled corticosteroid, budesonide, in newly detected asthma. N Engl J Med 1991;325:388-392.
- Donahue JG, Weiss ST, Livingston JM, Goetsch MA, Greineder DK, Platt R. Inhaled steroids and the risk of hospitalization for asthma. JAMA 1997;277:887-891.
- Suissa S, Ernst P, Benayoun S, Baltzan M, Cai B. Low-dose inhaled corticosteroids and the prevention of death from asthma. N Engl J Med 2000;343:332-336.
- O"Byrne PM, Pedersen S, Lamm CJ, Tan WC, Busse WW. Severe exacerbations and decline in lung function in asthma. Am J Respir Crit Care Med 2009;179:19-24.
- The Childhood Asthma Management Program Research Group. Long-term effects of budesonide or nedocromil in children with asthma. N Engl J Med 2000;343:1054-1063.
- Sovijärvi AR, Haahtela T, Ekroos HJ, et al. Sustained reduction in bronchial hyperresponsiveness with inhaled fluticasone propionate within three days in mild asthma: time course after onset and cessation of treatment. Thorax 2003;58:500-504.
- Lazarus SC, Boushey HA, Fahy JV, et al. Long-acting beta2-agonist monotherapy vs continued therapy with inhaled corticosteroids in patients with persistent asthma: a randomized controlled trial. JAMA 2001;285:2583-2593.
- Lazarus SC, Chinchilli VM, Rollings NJ, et al. Smoking affects response to inhaled corticosteroids or leukotriene receptor antagonists in asthma. Am J Respir Crit Care Med 2007;175:783-790.
- Tantisira KG, Lake S, Silverman ES, et al. Corticosteroid pharmacogenetics: association of sequence variants in CRHR1 with improved lung function in asthmatics treated with inhaled corticosteroids. Hum Mol Genet 2004;13:1353-1359.
- Barnes PJ. Inhaled glucocorticoids for asthma. N Engl J Med 1995;332:868-875.
- Szefler SJ, Martin RJ, King TS, et al. Significant variability in response to inhaled corticosteroids for persistent asthma. J Allergy Clin Immunol 2002;109:410-418.
- Cumming RG, Mitchell P, Leeder SR. Use of inhaled corticosteroids and the risks of cataracts. N Engl J Med 1997;337:8-14.
- Garbe E, LeLorier J, Boivin JF, Suissa S. Inhaled and nasal glucocorticoids and the risk of ocular hypertension or open-angle glaucoma. JAMA 1997;277:722-727.
- Israel E, Banerjee TR, Fitzmaurice GM, Kotlov TV, LaHive K, LeBoff MS. Effects of inhaled glucocorticoids on bone density in premenopausal women. N Engl J Med 2001;345:941-947.
- Sharek PJ, Bergman DA. The effect of inhaled steroids on the linear growth of children with asthma: a meta-analysis. Pediatrics 2000;106:e8-e8.
- Agertoft L, Pedersen S. Effect of long-term treatment with inhaled budesonide on adult height in children with asthma. N Engl J Med 2000;343:1064-1069.
- DelGaudio JM. Steroid inhaler laryngitis: dysphonia caused by inhaled fluticasone therapy. Arch Otolaryngol Head Neck Surg 2002;128:677-681.
- Boulet LP, Bateman ED, Voves R, Müller T, Wolf S, Engelstätter R. A randomized study comparing ciclesonide and fluticasone propionate in patients with moderate persistent asthma. Respir Med 2007;101:1677-1686.
- Skoner DP, Maspero J, Banerji D, Ciclesonide Pediatric Growth Study Group. Assessment of the long-term safety of inhaled ciclesonide on growth in children with asthma. Pediatrics 2008;121:e1-e14.
- Hodges IG, Netherway TA. Once-daily fluticasone propionate is as effective as twice-daily treatment in stable, mild-to-moderate childhood asthma. Clin Drug Investig 2005;25:13-22.
- Jónasson G, Carlsen K-H, Jonasson C, Mowinckel P. Low-dose inhaled budesonide once or twice daily for 27 months in children with mild asthma. Allergy 2000;55:740-748.
- Barnes NC. The properties of inhaled corticosteroids: similarities and differences. Prim Care Respir J 2007;16:149-154.
- Derendorf H, Nave R, Drollmann A, Cerasoli F, Wurst W. Relevance of pharmacokinetics and pharmacodynamics of inhaled corticosteroids to asthma. Eur Respir J 2006;28:1042-1050.
- Adams N, Bestall J, Jones PW. Budesonide at different doses for chronic asthma. Cochrane Database Syst Rev 2001;4:CD003271-CD003271.
- Lemanske RF Jr, Sorkness CA, Mauger EA, et al. Inhaled corticosteroid reduction and elimination in patients with persistent asthma receiving salmeterol: a randomized controlled trial. JAMA 2001;285:2594-2603.
- Pearlman DS, Chervinsky P, LaForce C, et al. A comparison of salmeterol with albuterol in the treatment of mild-to-moderate asthma. N Engl J Med 1992;327:1420-1425.
- Simons FE, Gerstner TV, Cheang MS. Tolerance to the bronchoprotective effect of salmeterol in adolescents with exercise-induced asthma using concurrent inhaled glucocorticoid treatment. Pediatrics 1997;99:655-659.
- Nelson JA, Strauss L, Skowronski M, Ciufo R, Novak R, McFadden ER Jr. Effect of long-term salmeterol treatment on exercise-induced asthma. N Engl J Med 1998;339:141-146.
- Weinberger M, Abu-Hasan M. Life-threatening asthma during treatment with salmeterol. N Engl J Med 2006;355:852-853.
- Smyth ET, Pavord ID, Wong CS, Wisniewski AF, Williams J, Tattersfield AE. Interaction and dose equivalence of salbutamol and salmeterol in patients with asthma. BMJ 1993;306:543-545.
- Wechsler ME, Lehman E, Lazarus SC, et al. b-Adrenergic receptor polymorphism and response to salmeterol. Am J Respir Crit Care Med 2006;173:519-526.
- Gibson PG, Powell H, Ducharme FM. Differential effects of maintenance long-acting beta-agonist and inhaled corticosteroid on asthma control and asthma exacerbations. J Allergy Clin Immunol 2007;119:344-350.
- Woolcock A, Lundback B, Ringdal N, Jacques LA. Comparison of addition of salmeterol to inhaled steroids with doubling of the dose of inhaled steroids. Am J Respir Crit Care Med 1996;153:1481-1488.
- Pauwels RA, Löfdahl C-G, Postma DS, et al. Effect of inhaled formoterol and budesonide on exacerbations of asthma. N Engl J Med 1997;337:1405-1411.
- Giembycz MA, Kaur M, Leigh R, Newton R. A Holy Grail of asthma management: toward understanding how long-acting b 2 -adrenoceptor agonists enhance the clinical efficacy of inhaled corticosteroids. Br J Pharmacol 2008;153:1090-1104.
- Nelson HS, Weiss ST, Bleecker ER, Yancey SW, Dorinsky PM, SMART Study Group. The Salmeterol Multicenter Asthma Research Trial: a comparison of usual pharmacotherapy for asthma or usual pharmacotherapy plus salmeterol. Chest 2006;129:15-26.
- Nelson HS. Is there a problem with inhaled long-acting beta-adrenergic agonists? J Allergy Clin Immunol 2006;117:3-16.
- Bateman E, Nelson H, Bousquet J, et al. Meta-analysis: effects of adding salmeterol to inhaled corticosteroids on serious asthma-related events. Ann Intern Med 2008;149:33-42.
- The American Lung Association Asthma Clinical Research Centers. Randomized comparison of strategies for reducing treatment in mild persistent asthma. N Engl J Med 2007;356:2027-2039.
- Lötvall J. Pharmacological similarities and differences between beta2-agonists. Respir Med 2001;95:Suppl B:S7-S11.
- Drazen JM, Israel E, O"Byrne PM. Treatment of asthma with drugs modifying the leukotriene pathway. N Engl J Med 1999;340:197-206.
- Reiss TF, Chervinsky P, Dockhorn RJ, Shingo S, Seidenberg B, Edwards TB. Montelukast, a once-daily leukotriene receptor antagonist, in the treatment of chronic asthma: a multicenter, randomized, double-blind trial. Arch Intern Med 1998;158:1213-1220.
- Knorr B, Matz J, Bernstein JA, et al. Montelukast for chronic asthma in 6- to 14-year-old children: a randomized, double-blind trial. JAMA 1998;279:1181-1186.
- Pizzichini E, Leff JA, Reiss TF, et al. Montelukast reduces airway eosinophilic inflammation in asthma: a randomized, controlled trial. Eur Respir J 1999;14:12-18.
Глюкокортикоиды — стероидные гормоны, синтезируемые корой надпочечников. Природные глюкокортикоиды и их синтетические аналоги применяются в медицине при надпочечниковой недостаточности. Кроме того, при некоторых заболеваниях используются противовоспалительные, иммунодепрессивные, противоаллергические, противошоковые и другие свойства этих препаратов.
Начало применения глюкокортикоидов в качестве лекарственных средств (ЛС ) относится к 40-м гг. XX века. Еще в конце 30-х гг. прошлого века было показано, что в коре надпочечников образуются гормональные соединения стероидной природы. В 1937 г. из коры надпочечников был выделен минералокортикоид дезоксикортикостерон, в 40-х гг. — глюкокортикоиды кортизон и гидрокортизон. Широкий спектр фармакологических эффектов гидрокортизона и кортизона предопределил возможность их использования в качестве ЛС . Вскоре был осуществлен их синтез.
Основным и наиболее активным глюкокортикоидом, образующимся в организме человека, является гидрокортизон (кортизол), другие, менее активные, представлены кортизоном, кортикостероном, 11-дезоксикортизолом, 11-дегидрокортикостероном.
Выработка гормонов надпочечников находится под контролем ЦНС и тесно связана с функцией гипофиза. Адренокортикотропный гормон гипофиза (АКТГ, кортикотропин) является физиологическим стимулятором коры надпочечников. Кортикотропин усиливает образование и выделение глюкокортикоидов. Последние, в свою очередь, влияют на гипофиз, угнетая выработку кортикотропина и уменьшая, таким образом, дальнейшую стимуляцию надпочечников (по принципу отрицательной обратной связи). Длительное введение в организм глюкокортикоидов (кортизона и его аналогов) может привести к угнетению и атрофии коры надпочечников, а также к угнетению образования не только АКТГ , но и гонадотропных и тиреотропного гормонов гипофиза.
Практическое применение в качестве ЛС из естественных глюкокортикоидов нашли кортизон и гидрокортизон. Кортизон, однако, чаще, чем другие глюкокортикоиды, вызывает побочные явления и, в связи с появлением более эффективных и безопасных препаратов в настоящее время имеет ограниченное применение. В медицинской практике используют естественный гидрокортизон или его эфиры (гидрокортизона ацетат и гидрокортизона гемисукцинат).
Синтезирован целый ряд синтетических глюкокортикоидов, среди которых выделяют нефторированные (преднизон, преднизолон, метилпреднизолон) и фторированные (дексаметазон, бетаметазон, триамцинолон, флуметазон и др.) глюкокортикоиды. Эти соединения, как правило, более активны, чем природные глюкокортикоиды, действуют в меньших дозах. Действие синтетических стероидов сходно с действием природных кортикостероидов, но они обладают различным соотношением глюкокортикоидной и минералокортикоидной активности. Более благоприятным соотношением между глюкокортикоидной/противовоспалительной и минералокортикоидной активностью отличаются фторированные производные. Так, противовоспалительная активность дексаметазона (по сравнению с таковой гидрокортизона) выше в 30 раз, бетаметазона — в 25-40 раз, триамцинолона — в 5 раз, при этом влияние на водно-солевой обмен минимально. Фторированные производные отличаются не только высокой эффективностью, но и низкой абсорбцией при местном применении, т.е. меньшей вероятностью развития системных побочных эффектов.
Механизм действия глюкокортикоидов на молекулярном уровне до конца не выяснен. Считают, что действие глюкокортикоидов на клетки-мишени осуществляется, главным образом, на уровне регуляции транскрипции генов. Оно опосредуется взаимодействием глюкокортикоидов со специфическими глюкокортикоидными внутриклеточными рецепторами (альфа-изоформа). Эти ядерные рецепторы способны связываться с ДНК и относятся к семейству лиганд-чувствительных регуляторов транскрипции. Рецепторы глюкокортикоидов обнаружены практически во всех клетках. В разных клетках, однако, количество рецепторов варьирует, они также могут различаться по молекулярной массе, сродству к гормону и другим физико-химическим характеристикам. При отсутствии гормона внутриклеточные рецепторы, которые представляют собой цитозольные белки, неактивны и входят в состав гетерокомплексов, включающих также белки теплового шока (heat shock protein, Hsp90 и Hsp70), иммунофилин с молекулярной массой 56000 и др. Белки теплового шока способствуют поддержанию оптимальной конформации гормоносвязывающего домена рецептора и обеспечивают высокое сродство рецептора к гормону.
После проникновения через мембрану внутрь клетки глюкокортикоиды связываются с рецепторами, что приводит к активации комплекса. При этом олигомерный белковый комплекс диссоциирует — отсоединяются белки теплового шока (Hsp90 и Hsp70) и иммунофилин. В результате этого рецепторный белок, входящий в комплекс в виде мономера, приобретает способность димеризоваться. Вслед за этим образовавшиеся комплексы «глюкокортикоид + рецептор» транспортируются в ядро, где взаимодействуют с участками ДНК , расположенными в промоторном фрагменте стероид-отвечающего гена — т.н. глюкокортикоид-отвечающими элементами (glucocorticoid response element, GRE) и регулируют (активируют или подавляют) процесс транскрипции определенных генов (геномный эффект). Это приводит к стимуляции или супрессии образования м-РНК и изменению синтеза различных регуляторных белков и ферментов, опосредующих клеточные эффекты.
Исследования последних лет показывают, что ГК-рецепторы взаимодействуют, кроме GRE, с различными факторами транскрипции, такими как активаторный белок транскрипции (AP-1), ядерный фактор каппа В (NF-kB) и др. Показано, что ядерные факторы AP-1 и NF-kB являются регуляторами нескольких генов, принимающих участие в иммунном ответе и воспалении, включая гены цитокинов, молекул адгезии, протеиназ и др.
Кроме того, недавно открыт еще один механизм действия глюкокортикоидов, связанный с влиянием на транскрипционную активацию цитоплазматического ингибитора NF-kB — IkBa.
Однако ряд эффектов глюкокортикоидов (например быстрое ингибирование глюкокортикоидами секреции АКТГ) развиваются очень быстро и не могут быть объяснены экспрессией генов (т.н. внегеномные эффекты глюкокортикоидов). Такие свойства могут быть опосредованы нетранскрипторными механизмами, либо взаимодействием с обнаруженными в некоторых клетках рецепторами глюкокортикоидов на плазматической мембране. Полагают также, что эффекты глюкокортикоидов могут реализовываться на разных уровнях в зависимости от дозы. Например, при низких концентрациях глюкокортикоидов (>10 -12 моль/л) проявляются геномные эффекты (для их развития требуется более 30 мин), при высоких — внегеномные.
Глюкортикоиды вызывают множество эффектов, т.к. оказывают влияние на большинство клеток организма.
Они обладают противовоспалительным, десенсибилизирующим, противоаллергическим и иммунодепрессивным действием, противошоковыми и антитоксическими свойствами.
Противовоспалительное действие глюкокортикоидов обусловлено многими факторами, ведущим из которых является подавление активности фосфолипазы А 2 . При этом глюкокортикоиды действуют опосредованно: они увеличивают экспрессию генов, кодирующих синтез липокортинов (аннексинов), индуцируют продукцию этих белков, один из которых — липомодулин — ингибирует активность фосфолипазы А 2 . Угнетение этого фермента приводит к подавлению либерации арахидоновой кислоты и торможению образования ряда медиаторов воспаления — простагландинов, лейкотриенов, тромбоксана, фактора активации тромбоцитов и др. Кроме того, глюкокортикоиды уменьшают экспрессию гена, кодирующего синтез ЦОГ-2 , дополнительно блокируя образование провоспалительных простагландинов.
Кроме того, глюкокортикоиды улучшают микроциркуляцию в очаге воспаления, вызывают вазоконстрикцию капилляров, уменьшают экссудацию жидкости. Глюкокортикоиды стабилизируют клеточные мембраны, в т.ч. мембраны лизосом, предотвращая выход лизосомальных ферментов и снижая тем самым их концентрацию в месте воспаления.
Таким образом, глюкокортикоиды влияют на альтеративную и экссудативную фазы воспаления, препятствуют распространению воспалительного процесса.
Ограничение миграции моноцитов в очаг воспаления и торможение пролиферации фибробластов обусловливают антипролиферативное действие. Глюкокортикоиды подавляют образование мукополисахаридов, ограничивая тем самым связывание воды и белков плазмы в очаге ревматического воспаления. Угнетают активность коллагеназы, препятствуя деструкции хрящей и костей при ревматоидном артрите.
Противоаллергическое действие развивается в результате снижения синтеза и секреции медиаторов аллергии, торможения высвобождения из сенсибилизированных тучных клеток и базофилов гистамина и других биологически активных веществ, уменьшения числа циркулирующих базофилов, подавления пролиферации лимфоидной и соединительной ткани, уменьшения количества Т- и B-лимфоцитов, тучных клеток, снижения чувствительности эффекторных клеток к медиаторам аллергии, угнетения антителообразования, изменения иммунного ответа организма.
Характерной особенностью глюкокортикоидов является иммунодепрессивная активность. В отличие от цитостатиков, иммунодепрессивные свойства глюкокортикоидов не связаны с митостатическим действием, а являются результатом подавления разных этапов иммунной реакции: торможения миграции стволовых клеток костного мозга и В-лимфоцитов, подавления активности Т- и B-лимфоцитов, а также угнетения высвобождения цитокинов (ИЛ-1, ИЛ-2, интерферона-гамма) из лейкоцитов и макрофагов. Кроме того, глюкокортикоиды снижают образование и увеличивают распад компонентов системы комплемента, блокируют Fc-рецепторы иммуноглобулинов, подавляют функции лейкоцитов и макрофагов.
Противошоковое и антитоксическое действие глюкокортикоидов связано с повышением АД (за счет увеличения количества циркулирующих катехоламинов, восстановления чувствительности адренорецепторов к катехоламинам и вазоконстрикции), активацией ферментов печени, участвующих в метаболизме эндо- и ксенобиотиков.
Глюкокортикоиды оказывают выраженное влияние на все виды обмена: углеводный, белковый, жировой и минеральный. Со стороны углеводного обмена это проявляется тем, что они стимулируют глюконеогенез в печени, повышают содержание глюкозы в крови (возможна глюкозурия), способствуют накоплению гликогена в печени. Влияние на белковый обмен выражается в угнетении синтеза и ускорении катаболизма белков, особенно в коже, в мышечной и костной ткани. Это проявляется мышечной слабостью, атрофией кожи и мышц, замедлением заживления ран. Эти ЛС вызывают перераспределение жира: повышают липолиз в тканях конечностей, способствуют накоплению жира преимущественно в области лица (лунообразное лицо), плечевого пояса, живота.
Глюкокортикоиды обладают минералокортикоидной активностью: задерживают в организме натрий и воду за счет увеличения реабсорбции в почечных канальцах, стимулируют выведение калия. Эти эффекты более характерны для природных глюкокортикоидов (кортизон, гидрокортизон), в меньшей степени — для полусинтетических (преднизон, преднизолон, метилпреднизолон). Преобладает минералокортикоидная активность у флудрокортизона. У фторированных глюкокортикоидов (триамцинолон, дексаметазон, бетаметазон) минералокортикоидная активность практически отсутствует.
Глюкокортикоиды снижают всасывание кальция в кишечнике, способствуют его выходу из костей и повышают выведение кальция почками, в результате чего возможно развитие гипокальциемии, гиперкальциурии, глюкокортикоидного остеопороза.
После приема даже одной дозы глюкокортикоидов отмечают изменения со стороны крови: снижение количества лимфоцитов, моноцитов, эозинофилов, базофилов в периферической крови с одновременным развитием нейтрофильного лейкоцитоза, повышением содержания эритроцитов.
При длительном применении глюкокортикоиды подавляют функцию системы гипоталамус — гипофиз — надпочечники.
Глюкокортикоиды различаются по активности, фармакокинетическим параметрам (степень всасывания, T 1/2 и др.), способам применения.
Системные глюкокортикоиды можно разделить на несколько групп.
По происхождению они подразделяются на:
Природные (гидрокортизон, кортизон);
Синтетические (преднизолон, метилпреднизолон, преднизон, триамцинолон, дексаметазон, бетаметазон).
По длительности действия глюкокортикоиды для системного применения можно разделить на три группы (в скобках — биологический (из тканей) период полувыведения (T 1/2 биол.):
Глюкокортикоиды короткого действия (T 1/2 биол. — 8-12 ч): гидрокортизон, кортизон;
Глюкокортикоиды средней продолжительности действия (T 1/2 биол. — 18-36 ч): преднизолон, преднизон, метилпреднизолон;
Глюкокортикоиды длительного действия (T 1/2 биол. — 36-54 ч): триамцинолон, дексаметазон, бетаметазон.
Продолжительность действия глюкокортикоидов зависит от пути/места введения, растворимости лекарственной формы (мазипредон — водорастворимая форма преднизолона), вводимой дозы. После приема внутрь или в/в введения продолжительность действия зависит от T 1/2 биол., при в/м введении — от растворимости лекарственной формы и T 1/2 биол., после локальных инъекций — от растворимости лекарственной формы и специфического пути/места введения.
При приеме внутрь глюкокортикоиды быстро и почти полностью всасываются из ЖКТ . С max в крови отмечается через 0,5-1,5 ч. Глюкокортикоиды связываются в крови с транскортином (кортикостероидсвязывающий альфа 1 -глобулин) и альбумином, причем природные глюкокортикоиды связываются с белками на 90-97%, синтетические — на 40-60%. Глюкокортикоиды хорошо проникают через гистогематические барьеры, в т.ч. через ГЭБ , проходят через плаценту. Фторированные производные (в т.ч. дексаметазон, бетаметазон, триамцинолон) через гистогематические барьеры проходят хуже. Глюкокортикоиды подвергаются биотрансформации в печени с образованием неактивных метаболитов (глюкуронидов или сульфатов), которые выводятся преимущественно почками. Природные препараты метаболизируются быстрее, чем синтетические, и имеют менее длительный период полувыведения.
Современные глюкокортикоиды представляют собой группу средств, широко применяющихся в клинической практике, в т.ч. в ревматологии, пульмонологии, эндокринологии, дерматологии, офтальмологии, оториноларингологии.
Основными показаниями к применению глюкокортикоидов являются коллагенозы, ревматизм, ревматоидный артрит, бронхиальная астма, острый лимфобластный и миелобластный лейкоз, инфекционный мононуклеоз, экзема и другие кожные болезни, различные аллергические заболевания. Для терапии атопических, аутоиммунных заболеваний глюкокортикоиды являются базовыми патогенетическими средствами. Применяют глюкокортикоиды также при гемолитической анемии, гломерулонефрите, остром панкреатите, вирусном гепатите и заболеваниях органов дыхания (ХОБЛ в фазе обострения, острый респираторный дистресс-синдром и др.). В связи с противошоковым эффектом глюкокортикоиды назначают для профилактики и лечения шока (посттравматического, операционного, токсического, анафилактического, ожогового, кардиогенного и др.).
Иммунодепрессивное действие глюкокортикоидов позволяет использовать их при трансплантации органов и тканей для подавления реакции отторжения, а также при различных аутоиммунных заболеваниях.
Главный принцип глюкокортикоидной терапии — достижение максимального лечебного эффекта при минимальных дозах. Режим дозирования подбирают строго индивидуально, в большей степени в зависимости от характера заболевания, состояния больного и реакции на проводимое лечение, чем от возраста или массы тела.
При назначении глюкокортикоидов необходимо учитывать их эквивалентные дозы: по противовоспалительному эффекту 5 мг преднизолона соответствуют 25 мг кортизона, 20 мг гидрокортизона, 4 мг метилпреднизолона, 4 мг триамцинолона, 0,75 мг дексаметазона, 0,75 мг бетаметазона.
Различают 3 вида глюкокортикоидной терапии: заместительная, супрессивная, фармакодинамическая.
Заместительная терапия глюкокортикоидами необходима при надпочечниковой недостаточности. При этом виде терапии используют физиологические дозы глюкокортикоидов, при стрессовых ситуациях (например хирургическая операция, травма, острое заболевание) дозы увеличивают в 2-5 раз. При назначении следует учитывать суточный циркадный ритм эндогенной секреции глюкокортикоидов: в 6-8 ч утра назначают бóльшую (или всю) часть дозы. При хронической недостаточности коры надпочечников (болезнь Аддисона) глюкокортикоиды могут применяться в течение всей жизни.
Супрессивная терапия глюкокортикоидами применяется при адреногенитальном синдроме — врожденной дисфункции коры надпочечников у детей. При этом глюкокортикоиды используют в фармакологических (супрафизиологических) дозах, что приводит к подавлению секреции АКТГ гипофизом и последующему снижению повышенной секреции андрогенов надпочечниками. Бóльшую (2/3) часть дозы назначают на ночь, чтобы, по принципу отрицательной обратной связи, предотвратить пик выброса АКТГ .
Фармакодинамическая терапия используется наиболее часто, в т.ч. при лечении воспалительных и аллергических заболеваний.
Можно выделить несколько разновидностей фармакодинамической терапии: интенсивную, лимитирующую, долговременную.
Интенсивная фармакодинамическая терапия: применяют при острых, угрожающих жизни состояниях, глюкокортикоиды вводят в/в , начиная с больших доз (5 мг/кг — сутки); после выхода больного из острого состояния (1-2 дня) глюкокортикоиды отменяют сразу, одномоментно.
Лимитирующая фармакодинамическая терапия: назначают при подострых и хронических процессах, в т.ч. воспалительных (системная красная волчанка, системная склеродермия, ревматическая полимиалгия, бронхиальная астма тяжелого течения, гемолитическая анемия, острый лейкоз и др.). Длительность терапии составляет, как правило, несколько месяцев, глюкокортикоиды применяют в дозах, превышающих физиологические (2-5 мг/кг/сут), с учетом циркадного ритма.
Для уменьшения угнетающего влияния глюкокортикоидов на гипоталамо-гипофизарно-надпочечниковую систему предложены разные схемы прерывистого назначения глюкокортикоидов:
- альтернирующая терапия — используют глюкокортикоиды короткой/средней продолжительности действия (преднизолон, метилпреднизолон), однократно, утром (около 8 ч), каждые 48 ч;
- интермиттирующая схема — глюкокортикоиды назначают короткими курсами (3-4 дня) с 4-дневными перерывами между курсами;
- пульс-терапия — быстрое в/в введение большой дозы препарата (не менее 1 г) — для неотложной терапии. Препарат выбора для пульс-терапии — метилпреднизолон (лучше других поступает в воспаленные ткани и реже вызывает побочные эффекты).
Долговременная фармакодинамическая терапия: применяют при лечении заболеваний с хроническим течением. Глюкокортикоиды назначают внутрь, дозы превосходят физиологические (2,5-10 мг/сут), терапию назначают в течение нескольких лет, отмена глюкокортикоидов при этом виде терапии проводится очень медленно.
Дексаметазон и бетаметазон не применяют для длительной терапии, поскольку при самом сильном и длительном, по сравнению с другими глюкокортикоидами, противовоспалительным действии они вызывают и самые выраженные побочные эффекты, в т.ч. угнетающее действие на лимфоидную ткань и кортикотропную функцию гипофиза.
Во время лечения возможен переход от одного вида терапии к другому.
Глюкокортикоиды применяют внутрь, парентерально, интра- и периартикулярно, ингаляционно, интраназально, ретро- и парабульбарно, в виде глазных и ушных капель, наружно в виде мазей, кремов, лосьонов и др.
Например, при ревматических заболеваниях глюкокортикоиды применяют для системной, местной или локальной (интраартикулярно, периартикулярно, наружно) терапии. При бронхообструктивных заболеваниях особо важное значение имеют ингаляционные глюкокортикоиды.
Глюкокортикоиды являются эффективными терапевтическими средствами во многих случаях. Необходимо, однако, учитывать, что они могут вызывать ряд побочных эффектов, в том числе симптомокомплекс Иценко-Кушинга (задержка натрия и воды в организме с возможным появлением отеков, потеря калия, повышение АД), гипергликемию вплоть до сахарного диабета (стероидный диабет), замедление процессов регенерации тканей, обострение язвенной болезни желудка и двенадцатиперстной кишки, изъязвление пищеварительного тракта, прободение нераспознанной язвы, геморрагический панкреатит, понижение сопротивляемости организма к инфекциям, гиперкоагуляцию с риском тромбоза, появление угрей, лунообразного лица, ожирения, нарушения менструального цикла и др. При приеме глюкокортикоидов отмечается усиленное выведение кальция и остеопороз (при длительном приеме глюкокортикоидов в дозах более 7,5 мг/сут — в эквиваленте по преднизолону — возможно развитие остеопороза длинных трубчатых костей). Профилактику стероидного остеопороза осуществляют препаратами кальция и витамина D с момента начала приема глюкокортикоидов. Наиболее выраженные изменения в костно-мышечной системе отмечаются в первые 6 мес лечения. Одним из опасных осложнений является асептический некроз костей, поэтому необходимо предупреждать пациентов о возможности его развития и при появлении «новых» болей, особенно в плечевом, тазобедренном и коленном суставах, необходимо исключать асептический некроз кости. Глюкокортикоиды вызывают изменения со стороны крови: лимфопения, моноцитопения, эозинопения, снижение количества базофилов в периферической крови, развитие нейтрофильного лейкоцитоза, повышение содержания эритроцитов. Возможны также нервные и психические расстройства: инсомния, возбуждение (с развитием в некоторых случаях психоза), эпилептиформные судороги, эйфория.
При длительном применении глюкокортикоидов следует учитывать вероятное угнетение функции коры надпочечников (не исключена атрофия) с подавлением биосинтеза гормонов. Введение кортикотропина одновременно с глюкокортикоидами предотвращает атрофию надпочечников.
Частота и сила побочных явлений, вызываемых глюкокортикоидами, могут быть выражены в разной степени. Побочные эффекты, как правило, являются проявлением собственно глюкокортикоидного действия этих ЛС , но в степени, превышающей физиологическую норму. При правильном подборе дозы, соблюдении необходимых мер предосторожности, постоянном наблюдении за ходом лечения частоту развития побочных явлений можно значительно снизить.
Для предупреждения нежелательных эффектов, связанных с применением глюкокортикоидов, следует, особенно при длительном лечении, тщательно наблюдать за динамикой роста и развития у детей, периодически проводить офтальмологическое обследование (для выявления глаукомы, катаракты и др.), регулярно контролировать функцию гипоталамо-гипофизарно-адреналовой системы, содержание глюкозы в крови и моче (особенно у больных сахарным диабетом), проводить контроль АД , ЭКГ , электролитного состава крови, контроль за состоянием ЖКТ , костно-мышечной системы, контроль за развитием инфекционных осложнений и др.
Большинство осложнений при лечении глюкокортикоидами поддаются лечению и проходят после отмены ЛС . К необратимым побочным эффектам глюкокортикоидов относят задержку роста у детей (возникает при лечении глюкокортикоидами в течение более 1,5 лет), субкапсулярную катаракту (развивается при наличии семейной предрасположенности), стероидный диабет.
Резкая отмена глюкокортикоидов может вызвать обострение процесса — синдром отмены, особенно при прекращении длительной терапии. В связи с этим, лечение должно заканчиваться постепенным уменьшением дозы. Тяжесть синдрома отмены зависит от степени сохранности функции коры надпочечников. В легких случаях синдром отмены проявляется повышением температуры тела, миалгией, артралгией, недомоганием. В тяжелых случаях, особенно при сильном стрессе, может развиться аддисонический криз (сопровождающийся рвотой, коллапсом, судорогами).
В связи с побочными эффектами глюкокортикоиды применяются только при наличии четких показаний и под тщательным врачебным контролем. Противопоказания для назначения глюкокортикоидов являются относительными. В неотложных ситуациях единственным противопоказанием для кратковременного системного применения глюкокортикоидов является гиперчувствительность. В остальных случаях при планировании длительной терапии противопоказания должны приниматься во внимание.
Терапевтические и токсические эффекты глюкокортикоидов снижают — индукторы микросомальных ферментов печени, усиливают — эстрогены и пероральные противозачаточные средства. Гликозиды наперстянки, диуретики (вызывающие дефицит калия), амфотерицин B, ингибиторы карбоангидразы повышают вероятность аритмий и гипокалиемии. Алкоголь и НПВС повышают риск эрозивно-язвенных поражений или кровотечений в ЖКТ . Иммунодепрессанты увеличивают вероятность развития инфекций. Глюкокортикоиды ослабляют гипогликемическую активность противодиабетических средств и инсулина, натрийуретическую и диуретическую — мочегонных, антикоагулянтную и фибринолитическую — производных кумарина и индандиона, гепарина, стрептокиназы и урокиназы, активность вакцин (из-за снижения выработки антител), снижают концентрацию в крови салицилатов, мексилетина. При применении преднизолона и парацетамола повышается риск гепатотоксичности.
Известны пять ЛС , подавляющих секрецию кортикостероидов корой надпочечников (ингибиторы синтеза и действия кортикостероидов) : митотан, метирапон, аминоглутетимид, кетоконазол, трилостан. Аминоглутетимид, метирапон и кетоконазол подавляют синтез стероидных гормонов вследствие ингибирования гидроксилаз (изоферменты цитохрома P450), принимающих участие в биосинтезе. Все три ЛС обладают специфичностью, т.к. действуют на разные гидроксилазы. Эти препараты могут вызвать острую надпочечниковую недостаточность, поэтому их следует применять в строго определенных дозах и при тщательном наблюдении за состоянием гипоталамо-гипофизарно-надпочечниковой системы пациента.
Аминоглутетимид ингибирует 20,22-десмолазу, катализирующую начальную (лимитирующую) стадию стероидогенеза — превращение холестерина в прегненолон. В результате нарушается продукция всех стероидных гормонов. Кроме того, аминоглутетимид ингибирует 11-бета-гидроксилазу, а также ароматазу. Аминоглутетимид применяют при синдроме Кушинга, вызванном нерегулируемой избыточной секрецией кортизола опухолями коры надпочечников или эктопической продукцией АКТГ . Способность аминоглутетимида ингибировать ароматазу используют при лечении таких гормонально-зависимых опухолей, как рак предстательной железы, рак молочной железы.
Кетоконазол применяется в основном как противогрибковое средство. Однако в более высоких дозах он ингибирует несколько ферментов цитохрома Р450, вовлеченных в стероидогенез, в т.ч. 17-альфа-гидроксилазу, а также 20,22-десмолазу и блокирует, таким образом, стероидогенез во всех тканях. Согласно некоторым данным, кетоконазол является наиболее эффективным ингибитором стероидогенеза при болезни Кушинга. Однако целесообразность применения кетоконазола при избыточной продукции стероидных гормонов требует дальнейшего исследования.
Аминоглутетимид, кетоконазол и метирапон используются для диагностики и лечения гиперплазии надпочечников.
К антагонистам глюкокортикоидных рецепторов относится мифепристон. Мифепристон — антагонист прогестероновых рецепторов, в больших дозах блокирует глюкокортикоидные рецепторы, препятствует угнетению гипоталамо-гипофизарно-надпочечниковой системы (по механизму отрицательной обратной связи) и приводит к вторичному усилению секреции АКТГ и кортизола.
Одной из важнейших областей клинического применения глюкокортикоидов является патология различных отделов дыхательного тракта.
Показаниями для назначения системных глюкокортикоидов при заболеваниях органов дыхания являются бронхиальная астма, ХОБЛ в фазе обострения, пневмония тяжелого течения, интерстициальные болезни легких, острый респираторный дистресс-синдром.
После того, как в конце 40-х годов XX века были синтезированы глюкокортикоиды системного действия (пероральные и инъекционные формы), их сразу же стали применять для лечения тяжелой бронхиальной астмы. Несмотря на хороший терапевтический эффект, применение глюкокортикоидов при бронхиальной астме ограничивалось развитием осложнений — стероидного васкулита, системного остеопороза, сахарного диабета (стероидный диабет). Местные формы глюкокортикоидов стали применяться в клинической практике лишь спустя некоторое время — в 70-е гг. XX века. Публикация об успешном использовании первого топического глюкокортикоида — беклометазона (беклометазона дипропионат) — для лечения аллергического ринита относится к 1971 г. В 1972 г. появилось сообщение об использовании топической формы беклометазона для лечения бронхиальной астмы.
Ингаляционные глюкокортикоиды являются базисными препаратами при лечении всех патогенетических вариантов бронхиальной астмы персистирующего течения, применяются при ХОБЛ средней тяжести и тяжелого течения (со спирографически подтвержденным ответом на лечение).
К ингаляционным глюкокортикоидам относятся беклометазон, будесонид, флутиказон, мометазон, триамцинолон. Ингаляционные глюкокортикоиды отличаются от системных по фармакологическим свойствам: высокая аффинность к ГК-рецепторам (действуют в минимальных дозах), сильное местное противовоспалительное действие, низкая системная биодоступность (пероральная, легочная), быстрая инактивация, короткий T 1/2 из крови. Ингаляционные глюкокортикоиды угнетают все фазы воспаления в бронхах и снижают их повышенную реактивность. Очень важное значение имеет их способность понижать бронхиальную секрецию (уменьшать объем трахеобронхиального секрета) и потенцировать действие бета 2 -адреномиметиков. Применение ингаляционных форм глюкокортикоидов позволяет уменьшить потребность в таблетированных глюкокортикоидах. Важной характеристикой ингаляционных глюкокортикоидов является терапевтический индекс — соотношение местной противовоспалительной активности и системного действия. Из ингаляционных глюкокортикоидов наиболее благоприятный терапевтический индекс имеет будесонид.
Одним из факторов, определяющих эффективность и безопасность ингаляционных глюкокортикоидов, являются системы для их доставки в дыхательные пути. В настоящее время для этой цели используются дозированные и порошковые ингаляторы (турбухалер и др.), небулайзеры.
При правильном выборе системы и техники ингаляции системные побочные эффекты ингаляционных глюкокортикоидов незначительны ввиду низкой биодоступности и быстрой метаболической активации этих ЛС в печени. Следует иметь в виду, что все существующие ингаляционные глюкокортикоиды в той или иной степени всасываются в легких. Местные побочные эффекты ингаляционных глюкокортикоидов, особенно при длительном применении, заключаются в возникновении ротоглоточного кандидоза (у 5-25% больных), реже — кандидоза пищевода, дисфонии (у 30-58% больных), кашля.
Показано, что ингаляционные глюкокортикоиды и бета-адреномиметики длительного действия (салметерол, формотерол) обладают синергическим эффектом. Это обусловлено стимуляцией биосинтеза бета 2 -адренорецепторов и повышением их чувствительности к агонистам под влиянием глюкокортикоидов. В связи с этим при лечении бронхиальной астмы эффективными являются комбинированные препараты, предназначенные для длительной терапии, но не для купирования приступов — например фиксированная комбинация салметерол/флутиказон или формотерол/будесонид.
Ингаляции глюкокортикоидами противопоказаны при грибковых поражениях дыхательных путей, туберкулезе, беременности.
В настоящее время для интраназального применения в клинической практике используют беклометазона дипропионат, будесонид, флутиказон, мометазона фуроат. Кроме того, лекарственные формы в виде назальных аэрозолей существуют для флунизолида и триамцинолона, но в России они сейчас не применяются.
Назальные формы глюкокортикоидов эффективны при лечении неинфекционных воспалительных процессов в полости носа, рините, в т.ч. медикаментозном, профессиональном, сезонном (интермиттирующем) и круглогодичном (персистирующем) аллергическом рините, для предотвращения рецидива образования полипов в полости носа после их удаления. Топические глюкокортикоиды характеризуются относительно поздним началом действия (12-24 ч), медленным развитием эффекта — проявляется к 3-му дню, достигает максимума на 5-7-й день, иногда — через несколько недель. Наиболее быстро начинает действовать мометазон (12 ч).
Современные интраназальные глюкокортикоиды хорошо переносятся, при применении в рекомендуемых дозах системные (часть дозы всасывается со слизистой оболочки полости носа и попадает в системный кровоток) эффекты минимальны. Среди местных побочных эффектов у 2-10% пациентов в начале лечения отмечаются носовые кровотечения, сухость и жжение в носу, чиханье и зуд. Возможно, эти побочные эффекты являются следствием раздражающего действия пропеллента. Описаны единичные случаи перфорации носовой перегородки при применении интраназальных глюкокортикоидов.
Интраназальное применение глюкокортикоидов противопоказано при геморрагическом диатезе, а также при повторных носовых кровотечениях в анамнезе.
Таким образом, глюкокортикоиды (системные, ингаляционные, назальные) получили широкое применение в пульмонологии и оториноларингологии. Это обусловлено способностью глюкокортикоидов купировать основные симптомы заболеваний лор-органов и органов дыхания, а при персистирующем течении процесса — существенно пролонгировать межприступный период. Очевидное преимущество применения топических лекарственных форм глюкокортикоидов заключается в возможности минимизировать системные побочные эффекты, повысив, таким образом, эффективность и безопасность терапии.
В 1952 г. Sulzberger и Witten впервые сообщили об успешном применении 2,5% гидрокортизоновой мази для наружного лечения кожного дерматоза. Природный гидрокортизон — исторически первый глюкокортикоид, примененный в дерматологической практике, впоследствии он стал стандартом для сравнения силы разных глюкокортикоидов. Гидрокортизон, однако, недостаточно эффективен, особенно при тяжелых дерматозах, вследствие относительно слабого связывания со стероидными рецепторами клеток кожи и медленного проникновения через эпидермис.
Позже глюкокортикоиды нашли широкое применение в дерматологии для лечения различных заболеваний кожи неинфекционной природы: атопический дерматит, псориаз, экзема, красный плоский лишай и другие дерматозы. Они оказывают местное противовоспалительное, противоаллергическое действие, устраняют зуд (применение при зуде обосновано только в случае, если он вызван воспалительным процессом).
Топические глюкокортикоиды отличаются друг от друга по химической структуре, а также по силе местного противовоспалительного действия.
Создание галогенированных соединений (включение в молекулу галогенов — фтора или хлора) позволило увеличить противовоспалительный эффект и уменьшить системное побочное действие при местном применении вследствие меньшей абсорбции ЛС . Наиболее низкой всасываемостью при аппликации на кожу отличаются соединения, содержащие в своей структуре два атома фтора — флуметазон, флуоцинолона ацетонид и др.
Согласно Европейской классификации (Niedner, Schopf, 1993) по потенциальной активности местных стероидов выделяют 4 класса:
Слабые (класс I) — гидрокортизон 0,1-1%, преднизолон 0,5%, флуоцинолона ацетонид 0,0025%;
Средней силы (класс II) — алклометазон 0,05%, бетаметазона валерат 0,025%, триамцинолона ацетонид 0,02%, 0,05%, флуоцинолона ацетонид 0,00625% и др.;
Сильные (класс III) — бетаметазона валерат 0,1%, бетаметазона дипропионат 0,025%, 0,05%, гидрокортизона бутират 0,1%, метилпреднизолона ацепонат 0,1%, мометазона фуроат 0,1%, триамцинолона ацетонид 0,025%, 0,1%, флутиказон 0,05%, флуоцинолона ацетонид 0,025% и др.
Очень сильные (класс III) — клобетазола пропионат 0,05% и др.
Наряду с повышением терапевтического действия при использовании фторированных глюкокортикоидов увеличивается и частота развития побочных явлений. Наиболее частыми среди местных побочных явлений при применении сильных глюкокортикоидов являются атрофия кожи, телеангиэктазии, стероидные акне, стрии, инфекции кожи. Вероятность развития как местных, так и системных побочных эффектов возрастает при нанесении на обширные поверхности и длительном использовании глюкокортикоидов. Из-за развития побочных эффектов применение фторсодержащих глюкокортикоидов ограничено при необходимости длительного использования, а также в педиатрической практике.
В последние годы путем модификации молекулы стероида получены местные глюкокортикоиды нового поколения, которые не содержат атомов фтора, но при этом характеризуются высокой эффективностью и хорошим профилем безопасности (например мометазон в виде фуроата — синтетический стероид, который начал выпускаться с 1987 г. в США, метилпреднизолона ацепонат, который применяется в практике с 1994 г.).
Терапевтический эффект топических глюкокортикоидов зависит также от применяемой лекарственной формы. Глюкокортикоиды для местного применения в дерматологии выпускаются в форме мазей, кремов, гелей, эмульсий, лосьонов и др. Способность к проникновению в кожу (глубина проникновения) убывает в следующем порядке: жирная мазь>мазь>крем>лосьон (эмульсия). При хронической сухости кожи проникновение глюкокортикоидов в эпидермис и дерму затруднено, поэтому при дерматозах, сопровождающихся повышенной сухостью и шелушением кожи, лихенизацией целесообразнее применять мази, т.к. увлажнение рогового слоя эпидермиса мазевой основой в несколько раз увеличивает проникновение ЛС в кожу. При острых процессах с выраженным мокнутием целесообразнее назначать лосьоны, эмульсии.
Поскольку глюкокортикоиды для местного применения снижают сопротивляемость кожи и слизистых оболочек, что может привести к развитию суперинфекции, при вторичном инфицировании целесообразно сочетание в одной лекарственной форме глюкокортикоида с антибиотиком, например крем и мазь Дипрогент (бетаметазон + гентамицин), аэрозоли Оксикорт (гидрокортизон + окситетрациклин) и Полькортолон ТС (триамцинолон + тетрациклин) и др. , или с антибактериальным и противогрибковым средством, например Акридерм ГК (бетаметазон + клотримазол + гентамицин).
Топические глюкокортикоиды применяют при лечении таких осложнений хронической венозной недостаточности (ХВН), как трофические нарушения кожи, варикозная экзема, гемосидероз, контактный дерматит и др. Их использование обусловлено подавлением воспалительных и токсико-аллергических реакций в мягких тканях, возникающих при тяжелых формах ХВН. В отдельных случаях местные глюкокортикоиды используют для подавления сосудистых реакций, возникающих во время флебосклерозирующего лечения. Наиболее часто для этого используются мази и гели, содержащие гидрокортизон, преднизолон, бетаметазон, триамцинолон, флуоцинолона ацетонид, мометазона фуроат и др.
Применение глюкокортикоидов в офтальмологии основано на их местном противовоспалительном, противоаллергическом, противозудном действии. Показаниями к назначению глюкокортикоидов являются воспалительные заболевания глаза неинфекционной этиологии, в т.ч. после травм и операций — ирит, иридоциклит, склерит, кератит, увеит и др. С этой целью используются: гидрокортизон, бетаметазон, дезонид, триамцинолон и др. Наиболее предпочтительно применение местных форм (глазные капли или суспензия, мази), в тяжелых случаях — субъконъюнктивальные инъекции. При системном (парентерально, внутрь) использовании глюкокортикоидов в офтальмологии следует помнить о высокой вероятности (75%) развития стероидной катаракты при ежедневном использовании в течение нескольких месяцев преднизолона в дозе более 15 мг (а также эквивалентных доз других препаратов), при этом риск возрастает с увеличением длительности лечения.
Глюкокортикоиды противопоказаны при острых инфекционных заболеваниях глаз. При необходимости, например при бактериальных инфекциях, используют комбинированные препараты, содержащие в своем составе антибиотики, такие как капли глазные/ушные Гаразон (бетаметазон + гентамицин) или Софрадекс (дексаметазон + фрамицетин + грамицидин) и др. Комбинированные препараты, в состав которых входят ГК и антибиотики, широко используются в офтальмологической и оториноларингологической практике. В офтальмологии — для лечения воспалительных и аллергических заболеваний глаз при наличии сопутствующей или подозреваемой бактериальной инфекции, например при некоторых видах конъюнктивита, в послеоперационном периоде. В оториноларингологии — при наружном отите; рините, осложненном вторичной инфекцией и пр. Следует иметь в виду, что один и тот же флакон препарата не рекомендуется использовать для лечения отита, ринита и заболеваний глаз во избежание распространения инфекции.
Препараты
Препаратов - 2564 ; Торговых названий - 209 ; Действующих веществ - 27
| Действующее вещество | Торговые названия |
| Информация отсутствует | |
| |
|
| |
|
| |
|
| |
|
| |
|
| |
|
| |
|
Для цитирования:
Княжеская Н.П. Глюкокортикостероиды в терапии бронхиальной астмы // РМЖ. 2002. №5. С. 245
Кафедра пульмонологии ФУВ РГМУ
В последние годы отмечен значительный прогресс в лечении бронхиальной астмы (БА) . По-видимому, это связано с определением БА, как хронического воспалительного заболевания дыхательных путей, и вследствие этого - с широким применением ингаляционных глюкокортикостероидов (ГКС) в качестве базисных противовоспалительных препаратов. Однако несмотря на достигнутые успехи, уровень контроля над течением заболевания нельзя считать удовлетворительным. Так, например, почти каждый третий больной БА, как минимум, 1 раз в месяц просыпается ночью в связи с симптомами болезни. Более половины больных имеют ограничения физической активности, более трети вынуждены пропускать занятия в школе или отсутствовать на работе. Более 40% больных вынуждены обращаться за неотложной помощью вследствие обострения заболевания. Причины подобной ситуации многообразны, и не последнюю роль в этом играет недостаточная осведомленность врача в патогенезе БА и, соответственно, выбор неправильной тактики лечения.
Определение и классификация БА
Бронхиальная астма - хроническое заболевание дыхательных путей, в котором принимают участие многие клетки: тучные клетки, эозинофилы и Т-лимфоциты. У предрасположенных лиц это воспаление приводит к повторным эпизодам хрипов, одышки, тяжести в грудной клетке и кашлю, особенно ночью и/или ранним утром. Эти симптомы сопровождаются распространенной, но вариабельной обструкцией бронхиального дерева, которая, по крайней мере, частично обратима, спонтанно или под влиянием лечения. Воспаление также вызывает увеличение ответа дыхательных путей на различные стимулы (гиперреактивность).
Ключевыми положениями определения следует считать следующие:
1. БА - хроническое персистирующее воспалительное заболевание дыхательных путей вне зависимости от тяжести течения.
2. Воспалительный процесс приводит к гиперреактивности бронхов, обструкции и появлению респираторных симптомов.
3. Обструкция дыхательных путей обратима, по крайней мере, частично.
4. Атопия - генетическая предрасположенность к продукции иммуноглобулинов класса Е (может присутствовать не всегда).
Бронхиальную астму можно классифицировать на основе этиологии, тяжести течения и особенностей проявления бронхиальной обструкции.
Однако в настоящее время бронхиальную астму в первую очередь следует классифицировать по степени тяжести, т. к. именно это отражает степень выраженности воспалительного процесса в дыхательных путях и определяет тактику противовоспалительной терапии.
Степень тяжести определяется по следующим показателям:
- Количество ночных симптомов в неделю.
- Количество дневных симптомов в день и в неделю.
- Кратность применения b 2 -агонистов короткого действия.
- Выраженность нарушений физической активности и сна.
- Значения пиковой скорости выдоха (ПСВ) и ее процентное соотношение с должным или наилучшим значением.
- Суточные колебания ПСВ.
- Объем проводимой терапии.
Существует 5 степеней тяжести течения БА: легкая интермиттирующая; легкая персистирующая; средней тяжести персистирующая; тяжелая персистирующая; тяжелая персистирующая стероидозависимая (табл. 1).
БА интермиттирующего течения: симптомы астмы реже 1 раза в неделю; короткие обострения (от нескольких часов до нескольких дней). Ночные симптомы 2 раза в месяц или реже; отсутствие симптомов и нормальная функция легких между обострениями: пиковая скорость выдоха (ПСВ) > 80% от должного и колебания ПСВ менее 20%.БА легкого персистирующего течения . Симптомы 1 раз в неделю или чаще, но реже 1 раза в день. Обострения заболевания могут нарушать активность и сон. Ночные симптомы возникают чаще 2 раз в месяц. ПСВ более 80% от должного; колебания ПСВ 20-30%.
БА средней тяжести . Ежедневные симптомы. Обострения нарушают активность и сон. Ночные симптомы возникают более 1 раза в неделю. Ежедневный прием b 2 -агонистов короткого действия. ПСВ 60-80% от должного. Колебания ПСВ более 30%.
БА тяжелого течения: постоянные симптомы, частые обострения, частые ночные симптомы, физическая активность ограничена проявлениями астмы. ПСВ менее 60% от должного; колебания более 30%.
Необходимо отметить, что определение степени тяжести астмы по этим показателям возможно только перед началом лечения. Если больной уже получает необходимую терапию, то ее объем также должен учитываться. Таким образом, если у пациента по клинической картине определяется легкая персистирующая астма, но при этом он получает медикаментозное лечение, соответствующее тяжелой персистирующей астме, то у данного пациента диагностируется БА тяжелого течения.
БА тяжелого течения стероидозависимая: независимо от клинической картины пациент, получающий длительное лечение системными кортикостероидами, должен быть расценен, как страдающий БА тяжелого течения.
Ингаляционные ГКС
Рекомендован ступенчатый подход к терапии БА
в зависимости от тяжести ее течения (табл. 1). Все препараты для лечения БА разделены на две основные группы: для длительного контроля воспалительного процесса и средства для купирования острых симптомов астмы. Основой терапии для длительного контроля воспалительного процесса являются ингаляционные глюкокортикостероиды (ИГКС), которые следует применять, начиная со второй ступени (легкое персистирующее течение) до пятой (тяжелое стероидозависимое течение). Поэтому в настоящее время ИГКС рассматриваются в качестве средств первой линии для терапии БА. Чем выше степень тяжести течения БА, тем большие дозы ИГКС следует применять. По данным ряда исследований, у пациентов, начавших лечение ИГКС не позже двух лет от начала заболевания, отмечены существенные преимущества в улучшении контроля над симптомами астмы по сравнению с группой, начавшей лечение ИГКС по прошествии более чем 5 лет от дебюта заболевания.
Механизмы действия и фармакокинетика
ИГКС способны связываться со специфическими рецепторами в цитоплазме, активируют их и образуют с ними комплекс, который затем димеризуется и перемещается в ядро клетки, где связывается с ДНК и взаимодействует с механизмами транскрипции ключевых ферментов, рецепторов и других сложных белков. Это приводит к проявлению фармакологического и терапевтического действия.
Противовоспалительный эффект ИГКС связан с их ингибирующим действием на клетки воспаления и их медиаторы, включая продукцию цитокинов, вмешательство в метаболизм арахидоновой кислоты и синтез лейкотриенов и простагландинов, предотвращение миграции и активации клеток воспаления. ИГКС увеличивают синтез противовоспалительных белков (липокортина-1), увеличивают апоптоз и снижают количество эозинофилов путем ингибирования интерлейкина-5. Таким образом, ИГКС приводят к стабилизации клеточных мембран, уменьшают проницаемость сосудов, улучшают функцию b -рецепторов как путем синтеза новых, так и повышая их чувствительность, стимулируют эпителиальные клетки.
ИГКС отличаются от системных глюкокортикостероидов своими фармакологическими свойствами: липофильностью, быстротой инактивации, коротким периодом полувыведения из плазмы крови. Важно учитывать, что лечение ИГКС является местным (топическим), что обеспечивает выраженные противовоспалительные эффекты непосредственно в бронхиальном дереве при минимальных системных проявлениях. Количество ИГКС, доставляемое в дыхательные пути, зависит от номинальной дозы препарата, типа ингалятора, наличия или отсутствия пропеллента, а также техники выполнения ингаляции. До 80% пациентов испытывают сложности при использовании дозированных аэрозолей.
Наиболее важной характеристикой для проявления селективности и времени задержки препарата в тканях является липофильность . Благодаря липофильности ИГКС накапливаются в дыхательных путях, замедляется их высвобождение из тканей и увеличивается их сродство к глюкокортикоидному рецептору. Высоколипофильные ИГКС быстрее и лучше захватываются из просвета бронхов и длительно задерживаются в тканях дыхательных путей. ИГКС отличает от системных препаратов их топическое (местное) действие. Поэтому бесполезно назначать ингаляции системных ГКС (гидрокортизона, преднизолона и дексаметазона): эти препараты вне зависимости от способа применения обладают только системным действием.
В многочисленных рандомизированных плацебо-контролируемых исследованиях у больных БА показана эффективность всех доз ИГКС в сравнении с плацебо.
Системная биодоступность складывается из пероральной и ингаляционной. От 20 до 40% от ингалируемой дозы препарата попадает в дыхательные пути (это величина значительно варьирует в зависимости от средства доставки и от ингаляционной техники пациента). Легочная биодоступность зависит от процента попадания препарата в легкие, наличия или отсутствия носителя (лучшие показатели имеют ингаляторы, не содержащие фреон) и от абсорбции препарата в дыхательных путях. 60-80% ингаляционной дозы оседает в ротоглотке и проглатывается, подвергаясь затем полному или частичному метаболизму в желудочно-кишечном тракте и печени. Пероральная доступность зависит от абсорбции в желудочно-кишечном тракте и от выраженности эффекта «первого прохождения» через печень, благодаря чему в системный кровоток поступают уже неактивные метаболиты (за исключением беклометазона 17-монопропионата - активного метаболита беклометазона дипропионата). Дозы ИГКС до 1000 мкг/сутки (для флютиказона до 500 мкг/сут) обладают незначительным системным действием.
Все ИГКС имеют быстрый системный клиренс , сравнимый с величиной печеночного кровотока. Это один из факторов, снижающих системное действие ИГКС.
Характеристика наиболее часто используемых препаратов
К ИГКС относятся беклометазона дипропионат, будесонид, флютиказона пропионат, флунизолид, триамсинолона ацетонид, мометазона фуроат. Они выпускаются в виде дозированных аэрозолей, порошковых ингаляторов, а также в виде растворов для ингаляции через небулайзер (будесонид).
Беклометазона дипропионат . Применяется в клинической практике более 20 лет и остается одним из самых эффективных и часто используемых препаратов. Разрешено применение препарата у беременных. Выпускается в виде дозированного аэрозольного ингалятора (Бекотид 50 мкг, Беклофорте 250 мкг, Альдецин 50 мкг, Беклокорт 50 и 250 мкг, Бекломет 50 и 250 мкг/доза), дозированного ингалятора, активируемого вдохом (Беклазон Легкое Дыхание 100 и 250 мкг/доза), порошкового ингалятора (Бекодиск 100 и 250 мкг/доза ингалятор Дискхалер; мультидозовый ингалятор Изихейлер, Бекломет 200 мкг/доза). Для ингаляторов Бекотид и Беклофорте производятся специальные спейсеры - «Волюматик» (клапанный спейсер большого объема для взрослых) и «Бэбихалер» (2-клапанный спейсер малого объема с силиконовой лицевой маской для детей раннего возраста).
Будесонид . Современный высокоактивный препарат. Используется в виде дозированного аэрозольного ингалятора (Будесонид-мите 50 мкг/доза; Будесонид-форте 200 мкг/доза), порошкового ингалятора (Пульмикорт Турбухалер 200 мкг/доза; Бенакорт Циклохалер 200 мкг/доза) и суспензии для небулайзера (Пульмикорт 0,5 и 0,25 мг/доза). Пульмикорт Турбухалер - единственная лекарственная форма ИГКС, не содержащая носителя. Для дозированных ингаляторов Будесонид мите и Будесонид форте производится спейсер. Будесонид является составной частью комбинированного препарата Симбикорт.
Будесонид имеет наиболее благоприятный терапевтический индекс, что связано с его высоким сродством к глюкокортикоидным рецепторам, и ускоренным метаболизмом после системной абсорбции в легких и кишечнике. Будесонид является единственным ИГКС, для которого доказана возможность однократного применения. Фактор, обеспечивающий эффективность применения будесонида один раз в день, - ретенция будесонида в дыхательных путях в виде внутриклеточного депо благодаря обратимой эстерификации (образованию эфиров жирных кислот). При снижении концентрации свободного будесонида в клетке активируются внутриклеточные липазы, высвобождающийся из эфиров будесонид вновь связывается с рецептором. Подобный механизм не свойственен другим ГКС и позволяет пролонгировать противовоспалительный эффект. В ряде исследований показано, что внутриклеточное депонирование может оказаться более важным в плане активности препарата, чем сродство к рецептору.
Исследования последних лет по препарату Пульмикорт Турбухалер доказали, что он не влияет на конечный рост при длительном применении у детей, на минерализацию кости, не вызывает ангиопатию и катаракту. Пульмикорт также рекомендован к применению у беременных: установлено, что его применение не вызывает увеличения числа аномалий плода. Пульмикорт Турбухалер является первым и единственным ИГКС, которому FDA (организация по контролю за лекарственными средствами в США) присвоила категорию «В» в рейтинге лекарств, назначаемых при беременности. В эту категорию включаются лекарства, прием которых в период беременности является безопасным. Остальные ИГКС относятся к категории «С» (прием их во время беременности не рекомендуется).
Флютиказона пропионат . Самый высокоактивный препарат на сегодняшний день. Обладает минимальной пероральной биодоступностью (<1%). Эквивалентные терапевтические дозы флютиказона почти в два раза меньше, чем у беклометазона и будесонида в аэрозольном ингаляторе и сопоставимы с дозами будесонида в Турбухалере (табл. 2). По данным ряда исследований, флютиказона пропионат больше угнетает надпочечники, но в эквивалентных дозах имеет сходную с другими ИГКС активность в отношении надпочечников.
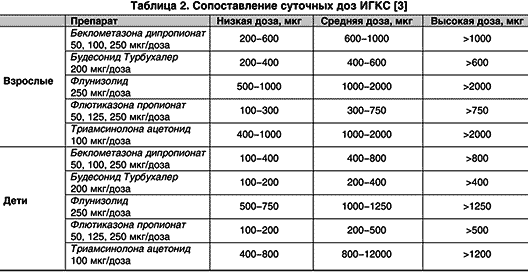
Представлен в виде дозированного аэрозольного ингалятора (Фликсотид 50, 125 и 250 мкг/доза) и порошкового ингалятора (Фликсотид Дискхалер - ротадиски 50, 100, 250 и 500 мкг/доза; Фликсотид Мультидиск 250 мкг/доза). Для аэрозольных ингаляторов производятся специальные спейсеры - «Волюматик» (клапанный спейсер большого объема для взрослых) и «Бэбихалер» (2-клапанный спейсер малого объема с силиконовой лицевой маской для детей раннего возраста). Флютиказон является составной частью комбинированного препарата Серетид Мультидиск.
Флунизолид . Препарат с низкой глюкокортикоидной активностью. На отечественном рынке представлен торговой маркой Ингакорт (дозированный ингалятор 250 мкг/доза, со спейсером). Несмотря на высокие терапевтические дозы, практически не имеет системных эффектов в связи с тем, что уже при первом прохождении через печень на 95% превращается в неактивное вещество. В настоящее время в клинической практике используется достаточно редко.
Триамсинолона ацетонид . Препарат с низкой гормональной активностью. Дозированный ингалятор 100 мкг/доза. Торговая марка Азмакорт, на российском рынке не представлен.
Мометазона фуроат . Препарат с высокой глюкокортикоидной активностью. На российском рынке представлен только в виде назального спрея Назонекс.
Клинические испытания, сравнивавшие эффективность ИГКС в виде улучшения симптомов и показателей функции внешнего дыхания, показывают, что:
- Будесонид и беклометазона дипропионат в аэрозольных ингаляторах при одинаковых дозах практически не отличаются по эффективности.
- Флютиказона пропионат обеспечивает такое же действие, как удвоенная доза беклометазона или будесонида в дозированном аэрозоле.
- Будесонид, применяемый через Турбухалер, оказывает такое же действие, как удвоенная доза будесонида в дозированном аэрозоле.
Нежелательные эффекты
Современные ИГКС относятся к препаратам с высоким терапевтическим индексом и имеют высокий профиль безопасности даже при длительном применении. Выделяют системные и местные нежелательные эффекты. Системные нежелательные эффекты могут стать клинически значимыми только при использовании высоких доз. Они зависят от сродства препаратов к рецептору, липофильности, объема распределения, периода полувыведения, биодоступности и других факторов. Риск возникновения системных нежелательных для всех имеющихся в настоящее время ИГКС коррелирует с желательными эффектами в дыхательных путях. Применение ИГКС в среднетерапевтических дозах снижает риск возникновения системных эффектов.
В основном побочные эффекты ИГКС связаны с их путем применения и сводятся к кандидозу полости рта, осиплости голоса, раздражению слизистой и кашлю. Чтобы избежать этих явлений, необходима правильная техника ингаляции и индивидуальный подбор ИГКС.
Комбинированные препараты
Несмотря на то, что ИГКС являются основой терапии БА, они не всегда позволяют полностью контролировать воспалительный процесс в бронхиальном дереве и, соответственно, проявления БА. В связи с этим возникала необходимость в назначении b 2 -агонистов короткого действия по потребности или регулярно. Таким образом появилась острая потребность в новом классе препаратов, свободных от недостатков, которые присущи b 2 -агонистам короткого действия, и обладающих доказанным длительным протективным и противовоспалительным действием на дыхательные пути.
Были созданы и в настоящее время широко применяются b 2 -агонисты длительного действия, которые на фармацевтическом рынке представлены двумя препаратами: формотерола фумаратом и сальметерола ксинафоатом. В современных руководствах по терапии астмы рекомендовано добавление b 2 -агонистов длительного действия при недостаточном контроле БА монотерапией ингаляционными ГКС (начиная со второй ступени). В ряде исследований было показано, что комбинация ингаляционного ГКС с b 2 -агонистом длительного действия более эффективна, чем удвоение дозы ингаляционных ГКС, и приводит к более значимому улучшению функции легких и лучшему контролю над симптомами астмы. Было показано также снижение количества обострений и значимое улучшение качества жизни у пациентов, получающих комбинированную терапию. Таким образом, появление комбинированных препаратов, содержащих ингаляционный ГКС и b 2 -агонист длительного действия, - отражение эволюции взглядов на терапию БА.
Главным преимуществом комбинированной терапии является повышение эффективности лечения при использовании более низких доз ИГКС. Кроме того, соединение двух препаратов в одном ингаляторе облегчает пациенту выполнение назначений врача и потенциально улучшает комплайнс.
Серетид Мультидиск . Составными компонентами являются сальметерола ксинафоат и флютиказона пропионат. Обеспечивает высокий уровень контроля над симптомами БА. Используется только в качестве базисной терапии, может назначаться, начиная со второй ступени. Препарат представлен в различных дозировках: 50/100, 50/250, 50/500 мкг сальметерола/флютиказона в 1 дозе. Мультидиск относится к ингаляционным устройствам малого сопротивления, что позволяет использовать его и у пациентов со сниженной скоростью вдоха.
Симбикорт Турбухалер . Составными компонентами являются будесонид и формотерола фумарат. На российском рынке представлен в дозировке 160/4,5 мкг в 1 дозе (дозы препаратов указаны как доза на выходе). Важная особенность Симбикорта - возможность использовать его как для базисной терапии (для контроля воспалительного процесса), так и для немедленного облегчения симптомов астмы. Это обусловлено прежде всего свойствами формотерола (быстрое начало действия) и способностью будесонида активно действовать в течение 24 часов на слизистую бронхиального дерева.
Симбикорт дает возможность индивидуального гибкого дозирования (1-4 ингаляционные дозы в сутки). Симбикорт можно использовать, начиная со 2 ступени, но особенно он показан пациентам с нестабильной астмой, для которой характерны внезапные тяжелые приступы затрудненного дыхания.
Системные ГКС
Системные ГКС применяются в основном для купирования обострения БА. Наиболее эффективны пероральные ГКС. Внутривенно кортикостероиды назначают при обострении БА, если более желателен внутривенный доступ, или при нарушении всасывания из желудочно-кишечного тракта, используя высокие дозы (до 1 г преднизолона, метилпреднизолона и гидрокортизона). Кортикостероиды приводят к клинически значимому улучшению спустя 4 часа после их введения.
При обострении БА показан короткий курс пероральных ГКС (7-14 дней), причем начинают с высоких доз (30-60 мг преднизолона). В последних публикациях рекомендуют следующий короткий курс системных ГКС при не угрожающих жизни обострениях: 6 таблеток преднизолона утром (30 мг) в течение 10 дней с последующим прекращением приема. Хотя схемы лечения системными ГКС могут быть различными, основополагающими принципами являются назначение их в высоких дозах для быстрого достижения эффекта и последующая быстрая отмена. Следует помнить, что как только пациент оказывается готовым к приему ингаляционных ГКС, они должны быть ему назначены с соблюдением ступенчатого подхода.
Системные глюкокортикоиды следует назначить, если:
- Обострение средней тяжести или тяжелое.
- Назначение ингаляционных b 2 -агонистов короткого действия в начале лечения к улучшению не привело.
- Обострение развилось, несмотря на то, что больной находился на длительном лечении пероральными кортикостероидами.
- Для купирования предыдущих обострений требовались пероральные кортикостероиды.
- 3 и более раз в год проводились курсы глюкокортикоидов.
- Больной находится на ИВЛ.
- Ранее были угрожающие жизни обострения.
Нежелательно использование пролонгированных форм системных стероидов для купирования обострений и проведения поддерживающей терапии БА.
Для длительной терапии при тяжелом течении БА системные ГКС (метилпреднизолон, преднизолон, триамсинолон, бетаметазон) следует назначать в наименьшей эффективной дозе. При длительном лечении альтернирующая схема назначения и прием в первой половине дня (для уменьшения влияния на циркадные ритмы секреции кортизола) вызывают наименьшее количество побочных эффектов. Следует подчеркнуть, что во всех случаях назначения системных стероидов больному должны быть назначены высокие дозы ингаляционных ГКС. Из пероральных ГКС предпочтение отдается тем, у которых отмечается минимальная минералокортикоидная активность, относительно короткий период полураспада и ограниченное действие на поперечно-полосатую мускулатуру (преднизолон, метилпреднизолон).
Стероидозависимость
Пациентам, которые вынуждены постоянно принимать системные ГКС, следует уделять особое внимание. Существует несколько вариантов формирования стероидозависимости у пациентов с БА и другими заболеваниями, сопровождающимися бронхообструкцией:
- Отсутствие комплайенса (взаимодействия) врача и пациента.
- Неназначение ингаляционных ГКС пациентам. Многие врачи считают, что нет необходимости назначать ингаляционные ГКС больным, получающим системные стероиды. Если пациент с БА получает системные стероиды, его следует расценивать, как больного с тяжелой формой БА, имеющего прямые показания к назначению высоких доз ингаляционных ГКС.
- У больных системными заболеваниями (включая легочные васкулиты, например, синдром Чардж-Стросса) бронхиальная обструкция может быть расценена, как БА. Отмена системных стероидов у этих больных может сопровождаться тяжелыми проявлениями системного заболевания.
- В 5% случаев встречается стероидорезистентность, для которой характерна резистентность стероидных рецепторов к стероидным препаратам. В настоящее время различают две подгруппы: больные с истинной стероидной резистентностью (тип II), не имеющие побочных эффектов при длительном приеме высоких доз системных ГКС, и пациенты с приобретенной резистентностью (тип I) - имеющие побочные эффекты системных ГКС. В последней подгруппе резистентность можно преодолеть, скорее всего, повышением дозы ГКС и назначением препаратов, имеющих аддитивный эффект.
1. Бронхиальная астма. Глобальная стратегия: совместный доклад Национального института Сердце, Легкие, Кровь и Всемирной организации здравоохранения. Пульмонология, 1996.
2. Бронхиальная астма. Руководство для врачей России (формулярная система). «Пульмонология», приложение-99.
3. Ведущие направления в диагностике и лечении бронхиальной астмы. Основные положения отчета группы экспертов EPR-2. National Institute of Health. National Heart, Lung and Blood Institute. NIH publication-97. Перевод под ред. Проф. Цой А.Н., М, Грантъ,1998.
4. Ильина Н.И. Ингаляционные глюкокортикоиды. Астма.ru. Аллергические и респираторные заболевания. 0*2001 (пилотный выпуск).
5. Огородова Л.М. Системы ингаляционной доставки препаратов в дыхательные пути. Пульмонология, 1999; №1, 84-87
6. Формулярная система: лечение бронхиальной астмы. Астма. ru ,0. 2001, 6-9
7. Чучалин А.Г. Бронхиальная астма. Москва, 1997.
8. Цой А.Н. Ингаляционные глюкокортикоиды: эффективность и безопасность. РМЖ 2001; 9: 182-185
9. Цой А.Н. Сравнительная фармакокинетика ингаляционных глюкокортикоидов. Аллергология 1999; 3: 25-33
10. Agertoft L., Pedersen S. Effect of long-term treatment with inhaled budesonide on adult height in children with asthma. N Engl J Med 2000; 343: 1064-9
11. Ankerst J., Persson G., Weibull E. A high dose of budesonide/formoterol in a single inhaler was well tolerated by asthmatic patients. Eur Respir J 2000; 16 (Suppl 31): 33s+poster
12. Barnes P.J. Inhaled glucocorticoides for asthma. N. Engl. Med. 1995; 332: 868-75
13. Beclomethasone Dipropionate and Budesonide. The clinical evidence Reviewed. Respir Med 1998; 92 (Suppl B)
14. The British Guidelines on Asthma Management. Thorax, 1997; 52 (Suppl. 1) 1-20.
15. Burney PGJ. Current questions in the epidemiology of asthma, in Holgate ST, et al, Asthma: Physiology. Immunology, and Treatment. London, Academic Press, 1993, pp 3-25.
16. Crisholm S et al. Once-daily budesonide in mild asthma. Respir Med 1998; 421-5
17. Kips JC, O/Connor BJ, Inman MD, Svensson K, Pauwels RA, O/Byrne PM. A long-termed study of the antiinflammatory effect of low-dosed budesonide plus formoterol versus high-dosed budesonide in asthma. Am Respir Crit Care Med 2000; 161: 996-1001
18. McFadden ER, Casale TB, Edwards TB et al. Administration of budesonide once daily by means of Turbuhaler to subjects with stable asthma. J Allergy Clin Immunol 1999; 104: 46-52
19. Miller-Larsson A., Mattsson H., Hjertberg E., Dahlback M., Tunek A., Brattsand R. Reversible fatty acid conjugation of budesonide: novel mechanism foe prolonged retention of topically applied steroid in airway tissue. Drug Metab Dispos 1998; 26: 623-30
20. Miller-Larsson A. et al. Prolonged airway activity and improved selectivity of budesonide possibly due to esterification. Am J Respir Crit Care Med 2000;162: 1455-1461
21. Pauwels RA et al. Effect of inhaled formoterol and budesonide on exacerbations of asthma. N Engl J Med 1997; 337: 1405-11
22. Pedersen S, O/Byrne P. A comparison of the efficacy and safety of inhaled corticosteroides in asthma. Allergy 1997; 52 (Suppl 39): 1-34.
23. Woolcock A.et al. Comparison of addition of salmeterol to inhaled steroids with doubling of the dose of inhaled steroids. Am J Respir Crit Care Med, 1996, 153, 1481-8.
Центральным звеном в патогенезе бронхиальной астмы (БА) является хроническое аллергическое воспаление нижних дыхательных путей . Это обстоятельство определяет выбор глюкокортикостероидов (ГКС) в качестве основных и наиболее эффективных лекарственных средств (ЛС), применяемых для базовой (ежедневной) терапии БА и лечения обострений этого заболевания .
ГКС в настоящее время рассматриваются как наиболее эффективные препараты для базовой терапии БА. Согласно принятой в доказательной медицине шкале оценки, применение ГКС относится к рекомендациям высшего уровня (уровень рекомендаций А). В большом числе исследований применение этих ЛС сопровождалось значительным улучшением функции дыхания, ростом показателей спирометрии, уменьшением выраженности симптомов бронхиальной астмы, снижением бронхиальной гиперреактивности и улучшением качества жизни (уровень доказательности А). Таким образом, ГКС положительно воздействуют практически на все проявления БА и должны постоянно применяться у всех больных, за исключением пациентов с легким интермиттирующим течением заболевания .
Широкое внедрение ГКС в практику лечения БА стало возможно лишь с появлением форм, использующихся для ингаляций. Применение ингаляций ГКС позволило, во-первых, усилить местные (по отношению к дыхательным путям) эффекты кортикостероидной терапии, а во-вторых, уменьшить выраженность и частоту нежелательных лекарственных реакций (НЛР), связанных с системным действием этих препаратов.
Использование ГКС в виде ингаляций позволяет полностью избежать у больных развития таких грозных осложнений ГКС-терапии, как язва верхних отделов желудочно-кишечного тракта, стероидный диабет и гипертензия. С другой стороны, при применении ГКС в форме ингаляций реже возникают такие НЛР, как синдром Кушинга, вторичная надпочечниковая недостаточность, глаукома и т. д. .
Вместе с тем при всех достоинствах этого метода ингаляционные ГКС в ряде случаев оказываются недостаточно эффективными.
- У больных с обострением БА или очень тяжелым течением заболевания, сопровождающимся значительным снижением бронхиальной проходимости, применение ингаляционных ГКС неэффективно, так как выраженная бронхообструкция существенно снижает поступление этих ЛС в средние и нижние отделы дыхательных путей. Считается, что при бронхообструкции, при которой величина пиковой скорости выдоха снижается до уровня менее 200 мл/с, применение ингаляционных ГКС малоэффективно .
- У ряда пациентов (пожилой возраст, заболевания протекающие с нарушением памяти и интеллекта) при использовании ингаляторов возникают значительные проблемы, которые часто оказывается невозможно устранить, что в свою очередь не позволяет проводить полноценную ингаляционную терапию.
- При очень тяжелом течении астмы или наличии относительной резистентности больного к действию ГКС может отмечаться полная или частичная неэффективность ингаляционных ГКС при их использовании в больших дозах .
- Ингаляционные ГКС практически неэффективны у ряда больных, страдающих особыми клиническими формами БА, например БА с лабильным течением1 .
Таким образом, вопрос о применении системных ГКС (ГКС для приема внутрь, внутривенно или внутримышечно в виде препаратов пролонгированного действия — депо-форм) остается достаточно актуальным, несмотря на высокий риск НЛР и наличие менее «опасных» ингаляционных форм.
Выбор препарата для системного применения
Современные руководства по клинической практике рекомендуют применять для лечения БА средства, обеспечивающие сочетание высокой противовоспалительной и минимальной минералокортикоидной активности. Из таблицы видно, что в наибольшей степени этим требованиям отвечают такие ЛС, как преднизолон и метилпреднизолон.
Фармакокинетика системных ГКС, применяемых для терапии БА
С точки зрения фармакокинетики эти ЛС отличает высокая (около 100%) биодоступность при приеме внутрь. У преднизолона и метилпреднизолона максимальная концентрация в крови отмечается уже через 0,5—1,5 ч после приема. На скорость их всасывания может оказывать влияние одновременный прием пищи — при этом скорость всасывания уменьшается, но биодоступность остается на прежнем уровне. Эти ЛС быстро метаболизируются в печени (период полувыведения составляет соответственно 60 и 200 мин) и выделяются с мочой в виде конъюгатов серной и глюкуроновой кислот.
Вместе с тем благодаря высокой липофильности преднизолон и метилпреднизолон активно распределяются в тканях организма, а период полувыведения из тканей составляет у них 0,5—1,5 сут. .
Эффективность ГКС усиливается при одновременном назначении эритромицина (замедляет метаболизм глюкокортикоидов в печени), салицилатов (увеличение не связанной с белками фракции глюкокортикоидов), эстрогенов. Индукторы микросомальных ферментов печени — фенобарбитал, фенитоин, рифампицин — снижают эффективность этих ЛС.
ГКС ослабляют действие антикоагулянтов, антидиабетических и антигипертензивных препаратов и усиливают действие теофиллина, симпатомиметиков, иммуносупрессоров, нестероидных противовоспалительных средств.
Важным для терапии БА является взаимодействие ГКС с b2-адреностимуляторами. При систематическом приеме стимуляторов b2-адренорецепторов достаточно быстро развивается толерантность к их бронхолитическому действию (происходит снижение чувствительности рецепторов — десенситизация и уменьшение их числа — down-регуляция) . ГКС способны увеличивать число b-адренорецепторов, повышая их транскрипцию, и препятствуют развитию десенситизации и down-регуляции .
Фармакодинамика и НЛР системных ГКС, применяемых для терапии БА
По своим фармакодинамическим особенностям преднизолон и метилпреднизолон практически не отличаются друг от друга. Оба препарата обладают выраженным противовоспалительным действием (преимущественно при аллергической и иммунной формах воспалительного процесса), подавляют синтез простагландинов, лейкотриенов и цитокинов, вызывают уменьшение проницаемости капилляров, снижают хемотаксис иммунокомпетентных клеток и подавляют активность фибробластов, Т-лимфоцитов, макрофагов и эозинофилов .
С другой стороны, применение этих ЛС приводит к задержке в организме натрия и воды (благодаря увеличению реабсорбции в дистальных почечных канальцах) и увеличению массы тела.
Уменьшение под воздействием ГКС всасывания кальция с пищей, снижение его накопления в костной ткани и усиленная экскреция кальция с мочой создают предпосылки для развития другой НЛР ГКС — остеопороза. При длительном применении преднизолона и метилпреднизолона отмечается развитие синдрома Кушинга, стероидного диабета, стимуляция катаболических процессов в коже, костной ткани и мышцах (вплоть до развития мышечной дистрофии и поражений кожных покровов). Эти препараты могут вызывать повышение уровня артериального давления (стероидная гипертензия), лимфоцитопению, моноцитопению и эозинопению.
Длительное применение системных ГКС (особенно в сочетании с хронической гипоксией) вызывает образование стероидных язв желудка и повышает риск кровотечения из верхних отделов ЖКТ.
Одним из самых неприятных последствий длительного использования ГКС является развитие вторичной надпочечниковой недостаточности при отмене ГКС. Риск возникновения вторичной надпочечниковой недостаточности существенно повышается:
- при использовании доз > 2,5-5 мг/сут. (в пересчете на преднизолон2);
- при продолжительности лечения > 10-14 дней;
- при приеме препаратов в вечерние часы.
Особенности фармакодинамики системных ГКС у больных БА
При приеме 40 мг преднизолона внутрь препарат начинает действовать (показатель, оцениваемый у больных БА по величине прироста объема форсированного выдоха за 1-ю секунду — ОФВ1) уже через 3 ч после приема препарата . Максимальный эффект (по влиянию на бронхиальную проходимость) отмечается через 9 ч после приема препарата и сохраняется даже спустя 24 ч после однократного приема. Уровень ОФВ1 достигает исходной величины через 36 ч . Эти данные относятся к больным БА в стабильном состоянии. Метаанализ применения ГКС у больных с тяжелым (уровень ОФВ1 <50% от должной величины) обострением БА показал, что значимое увеличение ОФВ1 у больных с обострением наблюдается не ранее чем через 12—24 ч после начала лечения3 .
При многократном назначении ГКС внутрь у пациентов со стабильным течением БА (преднизолон по 20 мг в день в течение 3 недель) в первую неделю лечения у 70% больных наблюдалось улучшение бронхиальной проходимости (прирост уровня ОФВ1 >10% от исходного). При этом максимальный ответ на лечение преднизолоном был отмечен уже спустя 5,1 сут. .
В целом эффективность системных ГКС у больных БА носит дозозависимый характер и повышается при постоянном приеме этих ЛС по сравнению с альтернирующим . Эффективность системных ГКС при купировании обострений БА (оценивается по числу больных, которые благодаря использованию системных ГКС избежали госпитализации в стационар) значительно выше, если они применяются в течение первого часа после появления симптомов обострения .
ПРИМЕНЕНИЕ СИСТЕМНЫХ ГКС НА ПРАКТИКЕ С ТОЧКИ ЗРЕНИЯ ДОКАЗАТЕЛЬНОЙ МЕДИЦИНЫ
С точки зрения доказательной медицины для назначения системных ГКС можно выделить несколько показаний .
Терапия обострения БА
Согласно глобальной стратегии по бронхиальной астме, системные ГКС должны применяться при всех обострениях БА4 (уровень рекомендаций A), кроме самых легких, особенно в тех случаях, когда :
- после первого введения b2-агонистов не отмечается длительного улучшения состояния больного;
- обострение БА развилось несмотря на то, что больной уже принимает ГКС внутрь;
- предшествующие обострения требовали приема системных ГКС;
- необходимо увеличение доз ингаляционных ГКС при обострениях БА (уровень рекомендаций D).
- Подобного мнения придерживаются эксперты Британского торакального общества, которое также выработало свои критерии назначения системных ГКС при обострениях астмы (уровень рекомендаций D) :
- ухудшение состояния и усиление симптомов "день ото дня";
- падение пиковой скорости выдоха ниже 60% от индивидуального лучшего показателя;
- нарушение сна из-за симптомов БА;
- постоянное наличие симптомов астмы в утренние часы (до полудня);
- уменьшение ответа на ингаляционные бронхолитические средства;
- появление/увеличение потребности в ингаляциях бронхолитических средств.
Исходя из этих рекомендаций для купирования обострений ГКС следует принимать перорально, так как назначение этих ЛС внутривенно не обеспечивает дополнительных преимуществ. Внутривенно ГКС должны применяться только у тех больных, которые по ряду причин не могут принимать таблетированные ЛС (уровень рекомендаций А).
Лучшие результаты отмечаются при назначении ГКС в течение первого часа после появления симптомов обострения (уровень рекомендаций В) .
Лечение обострения начинают с применения преднизолона внутрь в дозах от 60 до 80 мг или гидрокортизона — от 300 до 400 мг в день. Эти дозы являются адекватными для большинства госпитализированных пациентов (уровень рекомендаций В) .
Продолжать терапию ГКС следует в течение 10-14 дней у взрослых и 3—5 дней у детей (уровень рекомендаций D), хотя в ряде случаев, например при длительном сохранении симптомов обострения, курс лечения может быть продлен до трех недель (уровень рекомендаций С) .
Доказательств преимуществ постепенного снижения доз пероральных ГКС не существует (уровень рекомендаций B) , поэтому отмену ГКС следует проводить одномоментно. Разумеется, в этом случае больной должен заранее (за несколько дней до отмены преднизолона) начать прием ингаляционных ГКС.
Постепенное снижение дозы показано в тех случаях, когда больной принимал системные ГКС более 2—3 недель. В этом случае дозу уменьшают постепенно (в течение нескольких недель). Аналогичная ситуация может возникнуть и в том случае, когда больному не были заблаговременно назначены ингаляционные ГКС, так как нельзя отменять прием ГКС внутрь до присоединения к терапии ингаляционных ГКС.
Обычно после выписки из стационара пациенты продолжают прием системных ГКС (30—60 мг/сут.), по крайней мере, в течение 7—10 дней5 (уровень рекомендаций А) , особенно если в условиях стационара не были назначены ингаляционные ГКС.
Тяжелое течение БА
Больные с очень тяжелым течением БА, у которых симптомы заболевания сохраняются несмотря на применение максимальных доз ингаляционных ГКС, являются кандидатами для терапии системными ГКС. При этом назначению ГКС внутрь должно предшествовать применение всех имеющихся в распоряжении врача дополнительных средств для контроля за течением БА (пролонгированные b2-агонисты, пролонгированные теофиллины и т. д.) (уровень рекомендаций А) . Больные, требующие постоянного приема ГКС внутрь, должны наряду с этим получать ингаляционные ГКС (уровень рекомендаций А) , для того чтобы уровень поддерживающей дозы был минимальным. Для длительной терапии пероральными ГКС прием препаратов следует назначать однократно утром каждый день или через день .
«Трудная» астма
«Трудная» астма — термин, который ввел в медицинский обиход Barnes в середине 90-х годов . Это понятие объединяет несколько форм бронхиальной астмы, представляющих особые трудности для терапии: лабильная астма (см. выше), БА, связанная с менструальным циклом, ГКС-резистентная астма, БА у больных с гиперчувствительностью к грибковым и профессиональным аллергенам и т. д. Отличительной чертой большинства форм «трудной» астмы является необходимость ежедневного приема ГКС внутрь (в ряде случаев в высоких дозах).
Безопасность лечения
Применение ГКС внутрь требует постоянного контроля со стороны врача за безопасностью лечения и коррекции неизбежных осложнений. Больной должен быть информирован о возможных НЛР, а также использовать простейшие правила их профилактики (например, прием препарата только в утренние часы).
Наиболее актуальными в этом плане представляются следующие меры:
- тщательный сбор и анализ жалоб, связанных с верхними отделами ЖКТ, при подозрении на развитие стероидной язвы - проведение ЭГДС; профилактическое назначение противоязвенных средств у больных с заболеваниями желудка в анамнезе (ранитидин или омепрозол по 1 таблетке на ночь);
- контроль уровня АД и его медикаментозная коррекция;
- регулярное исследование уровня сахара крови;
- регулярное обследование у окулиста;
- ежегодное проведение денситометрии6, профилактическое назначение препаратов кальция, витамина D3;
- исследования, направленные на выявление грибковых инвазий и туберкулеза.
У больных герпесом, а также у лиц, контактировавших с больными ветряной оспой, применение ГКС необходимо немедленно прекратить.
Заключение
Системные ГКС продолжают занимать важное место в терапии БА благодаря своей высокой эффективности, однако их применение неизбежно сопровождается развитием НЛР. Цель врача — правильно определить показания к использованию системных ГКС, максимально уменьшить объем их использования за счет комбинирования с ингаляционными ГКС и другими ЛС (пролонгированные b2-агонисты, пролонгированные теофиллины и т. д.) или применения альтернирующих курсов лечения.
С другой стороны, не следует пренебрегать назначением коротких (и относительно безопасных) курсов ГКС у больных с обострением БА или оттягивать их назначение до последнего. Применение ГКС внутрь представляет собой общепризнанную терапевтическую тактику лечения БА и служит в первую очередь интересам самого больного.
Однако во всех случаях применения ГКС необходим целенаправленный контроль и последующая коррекция неизбежно возникающих НЛР.
А. Н. Цой
, доктор медицинских наук, профессор
В. В. Архипов
ММА им. И. М. Сеченова, Москва
Литература
- Barnes P. J., Chung K. F., Page C. P. Inflammatory Mediators of Asthma: An Update // PHARM. REV. 1998. Vol. 50. № 4. 515-596.
- NHLBI/WHO Workshop Report: Global Strategy for Asthma Management and Prevention // NIH Publication. № 02-3659. February 2002. P. 1-177 (рус. перевод М.: Атмосфера, 2002).
- Доказательная медицина // Клиническая фармакология. 1999. 6. с. 3-9.
- Barnes P. J., Pedersen S., Busse W. W. Efficacy and safety of inhaled corticosteroids // Am. J. Respi. Crit. Care Med. 1998. 157. s 51-s 53.
- Lipworth B. J. Treatment of acute asthma // Lancet. 1997. 350 (suppl. II). P. 18-23.
- Barnes P. J., Woolcock A .J. Difficult asthma // Eur. Respir. J. 1998. 12: 1209-1218.
- Ayres J. G. Classification and management of brittle asthma // Br. J. Hosp. Med. 1997. 57: 387-389.
- Mosby"s Drug Consult. Mosby"s GenRx(r), 2002, 12th ed. Версия для Internet. Web site: www.mdconsult.com
- Barnes P. J., Chung K. F., Page C. P. Inflammatory Mediators of Asthma: An Update // PHARM. REV. 1998. Vol. 50. №. 4. 515-596.
- Barnes P. J. Effects of b2-agonists and steroids on b2-adrenoreceptor // Eur. Respir. Rev. 1998. 8: 55; 210-215.
- Kia Soong Tan, McFarlane L. C., Lipworth B. J. Concomitant Administration of Low-Dose Prednisolone Protects Against In Vivo beta2-Adrenoceptor Subsensitivity Induced by Regular Formoterol. Chest 1998; Vol. 113: № 1; 34-41.
- Mak J. C. W., Nishikawa M., Barnes P. J. Glucocorticosteroids increase b2-adrenergic receptor transcription in human lung // Am. J. Physiol. 1995. 268: L41-46.
- Ellul-Micallef R., Borthwick R. C., McHardy G. J. R. The time course of response to prednisolone in chronic bronchial asthma // Clinical Science and Molecular Medicine Clin. Sci. Mod. Med. 1974. 47 105-117.
- Ellul-Micallef R., Borthwick R. C., McHardy G. J.R. The effect of oral prednisolone on gas exchange in chronic bronchial asthma // Br. J. Clin. Pharmacol. 1980. 9: 479-482.
- Ellul-Micallef R., Johansson S. A. Acute dose response studies in bronchial asthma with a new corticosteroid, budesonide // Br. J. Clin. Pharmacol. 1983. 15: 419-422.
- Rodrigo G, Rodrigo C. Corticosteroids in the emergency department therapy of acute adult asthma // Chest. 1999. 116: 285-295.
- Webb J., Clark T. J. H., Chilvers C. Time course of response to prednisolone in chronic airflow obstruction. Thorax. 1981. 36: 18-21.
- Lin R. Y., Persola G. R., Westfal R. E. Early Parenteral Corticosteroid Administration in Acute Asthma // American Journal of Emergency Medicine. Volume 15. № 7. November 1997. P. 621-625.
- Canаdian asthma consensus report, 1999 // CMAJ. 1999; 161 .
- The British Guidelines on Asthma Management: 1995 review and position statement. Thorax, 1997; 52 (suppl I): 1-21.
2 Преднизолон в дозе 5 мг по своей ГКС-активности эквивалентен 4 мг метилпреднизолона.
3 При этом трудно дефференцировать прирост ОФВ1 вследствие противовоспалительного действия ГКС от увеличения ОФВ1 под влиянием бронхолитиков, которые получали все больные с тяжелым обострением БА.
4 Под обострением БА понимают:
- обращение за скорой медицинской помощью и/или госпитализацию в стационар в связи с ухудшением течения БА;
- необходимость в приеме ГКС внутрь;
- значительное (>2 раз) увеличение потребности в ингаляциях b2-агонистов по сравнению с исходным периодом на протяжении двух или более дней подряд;
- снижение уровня пиковой скорости выдоха или объема форсированного выдоха за 1-ю секунду <50% от должного значения.
5 Pекомендация западных специалистов, где, как правило, продолжительность госпитализации невелика.
6 Особенно важно контролировать показатели минерального обмена костной ткани у женщин менопаузального возраста, у лиц с неблагоприятной наследственностью, у больных с переломами конечностей в анамнезе и т. д.
Ингаляционные глюкокортикостероиды в лечении бронхиальной астмы
В настоящее время ингаляционные глюкокортикостероиды (ИГКС) являются наиболее эффективными препаратами для базисной терапии бронхиальной астмы (БА). В большом числе исследований доказана способность ИГКС уменьшать выраженность симптомов БА, улучшать функцию внешнего дыхания (ФВД), снижать гиперреактивность бронхов, в итоге приводя к улучшению качества жизни.
В клинической практике при БА в настоящее время используют следующие ИГКС (табл. 1):
Беклометазона дипропионат (БДП);
Будесонид (БУД);
Триамцинолона ацетонид (ТА);
Флунизолид (ФЛУ);
Флутиказона пропионат (ФП).
Механизм действия ИГКС
Для возникновения противовоспалительного эффекта молекула глюкокортикостероида (ГКС) должна активировать внутриклеточный рецептор. Молекулы ГКС, осевшие при ингаляции на поверхности эпителия дыхательных путей, благодаря своей липофильности диффундируют через клеточную мембрану и проникают в цитоплазму клетки. Там они взаимодействуют со связывающей областью стероидного рецептора, образуя комплекс ГКС-рецептор. Этот активный комплекс за счет формирования димера проникает через ядерную мембрану и связывается с геном-мишенью в участке, называемом элементом ГКС-ответа. В результате ГКС влияет на генную транскрипцию, подавляя транс-
^ А.Б. Строк
Кафедра клинической фармакологии РГМУ
крипцию провоспалительных молекул или увеличивая транскрипцию противовоспалительных. Этот процесс называется трансактивацией.
В конце взаимодействия рецепторный комплекс отрывается от ДНК или фактора транскрипции, ГКС-составляющая высвобождается и подвергается метаболизму, а
Таблица 1. Препараты ИГКС
Торговое Действующее Форма выпуска
название вещество (разовая доза, мкг)
Беклазон Эко
Беклазон Эко Легкое дыхание
Беклоджет
Беклофорте
Бенакорт
Пульмикорт
суспензия
Пульмикорт
турбухалер
Фликсотид Серетид*
БДП ДАИ (100, 250)
БДП ДАИ, активируемый вдохом (100 , 250)
БДП ДАИ со спейсером (250)
БДП ДАИ (250)
БДП ДАИ (50, 100)
БУД ДПИ (200)
БУД Суспензия для ингаляции через небулайзер (250, 500 мкг/мл)
БУД ДПИ (100, 200)
ФП ДАИ (25, 50, 125, 250), ДПИ (50, 100, 250, 500)
Симбикорт
турбухалер*
Сальме- ДПИ (50/100, 50/250, терол + 50/500), ДАИ (25/50, + ФП 25/125, 25/250)
БУД + ДПИ (80/4,5; 160/4,5) + фор-мотерол
Обозначения: ДАИ - дозированный аэрозольный ингалятор, ДПИ - дозированный порошковый ингалятор. * Комбинированные препараты, содержащие ИГКС и длительнодействующий в2-агонист.
Клиническая фармакология
Таблица 2. Фармакокинетические показатели ИГКС (по Expert Panel Report-2, 1997; Цой А.Н., 1999)
Фармакокинетические БДП БУД ТА ФЛУ ФП
показатели
Пероральная биодоступность, % 20 11 23 20 <1
Ингаляционная биодоступность, % 25 28 22 39 16
Свободная фракция препарата в плазме, % 13 12 29 20 10
?! § о к л CQ 0,1 2,8 2,0 1,6 7,8
Местная активность* 600 980 3 О 3 О 1200
Время полудиссоциации с ГКС-рецептором, ч 7,5 5,1 ,9 3, 3,5 10,5
Аффинность к ГКС-рецептору** 13,5 9,6 3, 1,8 18,0
Системный клиренс, л/ч 230 84 37 58 69
* В тесте МакКензи, где активность дексаметазона принята за 1. ** По сравнению с дексаметазоном.
рецептор вступает в новый цикл функционирования.
Фармакокинетика ИГКС
ИГКС различаются по соотношению системного действия и местной противовоспалительной активности, которая часто оценивается по сосудосуживающему эффекту препаратов на кожу (тест МакКензи).
Местная активность ИГКС определяется следующими их свойствами:
Липофильность;
Способность задерживаться в тканях;
Неспецифическое (не рецепторное) тканевое сродство;
Сродство к ГКС-рецепторам;
Степень первичной инактивации в печени;
Длительность связи с клетками-мишенями.
Фармакокинетические показатели ИГКС представлены в табл. 2.
Биодоступность ИГКС складывается из биодоступности дозы, абсорбированной из
желудочно-кишечного тракта (ЖКТ), и биодоступности дозы, абсорбированной из легких. При использовании ДАИ (без спейсера) приблизительно 10-20% дозы препарата попадает в легкие и затем в системный кровоток, а большая часть (около 80%) проглатывается. Конечная системная биодоступность этой фракции зависит от эффекта первого прохождения через печень. Безопасность препарата определяется, главным образом, его биодоступностью из ЖКТ и находится в обратной пропорциональной зависимости от нее.
Меры, уменьшающие оседание препарата в ротоглотке (применение спейсера, активируемого вдохом ДАИ, полоскание рта и горла после ингаляции), значительно снижают пероральную биодоступность ИГКС. Снизить количество ГКС, поступающего в кровоток из легких, теоретически можно, если усилить его метаболизм в легких, но при этом снижается и сила местного действия.
ИГКС различаются и по липофильности. Наиболее липофильный препарат - ФП, далее располагаются БДП и БУД, а ТА и ФЛУ являются гидрофильными препаратами.
Клиническая эффективность ИГКС
Значительный интерес представляет выбор суточной дозы ИГКС, в результате назначения которой можно достигнуть быстрого и устойчивого эффекта.
Доза ИГКС, необходимая для предотвращения обострений БА, может отличаться от необходимой для контроля симптомов стабильной БА. Показано, что низкие дозы ИГКС эффективно уменьшают частоту обострений и потребность в Р2-агонис-тах, улучшают показатели ФВД, снижают выраженность воспаления в дыхательных путях и бронхиальную гиперреактивность, но для лучшего контроля воспаления и максимального снижения бронхиальной гиперреактивности требуются высокие до-
зы ИГКС. Кроме того, контроль течения БА может быть достигнут значительно быстрее при применении более высоких доз ИГКС (уровень доказательности А). Однако с повышением дозы ИГКС увеличивается вероятность системных нежелательных эффектов (НЭ). Тем не менее ИГКС в низких и средних дозах редко вызывают клинически значимые НЭ и характеризуются хорошим соотношением риск/польза (уровень доказательности А).
Все это свидетельствует о необходимости корректировать терапию ИГКС (дозировки, смена препарата или устройства доставки) в зависимости от состояния больного и с учетом фармакокинетического профиля ИГКС. Приведем основные позиции медицины доказательств относительно применения ИГКС при БА.
Все препараты ИГКС в эквипотентных дозах одинаково эффективны (уровень доказательности А).
Данные о дозозависимости эффектов ФП неоднозначны. Так, некоторые авторы отмечают их дозозависимое возрастание, тогда как в других исследованиях применение низких (100 мкг/сут) и высоких (1000 мкг/сут) доз ФП оказывается эффективным практически в равной степени.
Рандомизированное двойное слепое плацебоконтролируемое исследование START (Inhaled Steroid Treatment as Regular Therapy in Early Asthma Study) было призвано получить ответ на вопрос о пользе раннего назначения ИГКС (будесонида) пациентам с легкой БА. При анализе динамики ФВД был подтвержден благоприятный эффект ранней терапии ИГКС.
При применении ИГКС 4 раза в сутки их эффективность несколько выше, чем при использовании 2 раза в сутки (уровень доказательности А).
При недостаточном контроле БА добавление к ИГКС лекарственного средства другого класса предпочтительнее, чем увеличение дозы ИГКС (уровень доказательности А). Наиболее эффективной признана
комбинация ИГКС с длительнодействующими в2-агонистами (сальметеролом или формотеролом).
Больные с очень тяжелым течением БА, которым требуется постоянный прием системных ГКС, должны наряду с ними получать ИГКС (уровень доказательности А).
В ряде руководств содержится рекомендация удваивать дозы ИГКС в случае обострения БА, но эта рекомендация не опирается на какие-либо доказательства. Напротив, рекомендация назначать системные ГКС при обострении БА относится к уровню доказательности А.
Безопасность ИГКС
Проблема изучения безопасности ИГКС является особенно актуальной, учитывая число больных, страдающих БА и вынужденных принимать ИГКС годами.
Системные НЭ у ИГКС различны и зависят от их дозы, фармакокинетических параметров и типа ингалятора. Потенциальные системные НЭ включают:
Угнетение гипоталамо-гипофизарно-надпочечниковой системы (ГГНС);
Снижение скорости линейного роста у детей;
Влияние на костный метаболизм;
Воздействие на липидный обмен;
Развитие катаракты и глаукомы. Наиболее частым предметом дискуссий
остается влияние на ГГНС и скорость линейного роста у детей.
Влияние на ГГНС
К самым чувствительным тестам для оценки функции ГГНС относятся: монито-рирование сывороточного уровня кортизола в течение суток; измерение кортизола мочи, собранной за ночь или за сутки; тест со стимуляцией адренокортикотропным гормоном (АКТГ).
Влияние различных ИГКС на ГГНС было предметом многих исследований. Их результаты нередко были противоречивыми.
Клиническая фармакология
Так, у взрослых добровольцев отмечено, что БДП обладает большим, чем БУД, действием на ГГНС, оцененным по суточной экскреции кортизола с мочой. В другом исследовании БДП, БУД, ТА и ФП в дозе 2000 мкг/сут вызывали статистически достоверную супрессию плазменного кортизола, причем в наибольшей степени - ФП. В третьем испытании при сравнении одинаковых доз ФП и БДП (1500 мкг/сут), применявшихся в течение 1 года для лечения среднетяжелой и тяжелой БА, не было выявлено различий между группами по состоянию ГГНС (уровню кортизола плазмы и экскреции кортизола с мочой).
Таким образом, способность угнетать ГГНС была показана для всех ИГКС (особенно в высоких дозах), и был сделан вывод о важности использования минимальной дозы ИГКС, необходимой для сохранения контроля над симптомами БА.
Влияние на скорость линейного роста у детей
В исследовании START скорость линейного роста у детей в возрасте 5-15 лет при лечении будесонидом была достоверно меньше, чем при применении плацебо: разница между группами составила 0,43 см в год. Следует отметить, что задержка роста существенно не отличалась между детьми, получавшими будесонид в дозах 200 или 400 мкг/сут. Задержка роста была более выраженной в течение первого года лечения, а затем уменьшалась. Сходные данные были получены и в других длительных исследованиях ИГКС у детей с БА.
Местные НЭ
Местные НЭ ИГКС включают кандидоз полости рта и ротоглотки, дисфонию, кашель, возникающий вследствие раздражения верхних дыхательных путей, парадоксальный бронхоспазм.
При приеме низких доз ИГКС частота развития местных НЭ невелика. Так, кан-дидоз полости рта встречается у 5% паци-
ентов, использующих низкие дозы ИГКС, а при использовании высоких доз его частота может достигать 34%. Дисфония отмечается у 5-50% больных, применяющих ИГКС, и также ассоциирована с высокими дозами.
В некоторых случаях возможно развитие рефлекторного кашля или даже парадоксального бронхоспазма в ответ на ингаляцию ГКС. В клинической практике прием бронходилататоров часто маскирует брон-хоконстрикцию такого рода. При использовании фреонсодержащих ДАИ эти НЭ могут быть связаны с низкой температурой (эффект холодного фреона) и большой скоростью струи аэрозоля на выходе из баллончика, а также с гиперреактивностью дыхательных путей на воздействие лекарственного средства или дополнительных компонентов аэрозоля. Для бесфреоновых ДАИ (например, Беклазон Эко) характерна меньшая скорость и более высокая температура аэрозоля, что снижает вероятность рефлекторного кашля и бронхоспазма.
Для предотвращения развития местных НЭ больные, регулярно принимающие ИГКС, должны после ингаляций полоскать рот водой и пользоваться спейсером (уровень доказательности А). При использовании ДАИ со спейсером отпадает необходимость в координации вдоха и нажатия на баллончик. На стенках спейсера оседают крупные частицы лекарства, благодаря чему уменьшается его депозиция на слизистой оболочке рта и глотки и, как следствие этого, минимизируется системная абсорбция ИГКС. Эффективность комбинации ДАИ со спейсером сопоставима с таковой при использовании небулайзеров.
Влияние средств доставки ИГКС на эффективность терапии БА
Основное преимущество ингаляционного пути доставки ГКС непосредственно в дыхательные пути - более эффективное создание высоких концентраций препарата в дыхательных путях и минимизация сис-
темных НЭ. Эффективность ингаляционной терапии БА напрямую зависит от депозиции препарата в нижних дыхательных путях. Легочная депозиция препаратов при использовании различных ингаляционных устройств колеблется в пределах от 4 до 60% от отмеренной дозы.
Среди всех ингаляционных устройств наименее эффективны обычные ДАИ. Это связано со сложностями проведения ингаляции и прежде всего с синхронизацией вдоха и нажатия на баллончик. Только 20-40% больных могут воспроизвести правильную технику ингаляции при использовании обычных ДАИ. Особенно остро этот вопрос стоит у пожилых людей, детей, а также при тяжелых формах БА.
Решить проблемы с техникой ингаляции позволяет использование спейсера или других типов ингаляторов, которые не требуют от пациента точной координации движений во время ингаляции. К таким устройствам относятся ДПИ (турбухалер, мультидиск и др.) и ДАИ, активируемые вдохом (Беклазон Эко Легкое дыхание).
Современные мультидозовые порошковые ингаляторы (турбухалер, мультидиск) позволяют повысить легочную депозицию препаратов приблизительно в 2 раза по сравнению с ДАИ. Однако следует учитывать, что ряд больных по субъективным или объективным причинам не могут пользоваться ДПИ, к тому же их распространение ограничивает высокая стоимость.
ДАИ, активируемые вдохом, представлены в России ингаляционным устройством под названием Легкое дыхание. В виде такого ингалятора выпускается ИГКС бекло-метазона дипропионат (Беклазон Эко Легкое дыхание). Этот препарат не содержит фреона, а новый пропеллент гидрофторал-кан при распылении создает ультрадис-персный аэрозоль БДП. Более мелкие частицы аэрозоля лучше проникают в нижние
дыхательные пути - легочная депозиция Беклазона Эко в 2 раза выше, чем у других препаратов БДП. Это отражается в подходе к дозированию Беклазона Эко: при переходе на этот препарат с других препаратов БДП или будесонида доза уменьшается в 2 раза, а при переходе с флутиказона пропионата - остается такой же.
ДАИ Легкое дыхание исключает сложности с ингаляцией: при открывании колпачка ингалятора взводится пружина, автоматически высвобождающая дозу лекарства в момент вдоха. Нет необходимости нажимать на ингалятор и правильно вдыхать, так как ингалятор “подстраивается” под вдох (если мундштук не обхвачен губами и не начат вдох, то высвобождения препарата не происходит). Также благодаря новому пропелленту отсутствует необходимость встряхивать баллончик перед ингаляцией.
Детям особенно трудно координировать вдох с нажатием на баллончик. Поэтому Беклазон Эко Легкое дыхание может быть использован и в педиатрической практике.
Немаловажная деталь: Беклазон Эко Легкое дыхание комплектуется оптимайзе-ром - компактным спейсером, что оказывает дополнительное профилактическое действие в отношении НЭ и улучшает качество лечения.
Глобальная стратегия лечения и профилактики бронхиальной астмы. Пересмотр 2002 г. / Пер. с англ. под ред. Чучалина А.Г. М., 2002. Емельянов А.В., Шевелев С.Э., Амосов В.И. и др. Терапевтические возможности ингаляционных глюкокортикоидов при бронхиальной астме // Тер. архив. 1999. № 8. С. 37-40. Цой А.Н. Параметры фармакокинетики современных ингаляционных глюкокортикостероидов // Пульмонология. 1999. № 2. С. 73-79.
Чучалин А.Г Бронхиальная астма. М., 1997. Т. 2. С. 213-269.


