29.05.2019
Формы и фазы воспаления. Воспаление: общая характеристика, патоморфология альтеративного и экссудативного воспаления.
Общие сведения
Воспаление - комплексная местная сосудисто-мезенхимальная реакция на повреждение ткани, вызванное действием различного рода агентов. Эта реакция направлена на уничтожение агента, вызвавшего повреждение, и на восстановление поврежденной ткани. Воспаление - реакция, выработанная в ходе филогенеза, имеет защитно-приспособительный характер и несет в себе элементы не только патологии, но и физиологии. Такое двойственное значение для организма воспаления - своеобразная его особенность.
Еще в конце XIX столетия И.И. Мечников считал, что воспаление - это приспособительная и выработанная в ходе эволюции реакция организма и одним из важнейших ее проявлений служит фагоцитоз микрофагами и макрофагами патогенных агентов и обеспечение таким образом выздоровления организма. Но репаративная функция воспаления была для И.И. Мечникова сокрыта. Подчеркивая защитный характер воспаления, он в то же время полагал, что целительная сила природы, которую и представляет собой воспалительная реакция, не есть еще приспособление, достигшее совершенства. По мнению И.И. Мечникова, доказательством этого являются частые болезни, сопровождающиеся воспалением, и случаи смерти от них.
Этиология воспаления
Вызывающие воспаление факторы могут быть биологическими, физическими (в том числе травматическими), химическими; по происхождению они эндогенные или экзогенные.
К физическим факторам, вызывающим воспаление, относят лучевую и электрическую энергию, высокие и низкие температуры, различного рода травмы.
Химическими факторами воспаления могут быть различные химические вещества, токсины и яды.
Развитие воспаления определяется не только воздействием того или иного этиологического фактора, но и особенностью реактивности организма.
Морфология и патогенез воспаления
Воспаление может выражаться образованием микроскопического очага или обширного участка, иметь не только очаговый, но и диффузный характер. Иногда воспаление возникает в системе тканей, тогда говорят о системных воспалительных поражениях (ревматические болезни при системном воспалительном поражении соединительной ткани, системные васкулиты и др.). Иногда провести грань между локализованным и системным воспалительным процессом бывает трудно.
Воспаление развивается на территории гистиона и складывается из следующих последовательно развивающихся фаз: 1) альтерация; 2) экссудация; 3) пролиферация гематогенных и гистиогенных клеток и, реже, паренхиматозных клеток (эпителия). Взаимосвязь этих фаз показана на схеме IX.
Альтерация - повреждение ткани, является инициальной фазой воспаления и проявляется различного вида дистрофией и некрозом. В эту фазу воспаления происходит выброс биологически активных веществ - медиаторов воспаления. Это - пусковой механизм воспаления, определяющий кинетику воспалительной реакции.
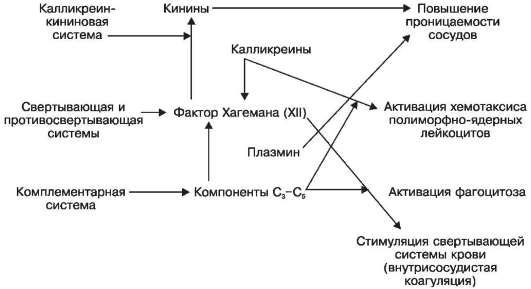
Медиаторы воспаления могут быть плазменного (гуморального) и клеточного (тканевого) происхождения. Медиаторы плазменного происхождения - это представители калликреин-кининовой (кинины, калликреины), свертывающей и противосвертывающеи (XII фактор свертывания крови, или фактор Хагемана, плазмин) и комплементарной (компоненты С 3 -С 5) систем. Медиаторы этих систем повышают проницаемость микрососудов, активируют хемотаксис полиморфно-ядерных лейкоцитов, фагоцитоз и внутрисосудистую коагуляцию (схема X).
Медиаторы клеточного происхождения связаны с эффекторными клетками - лаброцитами (тканевыми базофилами) и базофильными лейкоцитами, которые выбрасывают гистамин, серотонин, медленно реагирующую субстанцию анафилаксии и др.; тромбоцитами, продуцирующими, помимо гистамина, серотонина и простагландинов, также лизосомные ферменты; полиморфно-ядерными лейкоцитами, богатыми лейкокина-
Схема IX. Фазы воспаления
Схема X. Действие медиаторов воспаления плазменного (гуморального) происхождения
 ми,
лизосомными ферментами, катионными белками и нейтральными протеазами.
Эффекторными клетками, продуцирующими медиаторы воспаления, являются и
клетки иммунных реакций - макрофаги, выбрасывающие свои монокины
(интерлейкин I), и лимфоциты, продуцирующие лимфокины (интерлейкин II). С
медиаторами клеточного происхождения связано не только повышение проницаемости микрососудов
и фагоцитоз;
они обладают бактерицидным действием,
вызывают вторичную альтерацию
(гистолиз), включают иммунные механизмы
в воспалительную реакцию, регулируют пролиферацию
и дифференцировку клеток
на
поле воспаления, направленные на репарацию, возмещение или замещение
очага повреждения соединительной тканью (схема XI). Дирижером клеточных
взаимодействий на поле воспаления является макрофаг.
ми,
лизосомными ферментами, катионными белками и нейтральными протеазами.
Эффекторными клетками, продуцирующими медиаторы воспаления, являются и
клетки иммунных реакций - макрофаги, выбрасывающие свои монокины
(интерлейкин I), и лимфоциты, продуцирующие лимфокины (интерлейкин II). С
медиаторами клеточного происхождения связано не только повышение проницаемости микрососудов
и фагоцитоз;
они обладают бактерицидным действием,
вызывают вторичную альтерацию
(гистолиз), включают иммунные механизмы
в воспалительную реакцию, регулируют пролиферацию
и дифференцировку клеток
на
поле воспаления, направленные на репарацию, возмещение или замещение
очага повреждения соединительной тканью (схема XI). Дирижером клеточных
взаимодействий на поле воспаления является макрофаг.
Медиаторы плазменного и клеточного происхождения взаимосвязаны и работают по принципу аутокаталитической реакции с обратной связью и взаимной поддержкой (см. схемы X и XI). Действие медиаторов опосредовано рецепторами на поверхности эффекторных клеток. Из этого следует, что смена одних медиаторов другими во времени обусловливает смену клеточных форм на поле воспаления - от полиморфно-ядерного лейкоцита для фагоцитоза до фибробласта, активируемого монокинами макрофага, для репарации.
Экссудация - фаза, быстро следующая за альтерацией и выбросом медиаторов. Она складывается из ряда стадий: реакция микроциркуляторного русла с нарушениями реологических свойств крови; повышение сосудистой проницаемости на уровне микроциркуляторного русла; экссудация составных частей плазмы крови; эмиграция клеток крови; фагоцитоз; образование экссудата и воспалительного клеточного инфильтрата.
Схема XI. Действие медиаторов воспаления клеточного (тканевого) происхожде-
ния
 Реакция микроциркуляторного русла с нарушениями реологических свойств крови
-
один из ярких морфологических признаков воспаления. Изменения
микрососудов начинаются с рефлекторного спазма, уменьшения просвета
артериол и прекапилляров, которое быстро сменяется расширением всей
сосудистой сети зоны воспаления и прежде всего посткапилляров и венул. Воспалительная гиперемия
обусловливает повышение температуры (calor)
и покраснение (rubor)
воспаленного
участка. При начальном спазме ток крови в артериолах становится
ускоренным, а затем замедленным. В лимфатических сосудах, как и в
кровеносных, вначале происходит ускорение лимфотока, а затем его
замедление. Лимфатические сосуды переполняются лимфой и лейкоцитами.
Реакция микроциркуляторного русла с нарушениями реологических свойств крови
-
один из ярких морфологических признаков воспаления. Изменения
микрососудов начинаются с рефлекторного спазма, уменьшения просвета
артериол и прекапилляров, которое быстро сменяется расширением всей
сосудистой сети зоны воспаления и прежде всего посткапилляров и венул. Воспалительная гиперемия
обусловливает повышение температуры (calor)
и покраснение (rubor)
воспаленного
участка. При начальном спазме ток крови в артериолах становится
ускоренным, а затем замедленным. В лимфатических сосудах, как и в
кровеносных, вначале происходит ускорение лимфотока, а затем его
замедление. Лимфатические сосуды переполняются лимфой и лейкоцитами.
В бессосудистых тканях (роговица, клапаны сердца) в начале воспаления преобладают явления альтерации, а затем происходит врастание сосудов из соседних областей (это происходит очень быстро) и включение их в воспалительную реакцию.
Изменения реологических свойств крови состоят в том, что в расширенных венулах и посткапиллярах при замедленном токе крови нарушается распределение в кровяном потоке лейкоцитов и эритроцитов. Полиморфно-ядерные лейкоциты (нейтрофилы) выходят из осевого тока, собираются в краевой зоне и располагаются вдоль стенки сосуда. Крае-
вое расположение нейтрофилов сменяется их краевым стоянием, которое предшествует эмиграции за пределы сосуда.
Изменения гемодинамики и сосудистого тонуса в очаге воспаления приводят к стазу в посткапиллярах и венулах, который сменяется тромбозом. Те же изменения возникают и в лимфатических сосудах. Таким образом, при продолжающемся притоке крови в очаг воспаления отток ее, а также лимфы нарушается. Блокада отводящих кровеносных и лимфатических сосудов позволяет очагу воспаления выполнять роль барьера, предупреждающего генерализацию процесса.
Повышение сосудистой проницаемости на уровне микроциркуляторного русла является одним из существенных признаков воспаления. Вся гамма тканевых изменений, своеобразие форм воспаления в значительной мере определяются состоянием сосудистой проницаемости, глубиной ее повреждения. Большая роль в осуществлении повышенной проницаемости сосудов микроциркуляторного русла принадлежит поврежденным ультраструктурам клеток, что приводит к усилению микропиноцитоза. С повышенной сосудистой проницаемостью связаны экссудация в ткани и полости жидких частей плазмы, эмиграция клеток крови, образование экссудата (воспалительного выпота) и воспалительного клеточного инфильтрата.
Экссудация составных частей плазмы крови рассматривается как проявление сосудистой реакции, развивающейся в пределах микроциркуляторного русла. Она выражается в выходе за пределы сосуда жидких составных частей крови: воды, белков, электролитов.
Эмиграция клеток крови, т.е. выход их из тока крови через стенку сосудов, осуществляется с помощью хемотаксических медиаторов (см. схему X). Как уже было сказано, эмиграции предшествует краевое стояние нейтрофилов. Они прилипают к стенке сосуда (главным образом в посткапиллярах и венулах), затем образуют отростки (псевдоподии), которые проникают между эндотелиальными клетками - межэндотелиальная эмиграция (рис. 63). Базальную мембрану нейтрофилы преодолевают, вероятнее всего, на основе феномена тиксотропии (тиксотропия - изометрическое обратимое уменьшение вязкости коллоидов), т.е. перехода геля мембраны в золь при прикосновении клетки к мембране. В околососудистой ткани нейтрофилы продолжают свое движение с помощью псевдоподий. Процесс эмиграции лейкоцитов носит название лейкодиапедеза, а эритроцитов - эритродиапедеза.
Фагоцитоз (от греч. phagos - пожирать и kytos - вместилище) - поглощение и переваривание клетками (фагоцитами) различных тел как живой (бактерии), так и неживой (инородные тела) природы. Фагоцитами могут быть разнообразные клетки, но при воспалении наибольшее значение приобретают нейтрофилы и макрофаги.
Фагоцитоз обеспечивается рядом биохимических реакций. При фагоцитозе уменьшается содержание гликогена в цитоплазме фагоцита, что связано с усиленным анаэробным гликогенолизом, необходимым для выработки энергии для фагоцитоза; вещества, блокирующие гликогенолиз, подавляют и фагоцитоз.
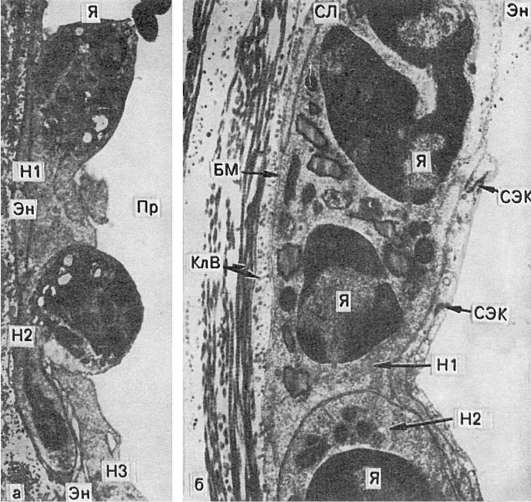 Рис. 63.
Эмиграция лейкоцитов через стенку сосуда при воспалении:
Рис. 63.
Эмиграция лейкоцитов через стенку сосуда при воспалении:
а - один из нейтрофилов (H1) тесно прилежит к эндотелию (Эн), другой (Н2) имеет хорошо очерченное ядро (Я) и пронизывает эндотелий (Эн). Большая половина этого лейкоцита расположена в подэндотелиальном слое. На эндотелии в этом участке видны псевдоподии третьего лейкоцита (Н3); Пр - просвет сосуда. х9000; б - нейтрофилы (СЛ) с хорошо контурированными ядрами (Я) расположены между эндотелием и базальной мембраной (БМ); стыки эндотелиальных клеток (СЭК) и коллагеновые волокна (КлВ) за базальной мембраной. х20 000 (по Флори и Грант)
Фагоцитирующий объект (бактерия), окруженный инвагинированной цитомембраной (фагоцитоз - потеря цитомембраны фагоцита), образует фагосому. При слиянии ее с лизосомой возникает фаголизосома (вторичная лизосома), в которой с помощью гидролитических ферментов осуществляется внутриклеточное переваривание - завершенный фагоцитоз (рис. 64). В завершенном фагоцитозе большую роль играют антибактериальные катионные белки лизосом нейтрофилов; они убивают микробы, которые затем перевариваются. В тех случаях, когда микроорганизмы не перевариваются фагоцитами, чаще макрофагами и размножаются в их цитоплазме, говорят о незавершенном фагоцитозе, или эндоцитобиозе. Его
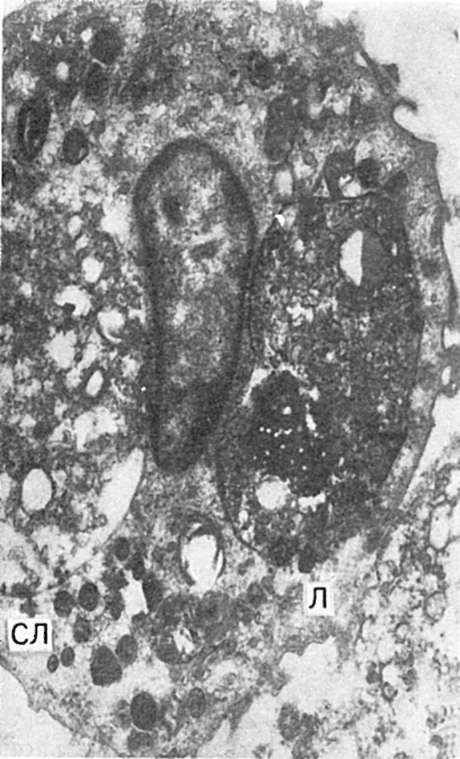 Рис. 64.
Фагоцитоз. Макрофаг с фагоцитированными обломками лейкоцита (СЛ) и липидными включениями (Л). Электронограмма. х
20 000.
Рис. 64.
Фагоцитоз. Макрофаг с фагоцитированными обломками лейкоцита (СЛ) и липидными включениями (Л). Электронограмма. х
20 000.
объясняют многими причинами, в частности тем, что лизосомы макрофагов могут содержать недостаточное количество антибактериальных катионных белков или вообще лишены их. Таким образом, фагоцитоз не всегда является защитной реакцией организма и иногда создает предпосылки для диссеминации микробов.
Образование экссудата и воспалительного клеточного инфильтрата завершает описанные выше процессы экссудации. Выпот жидких частей крови, эмиграция лейкоцитов, диапедез эритроцитов ведут к появлению в пораженных тканях или полостях тела воспалительной жидкости - экссудата. Накопление экссудата в ткани ведет к увеличению ее объема (tumor), сдавлению нервных окончаний и появлению боли (dolor), возникновение которой при воспалении связывают и с воздействием медиаторов (брадикинин), к нарушению функции ткани или органа (functio laesa).
Обычно экссудат содержит более 2% белков. В зависимости от степени проницаемости стенки сосуда, в ткань могут проникать разные белки. При небольшом повышении проницаемости сосудистого барьера через него проникают в основном альбумины и глобулины, а при высокой степени проницаемости наряду с ними выходят и крупномолекулярные белки, в частности фибриноген. В одних случаях в экссудате преобладают нейтрофилы, в других - лимфоциты, моноциты и гистиоциты, в третьих - эритроциты.
При скоплении в тканях клеток экссудата, а не жидкой его части говорят о воспалительном клеточном инфильтрате, в котором могут преобладать как гематогенные, так и гистиогенные элементы.
Пролиферация (размножение) клеток является завершающей фазой воспаления, направленной на восстановление поврежденной ткани. Возрастает число мезенхимальных камбиальных клеток, В- и Т-лимфоцитов, моноцитов. При размножении клеток в очаге воспаления наблюдаются клеточные дифференцировки и трансформации (схема XII): камбиальные мезенхимальные клетки дифференцируются в фибробласты; В-лимфоциты
Схема XII. Дифференцировка и трансформация клеток при воспалении
 дают начало образованию плазматических клеток.
Т-лимфоциты, видимо, не трансформируются в другие формы. Моноциты дают начало гистиоцитам
и макрофагам.
Макрофаги могут быть источником образования эпителиоидных
и гигантских клеток
(клетки инородных тел и Пирогова- Лангханса).
дают начало образованию плазматических клеток.
Т-лимфоциты, видимо, не трансформируются в другие формы. Моноциты дают начало гистиоцитам
и макрофагам.
Макрофаги могут быть источником образования эпителиоидных
и гигантских клеток
(клетки инородных тел и Пирогова- Лангханса).
На различных этапах пролиферации фибробластов образуются продукты их деятельности - белок коллаген и гликозаминогликаны, появляются аргирофильные и коллагеновые волокна, межклеточное вещество соединительной ткани.
В процессе пролиферации при воспалении участвует и эпителий (см. схему XII), что особенно выражено в коже и слизистых оболочках (желудок, кишечник). При этом пролиферирующий эпителий может образовывать полипозные разрастания. Пролиферация клеток на поле воспаления служит репарации. При этом дифференцировка пролиферирующих эпителиальных структур возможна лишь при созревании и дифференцировке соединительной ткани (Гаршин В.Н., 1939).
Воспаление со всеми его компонентами появляется только на поздних этапах внутриутробного развития. У плода, новорожденного и ребенка воспаление имеет ряд особенностей. Первой особенностью воспаления является преобладание альтеративного и продуктивного его компонентов, так как они филогенетически более древние. Второй особенностью воспаления, связанной с возрастом, является склонность местного процесса к распространению и генерализации в связи с анатомической и функциональной незрелостью органов иммуногенеза и барьерных тканей.
Регуляция воспаления осуществляется с помощью гормональных, нервных и иммунных факторов. Установлено, что одни гормоны, такие как соматотропный гормон (СТГ) гипофиза, дезоксикортикостерон, альдостерон, усиливают воспалительную реакцию (провоспалительные гормоны), другие - глюкокортикоиды и адренокортикотропный гормон (АКЛТ) гипофиза, напротив, уменьшают ее (противовоспалительные гормоны). Холинергические вещества, стимулируя выброс медиаторов воспаления, дей-
ствуют подобно провоспалительным гормонам, а адренергические, угнетая медиаторную активность, ведут себя подобно противовоспалительным гормонам. На выраженность воспалительной реакции, темпы ее развития и характер влияет состояние иммунитета. Особенно бурно воспаление протекает в условиях антигенной стимуляции (сенсибилизация); в таких случаях говорят об иммунном, или аллергическом, воспалении (см. Иммунопатологические процессы).
Исход воспаления различен в зависимости от его этиологии и характера течения, состояния организма и структуры органа, в котором оно развивается. Продукты тканевого распада подвергаются ферментативному расщеплению и фагоцитарной резорбции, происходит рассасывание продуктов распада. Благодаря клеточной пролиферации очаг воспаления постепенно замещается клетками соединительной ткани. Если очаг воспаления был небольшим, может наступить полное восстановление предшествующей ткани. При значительном дефекте ткани на месте очага образуется рубец.
Терминология и классификация воспаления
В большинстве случаев наименование воспаления той или иной ткани (органа) принято составлять, прибавляя к латинскому и греческому названию органа или ткани окончание -itis, а к русскому - -ит. Так, воспаление плевры обозначают как pleuritis - плеврит, воспаление почки - nephritis - нефрит, воспаление десен - gingivitis - гингивит и т.д. Воспаление некоторых органов имеет особые названия. Так, воспаление зева называют ангиной (от греч. ancho - душу, сдавливаю), воспаление легких - пневмонией, воспаление ряда полостей со скоплением в них гноя - эмпиемой (например, эмпиема плевры), гнойное воспаление волосяного фолликула с прилежащей сальной железой и тканями - фурункулом (от лат. furiare - приводить в ярость) и т.д.
Классификация. Учитываются характер течения процесса и морфологические формы в зависимости от преобладания экссудативной или пролиферативной фазы воспаления. По характеру течения выделяют острое, подострое и хроническое воспаление, по преобладанию экссудативной или пролиферативной фазы воспалительной реакции - экссудативное и .
До недавнего времени среди морфологических форм воспаления выделяли альтеративное воспаление, при котором преобладает альтерация (некротическое воспаление), а экссудация и пролиферация представлены крайне слабо или вообще не выражены. В настоящее время существование этой формы воспаления отрицается большинством патологов на том основании, что при так называемом альтеративном воспалении по существу отсутствует сосудисто-мезенхимальная реакция (экссудация и пролиферация), которая и составляет сущность воспалительной реакции. Таким образом, речь в данном случае идет не о воспалении, а о некрозе. Концепция альтеративного воспаления была создана Р. Вирховым, который исходил из своей «нутритивной теории» воспаления (она оказалась ошибочной), поэтому он называл альтеративное воспаление паренхиматозным.
Морфологические формы воспаления
Экссудативное воспаление
Экссудативное воспаление характеризуется преобладанием экссудации и образованием в тканях и полостях тела экссудата. В зависимости от характера экссудата и преобладающей локализации воспаления выделяют следующие виды экссудативного воспаления: 1) серозное; 2) фибринозное; 3) гнойное; 4) гнилостное; 5) геморрагическое; 6) катаральное; 7) смешанное.
Серозное воспаление. Оно характеризуется образованием экссудата, содержащего до 2% белков и небольшое количество клеточных элементов. Течение серозного воспаления, как правило, острое. Возникает чаще в серозных полостях, слизистых и мозговых оболочках, реже - во внутренних органах, коже.
Морфологическая картина. В серозных полостях накапливается серозный экссудат - мутноватая жидкость, бедная клеточными элементами, среди которых преобладают спущенные клетки мезотелия и единичные нейтрофилы; оболочки становятся полнокровными. Та же картина возникает и при серозном менингите. При воспалении слизистых оболочек, которые также становятся полнокровными, к экссудату примешиваются слизь и спущенные клетки эпителия, возникает серозный катар слизистой оболочки (см. ниже описание катарального воспаления). В печени жидкость накапливается в перисинусоидальных пространствах (рис. 65), в миокарде - между мышечными волокнами, в почках - в просвете клубочковой капсулы. Серозное воспаление кожи, например при ожоге, выражается образованием пузырей, возникающих в толще эпидермиса, заполненных мутноватым выпотом. Иногда экссудат накапливается под эпидермисом и отслаивает его от подлежащей ткани с образованием крупных пузырей.
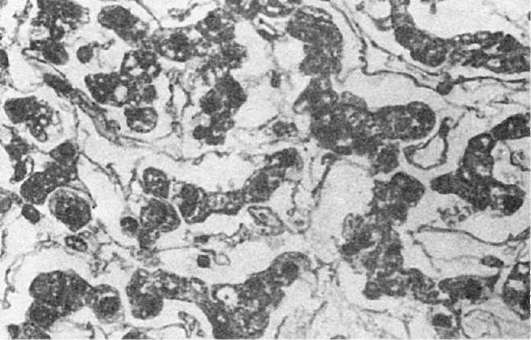 Рис. 65.
Серозный гепатит
Рис. 65.
Серозный гепатит
Причиной серозного воспаления являются различные инфекционные агенты (микобактерии туберкулеза, диплококк Френкеля, менингококк, шигелла), воздействие термических и химических факторов, аутоинтоксикация (например, при тиреотоксикозе, уремии).
Исход серозного воспаления обычно благоприятный. Даже значительное количество экссудата может рассасываться. Во внутренних органах (печень, сердце, почки) в исходе серозного воспаления при хроническом его течении иногда развивается склероз.
Значение определяется степенью функциональных нарушений. В полости сердечной сорочки выпот затрудняет работу сердца, в плевральной полости приводит к коллапсу (сдавлению) легкого.
Фибринозное воспаление. Оно характеризуется образованием экссудата, богатого фибриногеном, который в пораженной (некротизированной) ткани превращается в фибрин. Этому процессу способствует высвобождение в зоне некроза большого количества тромбопластина. Локализуется фибринозное воспаление в слизистых и серозных оболочках, реже - в толще органа.
Морфологическая картина. На поверхности слизистой или серозной оболочки появляется белесовато-серая пленка («пленчатое» воспаление). В зависимости от глубины некроза ткани, вида эпителия слизистой оболочки пленка может быть связана с подлежащими тканями рыхло и поэтому легко отделяется либо прочно и поэтому отделяется с трудом. В первом случае говорят о крупозном, а во втором - о дифтеритическом варианте фибринозного воспаления.
Крупозное воспаление (от шотл. croup - пленка) возникает при неглубоком некрозе ткани и пропитывании некротических масс фибрином (рис. 66). Пленка, рыхло связанная с подлежащей тканью, делает слизистую или серозную оболочку тусклой. Иногда кажется, что оболочка как бы посыпана опилками. Слизистая оболочка утолщается, набухает, если пленка отделяется, возникает поверхностный дефект. Серозная оболочка становится шероховатой, как бы покрытой волосяным покровом - нитями фибрина. При фибринозном перикардите в таких случаях говорят о «волосатом сердце». Среди внутренних органов крупозное воспаление развивается в легком - крупозная пневмония (см. Пневмонии).
Дифтеритическое воспаление (от греч. diphtera - кожистая пленка) развивается при глубоком некрозе ткани и пропитывании некротических масс фибрином (рис. 67). Оно развивается на слизистых оболочках. Фибринозная пленка плотно спаяна с подлежащей тканью, при отторжении ее возникает глубокий дефект.
Вариант фибринозного воспаления (крупозное или дифтеритическое) зависит, как уже говорилось, не только от глубины некроза ткани, но и от вида эпителия, выстилающего слизистые оболочки. На слизистых оболочках, покрытых плоским эпителием (полость рта, зев, миндалины, надгортанник, пищевод, истинные голосовые связки, шейка матки), пленки обычно плотно связаны с эпителием, хотя некроз и выпадение фибрина ограничиваются иногда только эпителиальным покровом. Это объясня-
 ется
тем, что клетки плоского эпителия тесно связаны между собой и с
подлежащей соединительной тканью и поэтому «крепко держат» пленку. В
слизистых оболочках, покрытых призматическим эпителием (верхние
дыхательные пути, желудочно-кишечный тракт и др.), связь эпителия с
подлежащей тканью рыхлая, поэтому образующиеся пленки легко отделяются
вместе с эпителием даже при глубоком выпадении фибрина. Клиническое
значение фибринозного воспаления, например, в зеве и трахее оказывается
неравнозначным даже при одной и той же причине его возникновения
(дифтеритическая ангина и крупозный трахеит при дифтерии).
ется
тем, что клетки плоского эпителия тесно связаны между собой и с
подлежащей соединительной тканью и поэтому «крепко держат» пленку. В
слизистых оболочках, покрытых призматическим эпителием (верхние
дыхательные пути, желудочно-кишечный тракт и др.), связь эпителия с
подлежащей тканью рыхлая, поэтому образующиеся пленки легко отделяются
вместе с эпителием даже при глубоком выпадении фибрина. Клиническое
значение фибринозного воспаления, например, в зеве и трахее оказывается
неравнозначным даже при одной и той же причине его возникновения
(дифтеритическая ангина и крупозный трахеит при дифтерии).
Причины фибринозного воспаления разные. Оно может вызываться диплококками Френкеля, стрептококками и стафилококками, возбудителями дифтерии и дизентерии, микобактерией туберкулеза, вирусами гриппа. Кроме инфекционных агентов, фибринозное воспаление может быть вызвано токсинами и ядами эндогенного (например, при уремии) или экзогенного (при отравлении сулемой) происхождения.
Течение фибринозного воспаления, как правило, острое. Иногда (например, при туберкулезе серозных оболочек) оно имеет хронический характер.
Исход фибринозного воспаления слизистых и серозных оболочек неодинаков. На слизистых оболочках после отторжения пленок остаются разной глубины дефекты - язвы; при крупозном воспалении они поверхностные, при дифтеритическом - глубокие и оставляют после себя рубцовые изменения. На серозных оболочках возможно рассасывание фибринозного экссудата. Однако нередко массы фибрина подвергаются организации, что приводит к образованию спаек между серозными листками плевры, брюшины, сердечной сорочки. В исходе фибринозного воспаления может произойти и полное зарастание серозной полости соединительной тканью - ее облитерация.
Значение фибринозного воспаления очень велико, так как оно составляет морфологическую основу многих болезней (дифтерия, дизентерия),
наблюдается при интоксикациях (уремия). При образовании пленок в гортани, трахее возникает опасность асфиксии; при отторжении пленок в кишечнике возможно кровотечение из образующихся язв. После перенесенного фибринозного воспаления могут оставаться длительно не заживающие, рубцующиеся язвы.
Гнойное воспаление. Для него характерно преобладание в экссудате нейтрофилов. Распадающиеся нейтрофилы, которых называют гнойными тельцами, вместе с жидкой частью экссудата образуют гной. В нем встречаются также лимфоциты, макрофаги, погибшие клетки ткани, микробы. Гной представляет собой мутную густую жидкость, имеющую желтозеленый цвет. Характерной особенностью гнойного воспаления является гистолиз, обусловленный воздействием на ткани протеолитических ферментов нейтрофилов. Гнойное воспаление встречается в любом органе, любой ткани.
Морфологическая картина. Гнойное воспаление в зависимости от распространенности его может быть представлено абсцессом или флегмоной.
Абсцесс (гнойник) - очаговое гнойное воспаление, характеризующееся образованием полости, заполненной гноем (рис. 68). Гнойник со временем отграничивается валом грануляционной ткани, богатой капиллярами, через стенки которых происходит усиленная эмиграция лейкоцитов. Образуется как бы оболочка абсцесса. Снаружи она состоит из соединительнотканных волокон, которые прилежат к неизмененной ткани, а внутри - из грануляционной ткани и гноя, непрерывно обновляющегося благодаря выделению грануляциями гнойных телец. Оболочку абсцесса, продуцирующую гной, называют пиогенной мембраной.
Флегмона - разлитое гнойное воспаление, при котором гнойный экссудат распространяется диффузно между тканевыми элементами, пропитывая, расслаивая и лизируя ткани. Чаще всего флегмона наблюдается там, где гнойный экссудат может легко пробить себе дорогу, т.е. по межмышечным прослойкам, по ходу сухожилий, фасций, в подкожной клетчатке, вдоль сосудисто-нервных стволов и т.д.
Различают мягкую и твердую флегмону. Мягкая флегмона характеризуется отсутствием видимых очагов некроза ткани, твердая флегмона - наличием таких очагов, которые не подвергаются гнойному расплавлению, вследствие чего ткань становится очень плотной; мертвая ткань отторгается. Флегмо-
 на
жировой клетчатки (целлюлит) отличается безграничным распространением.
Может происходить скопление гноя в полостях тела и в некоторых полых
органах, что называют эмпиемой
(эмпиема плевры, желчного пузыря, червеобразного отростка и т.д.).
на
жировой клетчатки (целлюлит) отличается безграничным распространением.
Может происходить скопление гноя в полостях тела и в некоторых полых
органах, что называют эмпиемой
(эмпиема плевры, желчного пузыря, червеобразного отростка и т.д.).
Причиной гнойного воспаления чаще являются гноеродные микробы (стафилококк, стрептококк, гонококки, менингококки), реже диплококки Френкеля, брюшнотифозные палочки, микобактерия туберкулеза, грибы и др. Возможно асептическое гнойное воспаление при попадании в ткань некоторых химических веществ.
Течение гнойного воспаления может быть острым и хроническим. Острое гнойное воспаление, представленное абсцессом или флегмоной, имеет тенденцию к распространению. Гнойники, расплавляя капсулу органа, могут прорываться в соседние полости. Между гнойником и полостью, куда прорвался гной, возникают свищевые ходы. В этих случаях возможно развитие эмпиемы. Гнойное воспаление при его распространении переходит на соседние органы и ткани (например, при абсцессе легкого возникает плеврит, при абсцессе печени - перитонит). При абсцессе и флегмоне гнойный процесс может получить лимфогенное и гематогенное распространение, что ведет к развитию септикопиемии (см. Сепсис).
Хроническое гнойное воспаление развивается в тех случаях, когда гнойник инкапсулируется. В окружающих тканях при этом развивается склероз. Если гной в таких случаях находит выход, появляются хронические свищевые ходы, или фистулы, которые вскрываются через кожные покровы наружу. Если свищевые ходы не открываются, а процесс продолжает распространяться, гнойники могут возникать на значительном отдалении от первичного очага гнойного воспаления. Такие отдаленные гнойники носят название натечного абсцесса, или натечника. При длительном течении гнойное воспаление распространяется по рыхлой клетчатке и образует обширные затеки гноя, вызывающие резкую интоксикацию и приводящие к истощению организма. При ранениях, осложнившихся нагноением раны, развивается раневое истощение, или гнойно-резорбтивная лихорадка (Давыдовский И.В., 1954).
Исход гнойного воспаления зависит от его распространенности, характера течения, вирулентности микроба и состояния организма. В неблагоприятных случаях может наступить генерализация инфекции, развивается сепсис. Если процесс отграничивается, абсцесс вскрывается спонтанно или хирургически, что приводит к освобождению от гноя. Полость абсцесса заполняется грануляционной тканью, которая созревает, и на месте гнойника образуется рубец. Возможен и другой исход: гной в абсцессе сгущается, превращается в некротический детрит, подвергающийся петрификации. Длительно протекающее гнойное воспаление часто ведет к амилоидозу.
Значение гнойного воспаления определяется прежде всего его способностью разрушать ткани (гистолиз), что делает возможным распространение гнойного процесса контактным, лимфогенным и гематогенным
путем. Гнойное воспаление лежит в основе многих заболеваний, а также их осложнений.
Гнилостное воспаление (гангренозное, ихорозное, от греч. ichor - сукровица). Развивается обычно вследствие попадания в очаг воспаления гнилостных бактерий, вызывающих разложение ткани с образованием дурнопахнущих газов.
Геморрагическое воспаление. Возникает в тех случаях, когда экссудат содержит много эритроцитов. В развитии этого вида воспаления велика роль не только резко повышенной проницаемости микрососудов, но и отрицательного хемотаксиса в отношении нейтрофилов. Возникает геморрагическое воспаление при тяжелых инфекционных заболеваниях - сибирской язве, чуме, гриппе и др. Иногда эритроцитов так много, что экссудат напоминает кровоизлияние (например, при сибиреязвенном менингоэнцефалите). Часто геморрагическое воспаление присоединяется к другим видам экссудативного воспаления.
Исход геморрагического воспаления зависит от вызвавшей его причины.
Катаральное воспаление (от греч. katarrheo - стекаю), или катар. Развивается на слизистых оболочках и характеризуется обильным выделением экссудата на их поверхности (рис. 69). Экссудат может быть серозным, слизистым, гнойным, геморрагическим, причем к нему всегда примешиваются слущенные клетки покровного эпителия. Катаральное воспаление может быть острым и хроническим. Острый катар характерен для ряда инфекций (например, острый катар верхних дыхательных путей при острой респираторной инфекции). При этом характерна смена одного вида катара другим - серозного катара слизистым, а слизистого - гнойным или гнойно-геморрагическим. Хронический катар встречается как при инфекционных (хронический гнойный катаральный бронхит), так и неинфекционных (хронический катаральный гастрит) заболеваниях. Хронический катар сопровождается атрофией (атрофический катар) или гипертрофией (гипертрофический катар) слизистой оболочки.
 Рис. 69.
Катаральный бронхит
Рис. 69.
Катаральный бронхит
Причины катарального воспаления различны. Чаще всего катары имеют инфекционную или инфекционно-аллергическую природу. Они могут развиваться при аутоинтоксикации (уремический катаральный гастрит и колит), в связи с воздействием термических и химических агентов.
Значение катарального воспаления определяется его локализацией, интенсивностью, характером течения. Наибольшее значение приобретают катары слизистых оболочек дыхательных путей, нередко принимающие хронический характер и имеющие тяжелые последствия (эмфизема легких, пневмосклероз). Не меньшее значение имеет и хронический катар желудка, который способствует развитию опухоли.
Смешанное воспаление. В тех случаях, когда к одному виду экссудата присоединяется другой, наблюдается смешанное воспаление. Тогда говорят о серозно-гнойном, серозно-фибринозном, гнойно-геморрагическом или фибринозно-геморрагическом воспалении. Чаще смена вида экссудативного воспаления наблюдается при присоединении новой инфекции, изменении реактивности организма.
Пролиферативное (продуктивное) воспаление
Пролиферативное (продуктивное) воспаление характеризуется преобладанием пролиферации клеточных и тканевых элементов. Альтеративные и экссудативные изменения отступают на второй план. В результате пролиферации клеток образуются очаговые или диффузные клеточные инфильтраты. Они могут быть полиморфно-клеточными, лимфоцитарномоноцитарными, макрофагальными, плазмоклеточными, эпителиоидноклеточными, гигантоклеточными и др.
Продуктивное воспаление встречается в любом органе, любой ткани. Выделяют следующие виды пролиферативного воспаления: 1) межуточное (интерстициальное); 2) гранулематозное; 3) воспаление с образованием полипов и остроконечных кондилом.
Межуточное (интерстициальное) воспаление. Характеризуется образованием клеточного инфильтрата в строме - миокарда (рис. 70), печени, почек, легких. Инфильтрат может быть представлен гистиоцитами, моноцитами, лимфоцитами, плазматическими клетками, лаброцитами, единичными нейтрофилами, эозинофилами. Прогрессирование межуточного воспаления приводит к развитию зрелой волокнистой соединительной ткани - развивается склероз (см. схему XII).
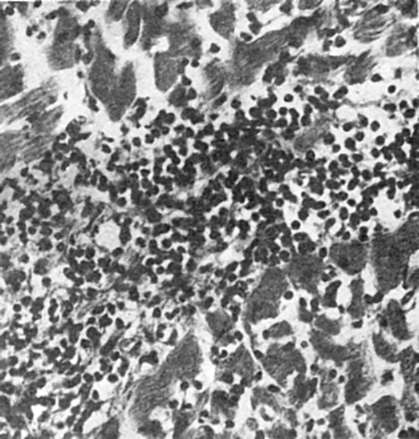 Рис. 70.
Межуточный (интерстициальный) миокардит
Рис. 70.
Межуточный (интерстициальный) миокардит
Если в клеточном инфильтрате много плазматических клеток, то они могут превращаться в гомогенные шаровидные образования, которые называют гиалиповыми шарами, или фуксинофильными тельцами (тельца Русселя). Внешне органы при межуточном воспалении изменяются мало.
Гранулематозное воспаление. Характеризуется образованием гранулем (узелков), возникающих в результате пролиферации и трансформации способных к фагоцитозу клеток.
Морфогенез гранулемы складывается из 4 стадий: 1) накопление в очаге повреждения ткани юных моноцитарных фагоцитов; 2) созревание этих клеток в макрофаги и образование макрофагальной гранулемы; 3) созревание и трансформация моноцитарных фагоцитов и макрофагов в эпителиоидные клетки и образование эпителиоидной клеточной гранулемы; 4) слияние эпителиоидных клеток (или макрофагов) и образование гигантских клеток (клеток инородных тел или клеток Пирогова-Лангханса) и эпителиоидно-клеточной или гигантоклеточной гранулемы. Гигантские клетки характеризуются значительным полиморфизмом: от 2-3-ядерных до гигантских симпластов, содержащих 100 ядер и более. В гигантских клетках инородных тел ядра располагаются в цитоплазме равномерно, в клетках Пирогова-Лангханса - преимущественно по периферии. Диаметр гранулем, как правило, не превышает 1-2 мм; чаще они обнаруживаются лишь под микроскопом. Исходом гранулемы является склероз.
Таким образом, руководствуясь морфологическими признаками, следует различать три вида гранулем: 1) макрофагальная гранулема (простая гранулема, или фагоцитома); 2) эпителиоидно-клеточная гранулема (эпителиоидоцитома); 3) гигантоклеточная гранулема.
В зависимости от уровня метаболизма различают гранулемы с низким и высоким уровнями обмена. Гранулемы с низким уровнем обмена возникают при воздействии инертными веществами (инертные инородные тела) и состоят в основном из гигантских клеток инородных тел. Гранулемы с высоким уровнем обмена появляются при действии токсических раздражителей (микобактерии туберкулеза, лепры и др.) и представлены эпителиоидно-клеточными узелками.
Этиология гранулематоза разнообразна. Различают инфекционные, неинфекционные и неустановленной природы гранулемы. Инфекционные гранулемы находят при сыпном и брюшном тифах, ревматизме, бешенстве, вирусном энцефалите, туляремии, бруцеллезе, туберкулезе, сифилисе, лепре, склероме. Неинфекционные гранулемы встречаются при пылевых болезнях (силикоз, талькоз, асбестоз, биссиноз и др.), медикаментозных воздействиях (гранулематозный гепатит, олеогранулематозная болезнь); они появляются также вокруг инородных тел. К гранулемам неустановленной природы относят гранулемы при саркоидозе, болезнях Крона и Хортона, гранулематоз Вегенера и др. Руководствуясь этиологией, в настоящее время выделяют группу гранулематозных болезней.
Патогенез гранулематоза неоднозначен. Известно, что для развития гранулемы необходимы два условия: наличие веществ, способных стиму-
лировать систему моноцитарных фагоцитов, созревание и трансформацию макрофагов, и стойкость раздражителя по отношению к фагоцитам. Эти условия неоднозначно воспринимаются иммунной системой. В одних случаях гранулема, в эпителиоидных и гигантских клетках которой резко снижена фагоцитарная активность, иначе фагоцитоз, подменяется эндоцитобиозом, становится выражением реакции гиперчувствительности замедленного типа. В этих случаях говорят об иммунной гранулеме, которая имеет обычно морфологию эпителиоидно-клеточной с гигантскими клетками Пирогова-Лангханса. В других случаях, когда фагоцитоз в клетках гранулемы относительно достаточен, говорят о неиммунной гранулеме, которая представлена обычно фагоцитомой, реже - гигантоклеточной гранулемой, состоящей из клеток инородных тел.
Гранулемы делят также на специфические и неспецифические. Специфическими называют те гранулемемы, морфология которых относительно специфична для определенного инфекционного заболевания, возбудитель которого можно найти в клетках гранулемы при гистобактериоскопическом исследовании. К специфическим гранулемам (ранее они были основой так называемого специфического воспаления) относят гранулемы при туберкулезе, сифилисе, лепре и склероме.
Туберкулезная гранулема имеет следующее строение: в центре нее расположен очаг некроза, по периферии - вал из эпителиоидных клеток и лимфоцитов с примесью макрофагов и плазматических клеток. Между эпителиоидными клетками и лимфоцитами располагаются гигантские клетки Пирогова-Лангханса (рис. 71, 72), которые весьма типичны для туберкулезной гранулемы. При импрегнации солями серебра среди клеток гранулемы обнаруживается сеть аргирофильных волокон. Небольшое число кровеносных капилляров обнаруживается только в наружных зонах
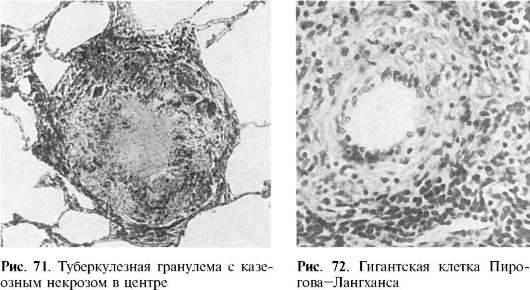 бугорка. При окраске по Цилю-Нильсену в гигантских клетках выявляют микобактерии туберкулеза.
бугорка. При окраске по Цилю-Нильсену в гигантских клетках выявляют микобактерии туберкулеза.
представлена обширным очагом некроза, окруженным клеточным инфильтратом из лимфоцитов, плазмоцитов и эпителиоидных клеток; гигантские клетки Пирогова-Лангханса встречаются редко (рис. 73). Для гуммы весьма характерно быстрое образование вокруг очага некроза соединительной ткани с множеством сосудов с пролиферирующим эндотелием (эндоваскулиты). Иногда в клеточном инфильтрате удается выявить методом серебрения бледную трепонему.
Лепрозная гранулема (лепрома) представлена узелком, состоящим в основном из макрофагов, а также лимфоцитов и плазматических клеток. Среди макрофагов выделяются большие с жировыми вакуолями клетки, содержащие упакованные в виде шаров микобактерии лепры. Эти клетки, весьма характерные для лепромы, называют лепрозными клетками Вирхова (рис. 74). Распадаясь, они высвобождают микобактерии, которые свободно располагаются среди клеток лепромы. Количество микобактерии в лепроме огромно. Лепромы нередко сливаются, образуя хорошо васкуляризированную лепроматозную грануляционную ткань.
Склеромная гранулема состоит из плазматических и эпителиоидных клеток, а также лимфоцитов, среди которых много гиалиновых шаров. Очень характерно появление крупных макрофагов со светлой цитоплазмой, называемых клетками Микулича. В цитоплазме выявляется возбудитель болезни - палочки Волковича-Фриша (рис. 75). Характерен также значительный склероз и гиалиноз грануляционной ткани.
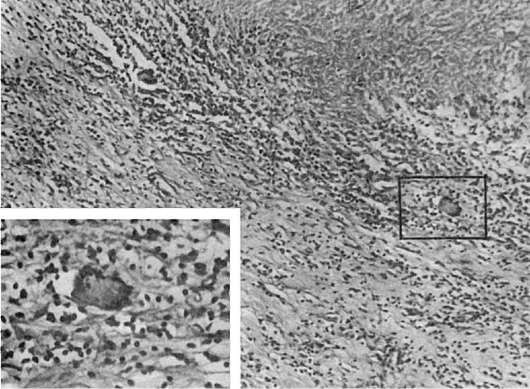 Рис. 73.
Сифилитическая гранулема (гумма)
Рис. 73.
Сифилитическая гранулема (гумма)
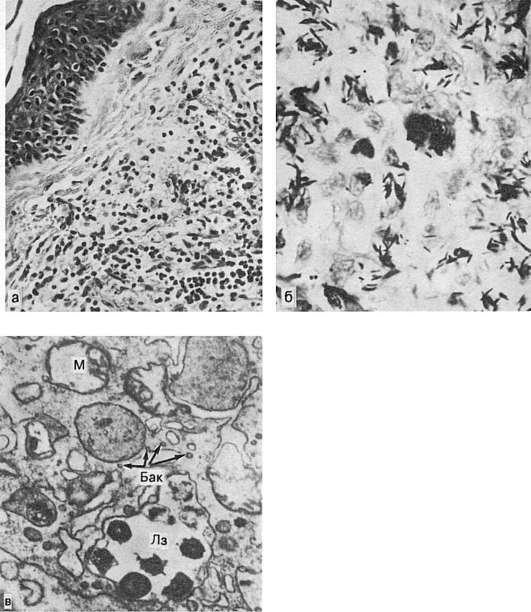 Рис. 74.
Лепра:
Рис. 74.
Лепра:
а - лепрома при лепроматозной форме; б - огромное число микобактерии в лепрозном узле; в - лепрозная клетка Вирхова. В клетке скопления микобактерий (Бак), большое число лизосом (Лз); деструкция митохондрий (М). Электронограмма. х25 000 (по Давиду)
 Рис. 75.
Клетка
Микулича при склероме. В цитоплазме видны огромные вакуоли (В), в
которых содержатся бациллы Волковича-Фриша (Б). ПзК - плазматическая
клетка (по Давиду). х7000
Рис. 75.
Клетка
Микулича при склероме. В цитоплазме видны огромные вакуоли (В), в
которых содержатся бациллы Волковича-Фриша (Б). ПзК - плазматическая
клетка (по Давиду). х7000
Неспецифические гранулемы не имеют характерных черт, присущих специфическим гранулемам. Они встречаются при ряде инфекционных (например, сыпнотифозная и брюшнотифозная гранулемы) и неинфекционных (например, гранулемы при силикозе и асбестозе, гранулемы инородных тел) заболеваний.
Исход гранулем двоякий - некроз или склероз, развитие которого стимулируют монокины (интерлейкин I) фагоцитов.
Продуктивное воспаление с образованием полипов и остроконечных кондилом. Такое воспаление наблюдается на слизистых оболочках, а также в зонах, граничащих с плоским эпителием. Для него характерно разрастание железистого эпителия вместе с клетками подлежащей соединительной ткани, что приводит к образованию множества мелких сосочков или более крупных образований, называемых полипами. Такие полипозные разрастания наблюдаются при длительном воспалении слизистой оболочки носа, желудка, прямой кишки, матки, влагалища и др. В участках плоского эпителия, который расположен вблизи призматического (например, в анусе, половых органах), отделяемое слизистых оболочек, постоянно раздражая плоский эпителий, ведет к разрастанию как эпителия, так и стромы. В результате этого возникают сосочковые образования - остроконечные кондиломы. Они наблюдаются при сифилисе, гонорее и других заболеваниях, сопровождающихся хроническим воспалением.
Течение продуктивного воспаления может быть острым, но в большинстве случаев хроническим. Острое течение продуктивного воспаления характерно для ряда инфекционных заболеваний (брюшной и сыпной тифы, туляремия, острый ревматизм, острый гломерулит), хроническое течение - для большинства межуточных продуктивных процессов в миокарде, почках, печени, мышцах, которые заканчиваются склерозом.
Исход продуктивного воспаления различен в зависимости от его вида, характера течения и структурно-функциональных особенностей органа и ткани, в которых оно возникает. Хроническое продуктивное воспаление ведет к развитию очагового или диффузного склероза органа. Если при этом развиваются деформация (сморщивание) органа и его структурная перестройка, то говорят о циррозе. Таковы нефроцирроз как исход хронического продуктивного гломерулонефрита, цирроз печени как исход хронического гепатита, пневмоцирроз как исход хронической пневмонии и т.д.
Значение продуктивного воспаления очень велико. Оно наблюдается при многих болезнях и при длительном течении может приводить к склерозу и циррозу органов, а значит - к их функциональной недостаточности.
Человек - существо довольно хрупкое. Но природа, заботящаяся о выживании вида, преподнесла людям весьма значимый подарок - иммунитет. Именно благодаря ему наш организм существует, эволюционирует и препятствует агрессивным инфекционным агентам.
Воспаление - вред или защита организма?
Важно учитывать, что воспаление не является синонимом инфекции. Это типовой иммунный ответ на любое болезнетворное проникновение в организм, тогда как инфекция - это и есть агрессивный агент, провоцирующий такую реакцию.
Историческая справка
Воспаление, стадии воспаления, его характерные признаки были известны еще в начале нашей эры. В частности, этими вопросами интересовались древние ученые - Клавдий Гален и римский писатель Корнелий Цельс.  Именно последний выделил четыре главные составляющие любого воспаления:
Именно последний выделил четыре главные составляющие любого воспаления:
- эритема (появление красноты);
- отёк;
- гипертермия;
- боль.
Существовал и пятый признак - нарушение функций пораженного участка или органа (последний пункт был дополнен гораздо позже Галеном).
Впоследствии немало ученых занималось этой темой. Изучал ее и знаменитый на весь мир биолог Илья Ильич Мечников. Он считал воспалительную реакцию целительной, истинным природным даром, но все же нуждающимся в дальнейшем эволюционном развитии, поскольку не все подобные процессы приводят к выздоровлению организма. Не говоря о том, что особо тяжелые воспаления заканчиваются летальными случаями.
Терминология
Если в организме происходит данный процесс (стадии развития воспаленияв этом случае не берутся во внимание), то к названию недуга, как правило, по-латыни, обязательно добавляется характерное окончание «-ит». Например, воспаления гортани, почек, сердца, брюшины, поджелудочной железы называются, соответственно, ларингит, нефрит, миокардит, перитонит, панкреатит. Если к общему воспалению органа присоединяется заболевание находящейся рядом с ним соединительной или жировой ткани, то к названию добавляют приставку «пара-»: паранефрит, параметрит и т. д. Но в данном вопросе, как и в любом правиле, есть исключения, например, такие специфические определения, как ангина или пневмония.
Почему появляется воспаление?
Итак, каковы основные причины воспаления? Их различают трех видов:
 Также причинами воспаления могут стать серьезные психологические травмы, постоянные стрессы и злоупотребление алкоголем.
Также причинами воспаления могут стать серьезные психологические травмы, постоянные стрессы и злоупотребление алкоголем.
Такие процессы или протекают остро, или принимают хроническую форму. Когда реакция на раздражитель наступает сразу, то есть лейкоциты и плазма приходят в движение и ведут себя в пораженных областях весьма активно, это характеризует именно острый процесс. Если же изменения на клеточном уровне происходят постепенно, то воспаление именуют хроническим. Подробнее о типах и формах речь пойдет в дальнейшем.
Симптоматика
Все стадии развития воспаления характеризуются сходными основными симптомами. Они подразделяются на местные и общие. Первая группа признаков включает в себя:
- Гиперемия (краснота) пораженного участка. Этот признак возникает вследствие интенсивного притока крови.
- Гипертермия - увеличение местной температуры, поскольку ускоряется обмен веществ.
- Отечность, если имеет место пропитка тканей экссудатом.
- Ацидоз - увеличение кислотности. Этот признак часто возникает из-за лихорадки.
- Гипералгия (интенсивные болевые ощущения). Появляется в ответ на воздействие на рецепторы и нервные окончания.
- Утрата или нарушение работы пораженной области. Происходит как результат всех вышеописанных симптомов.
 Кстати, воспаление внутренних органов не всегда проявляется болезненными ощущениями, но если процесс протекает на поверхности, то присутствуют практически все вышеперечисленные симптомы.
Кстати, воспаление внутренних органов не всегда проявляется болезненными ощущениями, но если процесс протекает на поверхности, то присутствуют практически все вышеперечисленные симптомы.
Общие признаки можно обнаружить с помощью лабораторных исследований, в частности, развернутого анализа крови. Например, характерные изменения формулы крови в лейкоцитарной ее части, а также значительное увеличение СОЭ. Таким образом, внимательно изучив данный комплекс симптомов, можно диагностировать воспаление. Стадии воспаления - следующий вопрос, интересующий людей, изучающих данную тему.
Стадии и типы развития воспалительного процесса
Как и любой процесс, этот также развивается ступенчато. Выделяют 3 Они могут быть развиты в разной степени, но присутствуют всегда. Если описать их простыми словами, то это повреждение, выход экссудата и тканевое разрастание. Первая стадия воспаления- альтерация. Далее следует экссудация, а после нее - пролиферация.
Теперь стоит немного подробнее обсудить типы воспалений, непосредственно связанные со стадиями. Как уже упоминалось, когда процесс развивается стремительно, то его называют острым. Обычно, чтобы квалифицировать его таковым, помимо временного фактора должны преобладать такие стадии острого воспаления, как экссудация и пролиферация.
 Существует еще одно разделение: банальный (обычный) и иммунный воспалительный процесс. Во втором случае реакция иммунитета. Изучая стадии и механизмы воспаления подобного типа, можно с уверенностью сказать, что ступенчатость зависит от того, замедленное оно или немедленное. Данное утверждение объясняется довольно просто: прежде всего стоит отметить, что механизмом при данном воспалении является тандем "антиген - антитело". Если реакция на определенное вмешательство в организм развивается сразу же, то сначала активируется именно этот механизм, а позже вследствие процессов фагоцитоза, смешения указанного тандема с лейкоцитами и повреждения данным комплексом сосудистых стенок стремительно нарастает отек тканей и множественные кровоизлияния. Примером такого острого состояния может служить анафилактический шок, отёк Квинке (или ангионевротический) и другие процессы, требующие применения реанимационных мер.
Существует еще одно разделение: банальный (обычный) и иммунный воспалительный процесс. Во втором случае реакция иммунитета. Изучая стадии и механизмы воспаления подобного типа, можно с уверенностью сказать, что ступенчатость зависит от того, замедленное оно или немедленное. Данное утверждение объясняется довольно просто: прежде всего стоит отметить, что механизмом при данном воспалении является тандем "антиген - антитело". Если реакция на определенное вмешательство в организм развивается сразу же, то сначала активируется именно этот механизм, а позже вследствие процессов фагоцитоза, смешения указанного тандема с лейкоцитами и повреждения данным комплексом сосудистых стенок стремительно нарастает отек тканей и множественные кровоизлияния. Примером такого острого состояния может служить анафилактический шок, отёк Квинке (или ангионевротический) и другие процессы, требующие применения реанимационных мер.
При замедленной реакции на антиген процесс не столь стремителен (например, В этом случае лимфоциты сначала находят и уничтожают инородного агента вместе с тканями. Далее происходит медленное нарастание гранулемы. Данный процесс характеризуется довольно затяжным течением.
Таким образом, выделяют следующие типы воспалительных процессов:
- Острый. Его длительность исчисляется несколькими часами. Бывают случаи, что он проходит около недели.
- Подострый. Обычно завершается по прошествии нескольких недель.
- Хронический. Может длиться годами или даже пожизненно, протекая волнообразно: от обострения до ремиссии.
Повреждение: первая стадия
Итак, переходим к непосредственному описанию ступенчатых изменений в организме. Любое воспаление начинается именно так. Как уже говорилось, 1 стадия воспаления называется альтерацией (от слова alteratio
- "повреждение").  Именно разрыв тканей и, соответственно, нарушение целостности клеток и сосудов ведут к некротическим изменениям и высвобождению Эти активные вещества меняют сосудистый тонус, вызывая резкие болевые ощущения и отёки.
Именно разрыв тканей и, соответственно, нарушение целостности клеток и сосудов ведут к некротическим изменениям и высвобождению Эти активные вещества меняют сосудистый тонус, вызывая резкие болевые ощущения и отёки.
Экссудация
Сосудистые расстройства в воспаленной области вызывают экссудацию (exudatio). Это и есть 2 стадия воспаления.Процесс заключается в выходекровяной жидкости в ткани. Она называется экссудатом, что и дало повод именовать этот процесс именно так. При возникновении данной стадии вызывает воспаление именно активизация медиаторов и нарушение работы сосудов. ![]() Вследствие спазма, происходящего в артериолах, на поврежденном участке значительно усиливается кровоток, что приводит к гиперемии. Далее увеличивается обмен веществ, а гиперемия из артериальной переходит в венозную. Сосудистое давление стремительно возрастает, и жидкая кровяная часть выходит из их границ. Экссудат может быть различного наполнения, от этого будет зависеть воспалительная форма, вызванная им.
Вследствие спазма, происходящего в артериолах, на поврежденном участке значительно усиливается кровоток, что приводит к гиперемии. Далее увеличивается обмен веществ, а гиперемия из артериальной переходит в венозную. Сосудистое давление стремительно возрастает, и жидкая кровяная часть выходит из их границ. Экссудат может быть различного наполнения, от этого будет зависеть воспалительная форма, вызванная им.
Продуктивный процесс
Третья стадия воспаления называется пролиферативной.Эта воспалительная ступеньявляется завершающей. Регенеративные процессы, происходящие в тканях, позволяют либо восстановить поврежденные воспалением участки, либо на этом месте образуется рубец. Но в данной устоявшейся и стабильной схеме есть нюансы: 3 стадии воспалениямогут быть разной степени интенсивности. Поэтому различают еще и различные формыэтих процессов.
Основные формы
Типы, формы и стадии воспаления - это то, на что необходимо обратить внимание в первую очередь. Как мы уже выяснили, продолжительность процесса определяется таким понятием, как тип. Но это не все характеристики, с помощью которых можно оценить воспаление.  Стадии воспаления - это основа его квалификации и оценки. Но случается так, что составляющие процесса выражены в разной степени. В зависимости от основы воспалительной реакции различают три формы специфических изменений:
Стадии воспаления - это основа его квалификации и оценки. Но случается так, что составляющие процесса выражены в разной степени. В зависимости от основы воспалительной реакции различают три формы специфических изменений:
Исходя из вышесказанного, следует более подробно остановиться на том, какие стадии гнойного воспаления выделяют специалисты:
- Серозный инфильтрат.
- Некротический процесс (флегмозный, гангренозный, абсцедирующий)
Основные гнойничковые образования подразделяются на следующие виды:
- Очаговое воспаление (гнойник). Иначе такой процесс называют абсцессом. При таком воспалении происходит следующее: в очаге инфекции образуется гноящаяся полость с постоянным притоком в нее лейкоцитов. Если абсцесс прорывается вовне, то его именуют свищем. Сюда же относят фурункулы и карбункулы.
- Эмпиема - это образование гнойного экссудата в естественных полостях (аппендикс, плевра, паренхимы) по причине невозможности оттока содержимого.
- Инфильтрат. По-другому эта стадия называется флегмоной. В данном случае гной пропитывает орган полностью. Процесс отличается широким распространением по всей структуре пораженной области.
Гнойный экссудат может полностью рассосаться, образуя рубец. Но существует и возможность неблагоприятного исхода. Это происходит, если гной поступает в кровоток. В результате неизбежно развивается сепсис, и процесс приобретает опасный, генерализованный характер, инфекция разносится по организму.
Характерный пример: пневмония
Это одно из серьезнейших и довольно непредсказуемых заболеваний, причиной которого являются различные возбудители, вызывающие воспаление легких. Именно наличие экссудата в альвеолах затрудняет дыхание больного и провоцирует изменение качества жизни в худшую сторону. Заболеваемость зависит от различных факторов, прежде всего от иммунитета человека. Но в любом случае отследить все три стадии воспалительного процессана примере данного недуга возможно.
![]() Пневмония также протекает ступенчато. С точки зрения патогенеза различают 4 стадии воспаления легких: прилив, красное опеченение, серое опеченение, разрешение. Первая из них как раз характеризует вторжение инфекционного агента в организм, повреждение целостности клеток (альтерация). Вследствие этого возникает гиперемия, кожные аллергические реакции, затрудненное дыхание, учащенный пульс, признаки тяжелой интоксикации.
Пневмония также протекает ступенчато. С точки зрения патогенеза различают 4 стадии воспаления легких: прилив, красное опеченение, серое опеченение, разрешение. Первая из них как раз характеризует вторжение инфекционного агента в организм, повреждение целостности клеток (альтерация). Вследствие этого возникает гиперемия, кожные аллергические реакции, затрудненное дыхание, учащенный пульс, признаки тяжелой интоксикации.
В стадиях гепатизации (красное и серое опеченение) активно образовывается экссудат в легочных тканях. Именно этот процесс вызывает явственные хрипы, проявления интоксикации, неврологические расстройства. Образование мокроты очень обильно - экссудат заполняет буквально всю пораженную область. Насколько серьезна пневмония, говорит фактор обширности поражения (очаг, сегмент, доля легкого или же тотальное воспаление). Бывают случаи сливания очагов в один.
Во время протекания стадии разрешения происходит отделение образовавшегося экссудата, восстановление (пролиферация) пораженных участков легкого и постепенное выздоровление. Безусловно, стадии воспаления легких наглядно демонстрируют процессы, характерные для описываемого состояния организма. Помимо пневмонии примером наиболее характерных заболеваний, напрямую связанных с развитием воспалений, могут стать:
- Атеросклероз.
- Раковые опухоли.
- Астматические изменения.
- Простатиты: как острый, так и хронический.
- Заболевания сердечно-сосудистой системы (например, ишемическая болезнь).
- Гломерулонефрит.
- Кишечные воспаления.
- Недуги органов, находящихся в районе малого таза.
- Ревматоидный артрит.
- Группа аутоиммунных заболеваний.
- Васкулит.
- Циститы.
- Неприятие трансплантата.
- Саркоидоз.
Наконец, банальная угревая сыпь также появляется вследствие воспалительных процессов на поверхности кожи и в более глубоких слоях эпидермиса.
 Примечательно, что иммунитет часто проделывает с организмом злую шутку, провоцируя развитие воспалений. Если вкратце описать данный процесс, то можно сказать, что иммунные тела атакуют собственный организм. Они могут воспринимать целые системы органов как угрозу жизнедеятельности всей структуры. Почему так происходит, к сожалению, до конца не изучено.
Примечательно, что иммунитет часто проделывает с организмом злую шутку, провоцируя развитие воспалений. Если вкратце описать данный процесс, то можно сказать, что иммунные тела атакуют собственный организм. Они могут воспринимать целые системы органов как угрозу жизнедеятельности всей структуры. Почему так происходит, к сожалению, до конца не изучено.
Краткое заключение
Конечно, от воспалительных изменений разной степени тяжести не застрахован ни один из ныне живущих. Более того, данный процесс подарен человечеству природой и призван развить иммунитет и помочь организму более успешно пройти по пути эволюции. Поэтому понимание механизмов, происходящих во время воспалительных метаморфоз, необходимо каждому сознательному жителю планеты.
Допущено
Всероссийским учебно - методическим центром
по непрерывному медицинскому и фармацевтическому образованию
Министерства здравоохранения Российской Федерации
в качестве учебника для студентов медицинских институтов
8.1. Инициирование воспалительного процесса
Инициирование воспалительного процесса происходит в результате повреждения тканей, безразлично какого происхождения:
- физического: ожог, холод, ионизирующая радиация;
- механического: механические травмы, неправильный прикус зубов, отрыв эпителиального слоя слизистой при удалении ватного валика и т.д.;
- химического: кислоты, щелочи;
- биологического: иммунные реакции ГЧНТ и ГЧЗТ с образованием комплексов антител или Т-киллеров с антигеном или в результате действия инфекционных возбудителей, попадания в кровоток ферментов (трипсина, фосфолипазы змеиного яда и т.д).
Хотя названы основные причины воспаления, их количество неограничено. Это вытекает из самой биологической природы воспаления, которое вызывается инфекционными или неинфекционными агентами. Воспаление возникает как местная реакция, ее биологический смысл в ограничении очага поражения. Выделение БАВ подключает общие реакции организма, направленные на восстановление гомеостаза. Если и они не справляются, то местный процесс переходит в болезнь, например, развивается бактериемия и сепсис.
Терминология: к названию органа добавляется окончание "ит" - гепатит, миокардит, гастрит, хейлит, глоссит, стоматит, пульпит, периодонтит.
8.2. Стадии местных реакций при воспалении
- Альтерация
- Сосудистые расстройства, экссудация и эмиграция
- Пролиферация
В запуске (этиологии) воспаления основное значение имеет прямое действие повреждающего фактора (физического, химического, биологического) на мембрану лизосомы (Рис. 16). Механизм возникновения воспалительных процессов в полости рта (пульпит, периодонтит, стоматит) аналогичен воспалению других органов. Первичная или вторичная альтерация связана с лизосомами.
Эти внутриклеточные частицы - "самое кислое место клетки" (т.е. работают при pH менее 7). Они располагают набором ферментов того же механизма действия и класса, что и ферменты желудочно-кишечного тракта и разрушают полимеры до мономеров: белки - до пептидов, а потом до аминокислот; нуклеиновые кислоты - до мононуклеотидов; углеводы - до моносахаридов.
Ферменты лизосом - ферменты распада. В норме их функция - захват белков цитоплазмы, отдельных мембран, даже внутриклеточных частиц и разрушение их до мономеров. Они работают внутри частиц, т.к. мембрана надежно ограничивает лизосомное содержимое. Роль - обновление (пластика) клетки. Процесс внутриклеточного переваривания необходим для любых процессов типа атрофии. При помощи этого механизма осуществляется атрофия лимфоидного фолликула, слизистой эндометрия при менструации, тканей, составляющих лунку удаленного зуба и т.д. Т.е. лизосомы необходимы для процесса дифференциации клеток - замены одних структур на другие. При воспалении функции лизосом меняются из-за повышения проницаемости их биомембран под влиянием этиологических факторов воспаления.
8.2.1. Первая стадия воспаления - альтерация
Развивается резкое усиление катаболизма (альтерация), накопление мономеров в очаге нарушения и увеличение осмотического давления. Гибель митохондрий ведет к усилению анаэробного процесса выработки АТФ - гликолизу. Глиалуронидаза и коллагеназа лизосом вызывают расщепление гиалуроновой кислоты, коллагена.
Ключевое событие - активация фактора Хагемана (XII РСК). Это белок является протеазой, с которой связаны все дальнейшие события.
Итог 1 стадии - альтерация + активация фактора Хагемана.
8.2.2. Вторая стадия - сосудистые реакции, экссудация, эмиграция
Патогенез:
- фактор Хагемана активирует реакцию свертывания крови, ведущую к микротромбозу (сладж) и циркуляторной гипоксии;
- фактор Хагемана активирует комплемент (из С3а - фрагмента образуется анафилотоксин, разрушающий тучные клетки - депо БАВ);
- фактор Хагемана вызывает активацию каскада образования кининов, определяющих повышение проницаемости, возбудимости, вазодилятацию, боль.
Все это ведет к тромбозу и отеку. Последний симптом объясняется повышением проницаемости стенок микрососудов и повышением осмотического давления в очаге воспаления.
8.2.2.1. Сосудистые реакции
Сосудистые реакции лежат в основе как, собственно, изменения кровотока в русле микроциркуляции, так и экссудации, и эмиграции. Новое явление - нарушение микроциркуляции, гиперемия, плазмопотеря, агрегация тромбоцитов, образование эритроцитарных столбиков. Это приводит к возникновению диссеминированного микротромбоза (сладжу), стазу. Кровь не может течь свободно, в результате развивается гипоксия. Безусловно, здесь участвуют биохимические факторы. Для агрегации необходимы АДФ, тромбин, вещества-регуляторы.
8.2.2.2. Экссудация
Экссудация - выход жидкой части крови в очаг воспаления, вызван повышением Роем давления в очаге и повышением проницаемости сосудов под влиянием ферментов лизосом, и БАВ (в первую очередь, гистамина и брадикининов). Воспалительный экссудат характеризуется наличием в нем белка и, прежде всего, фибриногена. Свертываясь, он образует фибринную пленку, отграничивающую очаг.
Регуляцию второй стадии воспаления ведут "моторы" воспаления - БАВ. Факторы тучных клеток и их аналогов в крови - базофилов - работают в раннюю фазу процессов. К ним относятся:
- Основные белки лизосом - катионные белки, оказывающие ряд эффектов, по свойствам похожих на гистаминовые. Они повышают проницаемость микрососудов, обусловливая экссудацию, эмиграцию. Хемотаксис - также опосредованный ими эффект, т.е. лейкоциты движутся к очагу воспаления по нарастающей концентрации основных белков лизосом (от периферии к центру).
- Амины - возникают из аминокислот. Гистамин образуется в тучных клетках (специализированные клетки соединительной ткани, расположенные вокруг микрососудов). В норме он связан с гепарином в единый комплекс. Одна из причин освобождения гистамина - основные белки лизосом, вторая - комплекс антиген-антитело. Гистамин повышает проницаемость капилляров и венул путем сокращения миофибрилл эндотелия, при "сморщивании" клеток образуются просветы, что способствует экссудации, отеку. Гистамин - основной фактор ГЧНТ, освобождающийся в ранние сроки.
При иммунных конфликтах за счет воздействия IgЕ, фиксированного на мембране, происходит освобождение Са 2+ и активация фосфолипазы А, которая, разрушая липиды мембран тучных клеток, вызывает образование в них каналов, через которые легко выходят гистамин, серотонин и гепарин.
Типичная кожная реакция на гистамин:
- гиперемия - за счет влияния на гистаминорецепторы клеток гладкой мускулатуры непосредственно или через аксон-рефлекс.
- отек как следствие повышения проницаемости капилляров.
Типичная реакция на серотонин: расширение артериол на фоне спазма венул, ведущее к местному застою крови и выходу плазмы в ткани. ЛСД, блокирующая М-серотониновые рецепторы, подавляет отек.
Ацетилхолин - производное аминокислоты, действующие эффекты выражены в меньшей степени, чем у гистамина.
В поздний период воспаления (часы и более) подключаются новые регуляторы - кинины. Это уже олигопептиды, т.е. они состоят из нескольких аминокислот. Брадикинин - циркулирующий в крови кинин, а каллидин образуется и действует только местно, т.к. быстро разрушается карбоксипептидазой. Период полураспада - 30 сек.

Каскад образования кининов представляется следующим образом (Рис. 17). В крови циркулирует фермент калликреин, в норме он не активен, образуется из самого себя после воздействия пептидаз (в основном, это фактор Хагемана). Ферменты лизосом животных и бактерий (стрептокиназа) могут прямо активировать каскад образования кининов, запуск кининовой системы осуществляется пептидазами - протеолитическпмп ферментами. Это лежит в основе использования ингибиторов протеолиза (например, тразилол).
Патофизиологические эффекты кининов:
- Напоминают эффекты гистамина (гипотензия, повышение проницаемости сосудов), но действующие концентрации во много раз меньше. Запуск эмиграции лейкоцитов.
- Непосредственно вызывают болевые ощущения.
- Брадикардия.
Патогенетическая терапия
При лечении аллергических и воспалительных процессов используют пипольфен и димедрол. У пипольфена средство к гистаминовым рецепторам в 10 раз больше, но действует он хуже, т.к. оказывает чистый антигистаминный эффект, а димедрол дополнительно блокирует действие кининов. Любые факторы, которые делают мембраны лизосом более прочными, тормозят образование кининов: салицилаты, ГКC.
- Другие группы БАВ поздней фазы воспаления: гормоны, производные жирных кислот (лейкотриены и простагландины). Лейкотриены впервые были выделены из лейкоцитов. Они спазмируют сосуды, и являются, как и простагландины, липидными гормонами. Образуются из ненасыщенных жирных кислот типа арахидоновой кислоты во всех клетках всех тканей.
Патофизиологические эффекты лейкотриенов и простагландинов подобны эффектам кининов. Они расширяют сосуды, повышают их проницаемость, способствуют отекам, болевым явлениям. Особенно выражен болевой синдром при пульпитах, может быть вследствие того, что при воспалении происходит отек, а пульпа расположена в неподатливой камере - полости зуба. В таких болезненно измененных деснах концентрация простагландинов в 20 раз больше, чем в норме. Простациклин (простагландин I 2) расширяет сосуды и препятствует агрегации тромбоцитов, тромбоксан А 2 - его антагонист. В норме простагланднны и кинины отвечают за физиологическую гиперемию.
Механизм действия салицилатов длительное время был спорным, сейчас известно, что главное в нем - блок биосинтеза простагландинов. По нарастанию противовоспалительной активности их можно расположить следующим образом: метиндол - бутадион - аспирин.
8.2.2.3. Эмиграция
Нейтрофилы, прилипая к нарушенному эндотелию сосудов выделяют факторы проницаемости (интерлейкин-1, лейкотриены, простагландины) и переходят (эмигрируют) в межклеточное пространство по градиенту концентрации основных белков лизосом, уже образовавшихся в очаге пораженной ткани. Там нейтрофилы выделяют дополнительные факторы хемотаксиса. С появлением их в очаге поражения и начинается воспаление. Цель - фагоцитоз. Все эти события относятся к ранней фазе воспаления. С помощью метода "кожного окна" (скарификация кожи и мазок на приложенном стекле) было показано, что появление нейтрофилов обнаруживается в первые 4 часа от начала воздействия повреждающего агента. Поздняя фаза воспаления развивается примерно через 24 часа и характеризуется появлением макрофагов в очаге воспаления, после чего его характер меняется, подключается иммунная система.
Механизм фагоцитоза и уничтожения воспалительного агента общий и заключается в том, что в месте контакта чужеродного тела (бактерии, иммунные комплексы и т.д.) с плазматической мембраной лейкоцита, макрофага, образуется ее впячивание. На ввернутой таким образом внутрь поверхности мембраны (фагосоме) начинается образование миелопероксидазой супероксидного радикала O 2 - , обладающего бактерицидным действием. Дефект генерации О 2 - ведет к феномену, называемому "незавершенным фагоцитозом" и проявляется хронизацией воспаления и картиной иммунодефицитного состояния.
Итог II стадии: сосудистая реакция в виде спазма, гиперемии, микротромбоз и циркуляторная гипоксия с развитием триады (дефицит АТФ, ацидоз, повреждение биомембран). Экссудация и эмиграция нейтрофилов (гнойный экссудат), затем макрофагов (очищение раны и запуск пролиферации).
8.3. Пролиферация - III стадия воспаления
Наиболее быстро происходит размножение клеток соединительной ткани - фибробластов. Например, гепатоциты, миокардиоциты, клетки слизистых не могут регенерировать столь быстро, поэтому на месте их воспалительного разрушения образуются рубцы. Прямых биохимических данных, что конкретно способствуют запуску пролиферации в очаге дефекта ткани, нет. Похоже, процесс подчиняется общему правилу: чем менее клеток в каком-либо объеме, тем больше они пролиферируют. Клетки, предоставленные сами себе, не нуждаются в активаторах пролиферации. Что же заставляет их пролиферировать? Это феномен контактного ингибирования. Если бы его не было, злокачественные опухоли вырастали бы в каждом органе.
Примечание верстальщика: текст размещается согласно первоисточника
Теория контактного ингибирования
В плазматической мембране клеток есть гликопротеиды и гликолипиды, играющие специфическую функцию. Они образуют своеобразные "усики" на наружной поверхности клеток. При соприкосновении клеток первичным моментом является соприкосновение "усиков", а вторичным - увеличение внутри клетки уровня цАМФ, который, вероятно, и запускает цепь биохимических реакций, ведущих к подавлению митоза клетки.
Оказывается, в клетках быстро пролиферирующих тканей цАМФ очень мало. Когда клеток становится много, концентрация цАМФ в них резко возрастает. При добавлении цАМФ рост клеток замедляется: в злокачественных опухолях мало цАМФ. Чем быстрее растет ткань, тем меньше в ее клетках цАМФ.
Резюме но функциям лизосом при воспалении. Лизосомы - это старт и финиш воспаления. Они разворачивают его и способствуют благоприятному его исходу. Остальные факторы воспаления являются моторами.
- Лизосомы осуществляют альтерацию тканей.
- Лизосомы играют ведущую роль в повышении концентрации БАВ, определяющих II стадию процесса:
- поставляют основные (катионные) белки
- способствуют освобождению гистамина, лейкотрпенов, а, возможно, и других факторов воспаления в результате дегрануляции тучных клеток;
- ферменты лизосом активируют систему кининов, фибринолиз (активацию плазмина).
- Лизосомы способствуют ликвидации самого воспалительного процесса, например, путем разрушения комплекса антиген-антитело и бактерии.
- Лизосомы участвуют в подготовке к III стадии воспаления путем ликвидации поврежденных тканей, поэтому ингибиторы пептидаз лучше помогают в начале воспаления, а сами пептидазы - в его конце.
Приведенные факторы и легли в основу обоснования современной гипотезы патогенеза воспаления: освобождения ферментов лизосом, атака ими внеклеточных субстратов (тучные клетки, предшественники БАВ). Продукты этих реакций нарушают микроциркуляцию в очаге воспаления. Исход зависит не только от факторов агрессии, но и от гомеостатических способностей самого организма.
8.4. Регуляция воспаления - фактически принципы его лечения
- стадия, альтерация
- стабилизаторы мембран лизосом (ГКС, салицилаты, соли золота)
- ингибиторы ферментов лизосом (контрикал, тразилол, дексаметазон, ингибиторы фосфолипаз)
- стадия, сосудистых расстройств, экссудации, эмиграции
- воздействие на сосудистые реакции - блокаторы синтеза рецепторов БАВ (антигистаминовые), биосинтеза простагландинов, лейкотриенов (салицилаты)
- воздействие на процессы экссудации - витамины С, РР для увеличения биосинтеза коллагена
- воздействие на процесс эмиграции - лечение иммунодефицитного состояния
- стадия, пролиферация: - использование стимуляторов биосинтеза белка (анаболики):
- обработка некротизированной ткани очага воспаления протеазами
- андрогены: способствуют процессам биосинтеза. Важны в процессе выздоровления, их не хватает. Хороши анаболические стероиды - нерабол Сохраняют способность повышать биосинтез белка, но лишены свойств мужских половых гормонов.
8.5.Общие реакции при воспалении и патогенетическая диагностика
8.5.1.Изменения содержания и соотношения белков плазмы крови: 8.5.1.1. Альбумины: при остром воспалении их количество увеличивается, а при хроническом - уменьшается. Их биосинтез ведется только гепатоцитами. 8.5.1.2. Глобулины: ряд белков этой фракции (иммуноглобулины) синтезируются плазматическими клетками. При остром воспалении увеличивается содержание альфа-1 и альфа-2 глобулинов, при хроническом - альфа-2 и гамма-глобулинов. Это важно для диагностики, т.к. иммуноглобулины относятся к фракции гамма-глобулинов и они образуются в более поздний период воспаления. Признак перехода процесса в хроническую форму - совокупность нарушений содержания альбуминов и глобулинов отражается в изменениях альбумин/глобулинового коэффициента. 8.5.2. Увеличение содержания гликопротеинов: фибриногена, протромбина и их углеводных компонентов - сиаловой кислоты, серомукоида. Большая часть гликопротеинов синтезируется в печени, т.е. их увеличение представляет собой вторичную реакцию. Чем острее воспаление, тем больше гликопротеинов в плазме крови. Для диагностики гликопротеины не дают ничего, т.к. повышаются и при сахарном диабете, при беременности. Но много дают для определения тяжести процесса.Вывод: гликопротеины - важный показатель динамики воспаления и эффективности лечения. Если во время лечения в крови увеличивается содержание гликопротеинов, то схему лечения необходимо менять. 8.5.3. Активация САС и деятельности коры надпочечников (ОАО), особенно пучковой (ГКС) и сетчатой (минералокортикостероиды), то есть как при типичной реакции на любой стресс.
Эффекты ГКС при воспалении:
- Повышают прочность мембран лизосом.
- Повышают прочность сосудистой стенки, следовательно, снижается экссудация.
- Уменьшают эмиграцию лейкоцитов в очаг воспаления.
- Ингибируют фагоцитоз.
- Тормозят развитие соединительной ткани, подавляют рост и размножение фибробластов
- Снижают биосинтез антител, как и всех белков.
- Подавляют образование T-лимфоцитов, вызывая атрофию лимфоидных органов
Поэтому ГКС широко используют в терапии воспаления, но локально подавляя процесс, они способствуют его генерализации. 8.5.4. Лихорадка. Нейтрофильный лейкоцитоз вызывает образование de novo особого белка - интерлейкина-1, ранее называемого лейкоцитарным пирогеном. Он вызывает смещение установочной точки центра терморегуляции на более высокий уровень, стимулирует фагоцитоз и активность Т-киллеров. 8.5.5. Лейкоцитоз. Под влиянием лейкоцитарных факторов и продуктов распада тканей очага воспаления формируется стимулирующий фактор, активирующий пролиферацию клеток миелоидного ростка костного мозга, как гранулярного, так и моноцптарного рядов.
8.6. Переход острого воспаления в хроническое
В основе лежит возникновение аутоаллергпческих процессов как на измененные в ходе воспаления собственные белки, так и в результате сходства с бактериальными возбудителями. Происходит формирование устойчивого цикла звеньев патогенеза по типу порочного круга.
Патогенетическая терапия: очень важно в схему противовоспалительного лечения включить антиаллергическую терапию: лечение возможного иммунодефицитного состояния.
8.7. Воспаление и гомеостаз
Безусловно, воспаление в своей основе играет защитную роль. С помощью этого сложного процесса организм стремится отграничить, окружить фактор агрессии или собственную омертвевшую ткань и удалить их, чтобы сохранить функциональное и морфологическое постоянство организма.
На это направлены как механизмы местного предотвращения нарушений гомеостаза, так и общие системные реакции восстановления гомеостаза. При избыточном действии фактора агрессии гомеостатические механизмы не справляются и, в этом случае, воспаление переходит в болезнь.
Медицинский термин «патогенез» означает механизм развития заболевания. Оно является патологическим процессом в организме, которое несет в основном защитную функцию от болезнетворных агентов. В этой статье мы рассмотрим патогенез, формы и фазы воспаления на каждом этапе развития болезни.
Как развивается патогенез воспаления?
Патогенез воспаления обусловлен тремя фазами воспалительного процесса:
процесс альтерации – повреждение тканей;
сосудистая реакция в патогенезе воспаления – нарушение циркуляции в мельчайших сосудах с повышенной проницаемостью стенок, экссудативный процесс и лейкоцитарная эмиграция
процесс пролиферации – образование обновленных тканей.
Следовательно, при наличии всех трех компонентов можно считать процесс, происходящий в организме – воспалительным. В противном случае, при отсутствии даже одного из вышеперечисленных факторов – патогенез воспаления не развивается. Каждый из факторов имеет право на самостоятельное существование без участия в воспалении.
Патогенез и альтерация воспаления
Альтерация в переводе с латинского языка означает изменение. Процесс альтерации бывает первичным и вторичным.
Во время первичной альтерации происходят процессы и изменения в тканях под непосредственным воздействием болезнетворного агента. Изменения в патогенезе воспаления зависят от длительности и силы повреждений клеток, нервных окончаний, сосудистой системы, способностью организма сопротивляться патогенному фактору и других. Результатом гибели поврежденных клеток являются освобожденные биологически активные вещества, влияющие на протекание воспалительного процесса.
Процесс вторичной альтерации в тканях подразумевает изменения в структуре тканей и нарушении обменных процессов. Масштаб альтерации в патогенезе воспаления охватывает клеточное пространство и межклеточное вещество. Таким образом, развивается воспалительный процесс с дистрофическими явлениями.
Реакция со стороны сосудистой системы при воспалении
Второй фактор, обуславливающий патогенез воспаления – сосудистая реакция. Его проявления наблюдаются в мелких сосудах, таких как капилляры, артериолы, венулы. Реакция сосудов в патогенезе воспаления заключается в резком ограничении распространения патогенных агентов и нарушении обменных процессов. Таким образом, наступает дистрофия тканей и некротические проявления в них, а так же попадание жидких частей крови в ткани и лейкоцитарную эмиграцию. Лейкоциты, попавшие в зону воспаления, принимают участие в механизмах защиты, в частности в фагоцитозе, что приводит к повышению иммунитета. В результате создаются необходимые воспалительные барьеры.
Патогенез фазы пролиферации при воспалении
Этот процесс начинается в самом начале воспалительного процесса. Ткани начинают обновляться при первых нарушениях в клетках. Источниками пролиферации в патогенезе воспаления являются эмигрировавшие в ткани клетки лимфы и макрофаги. Стимулируют пролиферацию продукты альтерации ткани, то есть тканевые стимуляторы.
Фазы развития воспаления и их патогенез
Любой воспалительный процесс можно разделить на этапы. Принято различать 3 фазы воспаления. Эти фазы плавно переходят одна в другую, из-за этого не всегда можно определить четкие границы. Далее мы внимательно рассмотрим все фазы воспаления, и как они протекают.
Патогенез первой фазы воспаления
После поражения ткани наступает первая фаза воспаления. Она характеризуется тем, что проницаемость сосудов увеличивается и жидкость из сосудов, белки и другие тельца, направляются в пораженную зону, происходит экссудат. Также происходит эмиграция лейкоцитов, выход их из сосудов. При экссудате повышается давление, что изменяет в свою очередь кровообращение, нарушается гомеостаз. При попадании лейкоцитов в место поражения начинается процесс фагоцитоза. Вследствие всего этого процесса на первой фазе воспаления ухудшается приток крови.
Вторая фаза воспалительных заболеваний
Заканчиваясь, первая фаза перетекает во вторую, во время которой организм делает попытки избавиться от раздражителей. Изначально задача заключается в том, чтобы избавить организм от токсинов посредством улучшения кровообращения и притока к пораженному месту полезных веществ, ферментов противовоспалительных. Так как при воспалении увеличивается количество лейкоцитов, то это аномальное явление сохраняется в течение еще нескольких дней. Это является защитой организма, в некотором смысле мерой предосторожности.
Патогенез третьей фазы воспаления
Третья фаза воспаления также называется регенеративной фазой. В этот период организм направлен на процесс восстановления ткани. Так как само воспаление произошло из-за некоторого повреждения ткани, то на последнем этапе восполняется урон с помощью соединительной ткани.
Альтернативная классификация фаз воспаления
Но существует еще одна схема, по которой происходит воспалительный процесс. Она была предложена Мартином. По его мнению, фазы воспаления делятся не на три, а на пять фаз. Он считал, что первая фаза самая кратковременная и характерна повышенной проницаемостью сосудов. Она делится три субфазы.
- Первая субфаза (А), это фаза, во время которой увеличивается проницаемость, длится около двух минут.
- Субфаза вторая (В), это уплотнение, происходит отек.
- Последняя субфаза (С), характеризуется образованием гистамина, а также освобождением вещества брадикинина, и разрушением аминов, которые были созданы в субфазе.
Далее протекает вторая фаза воспаления, в которой проницаемость сосудов понижается, за счет увеличения жидкости. При этом начинается расщепление белков до аминокислот. Кровообращение начинает восстановительный процесс на 4 этапе, а на пятом полностью восстанавливаются все ткани.
Формы течения воспаления и их патогенез
При воздействии на организм неблагоприятных факторов, поражающих организм возникает защитная реакция, которая имеет различные проявления. Выделяют 3 формы воспаления, в зависимости от того как они развиваются.
Альтернативная форма воспаления - как она развивается? Обычно она возникает в паренхиматозных органах, таких как сердце, печень, почки. Основной характеристикой которого, есть:
- атрофические,
- некротические,
- дистрофические процессы.
Как развивается экссудативная форма воспаления?
Это воспаление характеризуется тем, что происходит выход белков, различных других клеток и кровеносной жидкости в ткани, а также осуществляется миграция лейкоцитов. В свою очередь эта форма воспаления делится на такие виды: гнойное, гнилостное, гангренозное, серозное, геморрагическое.
Гнойный экссудат в своем составе имеет большое количество белков, а также лейкоцитов. Именно из-за лейкоцитов он приобретает желтовато-зеленую раскраску, так как они отмирают.
Геморрагический экссудат состоит из эритроцитов, и небольшого количества лейкоцитов. Обычно он розоватого или красного цвета. При этом поражаются сосудистые стенки.
Гнилостный (гангренозный) экссудат происходит при воздействии на организм гнилостных бактерий, которые действуют разрушительно на ткань.
Основной характеристикой серозного воспаления, является выделение тканью, которая воспалена, жидкости желтого, или зеленого цвета. Если воспаление в брюшной части, то там может скапливаться обильное количество жидкости, около пары литров.
Как правило, при восстановлении ранее разрушенной ткани, происходит увеличение соединительной, но иногда случается так, что она возникает в больших количествах. И это имеет отношение к продуктивным процессам.
Продуктивна форма воспалительных заболеваний и их патогенез
Обычно эта форма воспаления развивается при воспалении соединительных тканей. При нем наблюдается увеличение пораженного органа, в связи с выходом жидкостей, белков и лейкоцитов в ткани, а далее его уменьшение, так как происходит уплотнение ткани соединительной.
Но формы воспаления на этом не ограничиваются, ведь есть еще такое понятие как воспаление специфическое, которое возникает при определенном процессе. Например, туберкул- элемент воспаления при туберкулезе, узлы- при проказе. Вообще воспалительные процессы разнообразны, иногда проявляется одна форма, в другой раз другая, но в какой-то мере присутствуют все три формы.


