05.09.2018
intracelularna acidoza. Metabolička acidoza: simptomi i liječenje. Liječenje respiratorne acidoze
Acidoza(acidoza; lat. acidus kiselo + -ō sis) - jedan od oblika poremećaja acido-bazne ravnoteže organizma; karakterizira apsolutni ili relativni višak kiselina, tj. tvari koje doniraju vodikove ione (protone) u odnosu na baze koje ih vezuju.
Acidoza može biti kompenzirana i nekompenzirana ovisno o pH vrijednosti - pH vrijednosti biološke sredine (obično krvi), izražavajući koncentraciju vodikovih jona. Kod kompenzirane acidoze pH krvi se pomiče na donju granicu fiziološke norme (7,35). Sa izraženijim pomakom na kiselu stranu (pH manji od 7,35) acidoza smatra nekompenziranim. Ovaj pomak je zbog značajnog viška kiselina i nedovoljnosti fizičko-hemijskih i fizioloških mehanizama regulacije. acido-baznu ravnotežu.
Neuspjeh da se u potpunosti identificiraju ovi faktori može dovesti do katastrofalnog ishoda, bilo zbog lošeg upravljanja tekućinom i elektrolitom ili od stalne posljedice osnovne bolesti koja nije liječena. Ovdje izvještavamo o slučaju pacijenta kod kojeg se razvila teška hiponatremija, metabolička acidoza i hiperazotelija. Ove manifestacije su povezane sa istinskim smanjenjem volumena i ozbiljnim smanjenjem izlučivanja urina. Osim toga, pacijentu se može ponuditi konačan tretman nakon utvrđivanja osnovne bolesti odgovorne za kliničke manifestacije.
Po porijeklu acidoza može biti plinovita, negasovita i mješovita. Gasna acidoza nastaje zbog alveolarne hipoventilacije (nedovoljnog uklanjanja CO 2 iz tijela) ili kao rezultat udisanja zraka ili mješavine plinova koji sadrže povišene koncentracije ugljičnog dioksida. U ovom slučaju, parcijalni pritisak ugljičnog dioksida (pCO 2) u arterijske krvi prelazi maksimalne vrijednosti norme (45 mmHg st.), tj. javlja se hiperkapnija.
Ciprofloksacin je počeo nakon uzimanja uzorka urina. Tri dana kasnije, pacijent je ponovo pregledan zbog upornih simptoma mokrenja. Kontuzija abdomena je kasnije otkrila blagu hidronefrozu, koja je bila izraženija na lijevoj strani. Jugularne vene su bile neproširene, srce i pluća su bili normalni, a abdominalna masa ili bol nisu primećeni.
Kako biste klasifikovali pacijentovu hiponatremiju?
Nekoliko stanja može dovesti do visokog omjera ureje i kreatinina, kao što je prikazano u Tabeli 2. Naš pacijent ima jasne dokaze o dehidraciji. Uzroci visokog omjera uree i kreatinina. Kao što je već spomenuto, fizički pregled ukazuje na dehidraciju. Dakle, hiponatremija je nastala u uslovima hipovolemije.
Negasnu acidozu karakterizira višak nehlapljivih kiselina, primarno smanjenje bikarbonata u krvi i odsustvo hiperkapnije. Njegovi glavni oblici su metabolički, ekskretorni i egzogeni. acidoza.
metabolička acidoza nastaje zbog nakupljanja viška kiselih proizvoda u tkivima, njihovog nedovoljnog vezivanja ili uništenja; sa povećanjem proizvodnje ketonskih tijela (ketoacidoza), mliječne kiseline (laktata- acidoza) i druge organske kiseline. Ketoacidoza se najčešće javlja kod dijabetes, kao i tokom gladovanja (posebno ugljenih hidrata), visoke temperature, teške insulinske hipoglikemije, uz određene vrste anestezije, alkoholne intoksikacije, hipoksije, ekstenzivne upalnih procesa, ozljede, opekotine i sl. Najčešće se javlja laktatna acidoza. Kratkotrajna laktacidoza se javlja kod pojačanog mišićnog rada, posebno kod netreniranih ljudi, kada se povećava proizvodnja mliječne kiseline i dolazi do njene nedovoljne oksidacije zbog relativnog nedostatka kisika. Dugotrajni laktat acidoza primjećuju se kod teških oštećenja jetre (ciroza, toksična distrofija), dekompenzacije srčane aktivnosti, kao i smanjenja opskrbe tijela kisikom zbog insuficijencije vanjskog disanja i drugih oblika kisikovog gladovanja. U većini slučajeva, metabolički A. nastaje kao rezultat viška nekoliko kiselih proizvoda u tijelu.
Šta je uzrok aneurizme?
Dakle, pacijent ima pravu hiponatremiju, a brza korekcija ovog stanja će je dovesti u opasnost od centrokontin micelinolize. Aneurija je često uzrokovana opstrukcijom urinarnog trakta, a zatim je obično povezana s hidronefrozom. Stoga je hidronefroza kod našeg pacijenta mogla nastati samo ako je ustanovljena meka opstrukcija urinarnog trakta i diureza perzistira; simptom "aneurije" u takvom kontekstu bi trebao ukazivati na to da se urin ne izbacuje normalan sistem zbirka. Stoga se čini vrlo vjerojatnim da je pacijent imao fistulu između urinarnog trakta i šupljeg organa, na primjer. crijeva.
Ekskretorna acidoza kao rezultat smanjenja izlučivanja nehlapljivih kiselina iz organizma bilježi se kod bolesti bubrega (na primjer, kod kroničnog difuznog glomerulonefritisa), što dovodi do poteškoća u uklanjanju kiselih fosfata, organskih kiselina. Pojačano izlučivanje natrijevih jona u urinu, što uzrokuje razvoj bubrežne A., uočava se u uvjetima inhibicije procesa acido- i amoniogeneze, na primjer, kada dugotrajna upotreba sulfa lijekovi, neki diuretici. Ekskretorna acidoza (gastroenterični oblik) može se razviti sa povećanim gubitkom baze kroz gastrointestinalnog trakta na primjer, kod proljeva, upornog povraćanja bačenog u želudac alkalnim crijevnim sokom, kao i kod dugotrajnog povećana salivacija. Egzogeni A. nastaje kada se u organizam unese velika količina kiselih jedinjenja, uklj. neke lekove.
Kako biste demonstrirali fistulu?
Prethodna ekspozicija trbušne duplje za karcinom materice je glavni faktor rizika za unutrašnje fistule. Hipoteza o intestinalnoj fistuli može se testirati utvrđivanjem da li se promijenio volumen drenaže ileostome i analiziranjem njegovog sadržaja. Prisustvo kreatinina u stolici, na primjer, ukazuje na prisustvo vaginalne fistule. Radionuklidni pregled bubrega s djelimično očuvanom funkcijom bubrega s abnormalnom distribucijom urina također ukazuje na fistulu.
Radionuklidno skeniranje i retrogradna cistografija potvrdili su prisustvo fistula između segmenta tankog crijeva i Bešika. Nakon ovih tretmana, količina izlučenog urina kroz mjehur značajno se povećala. Radionuklidno skeniranje bubrega pomoću merkaptoacetil-3 pokazuje brzo i intenzivno uzimanje radioizotopa, a zatim brzi prijelaz iz korteksa u mozak. Traser se takođe prerano pojavljuje u karlici i bešici; sabirni sistem, međutim, izgleda blago proširen i postoji izotopna staza u gornjem urinarnom traktu, što ukazuje na blagu ili djelomičnu opstrukciju.
Razvoj mješovitih oblika acidoze (kombinacija plina i raznih vrsta negasnog A.) je posebno posljedica činjenice da CO 2 difundira kroz alveolokapilarne membrane oko 25 puta lakše nego O 2. Stoga je otežano oslobađanje CO 2 iz organizma zbog nedovoljne izmjene plinova u plućima praćeno smanjenjem oksigenacije krvi i, posljedično, razvojem gladovanja kisikom, praćenog nakupljanjem nepotpuno oksidiranih produkata intersticijalnog metabolizma. (uglavnom mlečna kiselina). Takvi oblici acidoze se uočavaju u patologiji kardiovaskularnog ili respiratornog sistema.
Od do se pojavljuje abnormalna sjena u području mjehurića kupole. Od do vidljivo je pojačanje tamne mrlje desna strana kupola mjehura i vjerovatno ukazuje na mjesto fistulizacije. S druge strane, još jedna sjena pokazuje da sve više urina prati "parauretralnu" rutu.
Šta je vaša glavna briga za ispravljanje hiponatremije?
U ovom konkretnom slučaju postoje dva razloga zašto je rizik od brze korekcije visok. Kako se cirkulirajući volumen obnavlja, povećanje volumena urina rezultirat će većim gubitkom slobodne vode od očekivanog zbog osmotske diureze izazvane ureom. Ključ za upravljanje poremećajem vode kod ovog pacijenta je davanje slobodne vode ili prevencija prekomjerne diureze vode uz obnavljanje efektivnog volumena cirkulacije.
Umjereno kompenzirana A. teče gotovo asimptomatski i prepoznata je istraživanjem tampon sistemi krv, kao i sastav urina. Sa produbljivanjem acidoze, jedan od prvih kliničkih simptoma je pojačano disanje, koje potom prelazi u oštar otežano disanje, patološki oblici disanja. Nekompenziranu A. karakterišu značajni poremećaji funkcija centralnog nervnog sistema, kardiovaskularnog sistema, gastrointestinalni trakt, itd. Acidoza dovodi do povećanja sadržaja kateholamina u krvi, dakle, kada se pojavi, dolazi do povećanja srčane aktivnosti, povećanja broja otkucaja srca, povećanja minutnog volumena krvi i porasta krvi. pritisak se prvo zapaža. Kako se A. produbljuje, reaktivnost adrenoreceptora opada, a uprkos povećanom sadržaju kateholamina u krvi, srčana aktivnost se inhibira, krvni pritisak pada. U ovom slučaju često se javljaju različite vrste srčanih aritmija, sve do ventrikularne fibrilacije. Osim toga, acidoza dovodi do naglog povećanja vagalnih učinaka, uzrokujući bronhospazam, pojačano lučenje bronhijalnih i probavnih žlijezda; često se javlja povraćanje, dijareja. Kod svih oblika A., kriva disocijacije oksihemoglobina se pomiče udesno, tj. smanjen je afinitet hemoglobina za kiseonik i njegova oksigenacija u plućima.
Acid-bazni test krvi
Slobodna voda se može dati kao 5% dekstroze, ali visoke brzine infuzije mogu dovesti do osmotske diureze izazvane dekstrozom. Besplatna voda se takođe može davati kao crevna voda iz slavine, što je bezbedno i efikasno.
Kako biste protumačili i objasnili poremećaj kiselinske baze u ovom slučaju?
Diureza slobodne vode se također može smanjiti upotrebom diuretik petlje da stimuliše oslobađanje smole. Očigledno, pacijent ima hiperhloremičnu metaboličku acidozu. Izračunati anjonski jaz u plazmi pod pretpostavkom da je normalan nivo albumina 15 mM, a anjonski jaz u urinu je -12 mM.
U uslovima acidoze, permeabilnost bioloških membrana se menja, neki od jona vodonika kreću se unutar ćelija u zamenu za jone kalijuma, koji se odvajaju od proteina u kiseloj sredini. Razvoj hiperkalemije u kombinaciji s niskim sadržajem kalija u miokardu dovodi do promjene njegove osjetljivosti na kateholamine, lijekovi i drugih uticaja. Kod nekompenziranog A. uočavaju se oštri poremećaji funkcije centralnog nervnog sistema. - vrtoglavica, pospanost, gubitak svijesti i izraženi poremećaji autonomnih funkcija.
Da li je moguće utvrditi kako je crijevo modificiralo urin da izazove poremećaje elektrolita i acidobazne ravnoteže. Jedan od njih zatim upoređuje urin prije nego što uđe u crijevo i nakon što izađe iz crijeva. Stoga će promjena u sastavu urina biti povezana s transportnim procesima između mjesta ulaska i izlaska. Međutim, ove pretpostavke vrijede samo ako postoji minimalno curenje urina iz crijeva u mjehur i minimalna kontaminacija iz tekućine iznad nivoa fistule.
Kliničke karakteristike i liječenje acidoze . Kliničke manifestacije kod svih oblika acidoze karakterišu sistemski funkcionalni poremećaji, uključujući depresiju centralnog nervnog sistema, oštećenje disanja, funkcije kardiovaskularnog sistema i mokrenja. Slična kršenja sa sve većom težinom toka osnovne bolesti mogu biti manifestacija drugih patoloških procesa, stoga je za pravovremeno otkrivanje A. potrebno poznavati bolest i patološka stanja pod kojim je moguć njen razvoj.
Kakav je uticaj tankog crijeva na sastav urina u odnosu na tretman vode?
Osim toga, aneurija u vrijeme uzimanja uzoraka sugerira da je malo vjerovatno značajno curenje dorzalne bešike u bešiku.
Možete li identificirati mjesto fistulizacije: proksimalni ileum ili jejunum
Tokom sljedećih sedmica naš pacijent je podvrgnut fistektomiji. Tokom operacije nađene su cementne adhezije u cijeloj trbušnoj šupljini i okolo zadnji zid balon kupole. Ove retroperitonealne adhezije su vjerovatno bile odgovorne za opstrukciju plućnog urinarnog trakta uočenu kod ovog pacijenta.Metabolička acidoza se najčešće javlja kod dekompenziranog dijabetes melitusa, dugotrajnog gladovanja (ketoacidoze), hipoksije bilo koje prirode, na primjer, kod kardiogenog šoka (uglavnom laktat- acidoza), uremija, zatajenje jetre, dijareja kod djece, trovanje kiselinom, posebno acetilsalicilnom kiselinom. K relativno rane manifestacije metabolički A. at hronične bolesti uključuju smanjenje učinkovitosti tekuće terapije (povećana tolerancija na srčane glikozide, antiaritmike, neke diuretike itd.). Karakteristični su poremećaji svijesti i aktivnosti bolesnika - od letargije, pospanosti i apatije do različitog stepena težine. koma, koji se pri pH vrijednosti manjoj od 7,2 uočava u gotovo svim slučajevima A. Kod ketoacidoze po pravilu dolazi do smanjenja tonusa skeletnih mišića, inhibicije tetivnih refleksa. Kod pacijenata s acidozom s uremijom često se otkrivaju mišićne fibrilacije. moguće su konvulzije uzrokovane hipokalcemijom. U akutnom ili brzoprogresivnom metaboličkom A., paralelno sa depresijom svijesti, bolesnik razvija više duboko disanje sa vidljivim učešćem respiratornih mišića; respiratorna pauza se skraćuje, zatim nestaje, protok vazduha u disajnim putevima se ubrzava, a disanje postaje bučno. Ovo takozvano veliko i bučno disanje je Kussmaulovo disanje (vidi sl. Dah) najčešće se opaža kod ketoacidoze i acidoze kod pacijenata sa uremijom. Istovremeno, važan klinički znak A. je miris zraka koji pacijent izdahne, koji podsjeća na miris trule jabuke kod ketoacidoze i miris amonijaka kod uremije (miris nestaje nakon uklanjanja acidoze). Sa značajnom depresijom centralnog nervnog sistema, posebno kod pacijenata sa teškom intoksikacijom, disanje može postati nekarakteristično za A. - površno, aritmično, dok se ovi mirisi obično primećuju. Priroda otkrivenih kardiovaskularnih poremećaja u velikoj mjeri ovisi o karakteristikama elektrolitnih poremećaja povezanih s acidozom. U većini slučajeva, krvni pritisak i minutni volumen se smanjuju; s nedostatkom natrijuma moguć je dehidracija, gubitak krvi kolaps .Često se opaža tahikardija, različiti poremećaji provodljivosti i srčanog ritma; uz hiperkalemiju (zatajenje bubrega) moguća je bradikardija. Diureza se u početku blago povećava, ali kod teške A., praćene padom krvnog tlaka, bilježi se oligurija, moguća je anurija, acidoza sa smanjenjem pH krvi ispod 6,8 je nespojiva sa životom.
Zbog narušene anatomije nije bilo moguće odrediti tačnu lokaciju fistulizacije, iako su hirurzi smatrali da se crijevni otvor nalazi u srednjem dijelu tankog crijeva. Na osnovu preoperativne evaluacije, i budući da fenotip elektrolitnih komplikacija nije odgovarao fenotipu bilo koje vrste prethodno opisanog curenja mokraće, moguće je da je naš pacijent imao mješoviti jejunalno-ilealni sindrom. Ovaj sindrom može nastati zbog fistulizacije mokraćne bešike u jejunumu, zbog čega urin dolazi u kontakt sa sluznicom i jejunuma i ileuma.
Gasna acidoza se uglavnom razvija hipoventilacijom pluća - najčešće opstruktivnim tipom respiratorna insuficijencija(kod pacijenata sa bronhiolitisom, sa egzacerbacijom hronični bronhitis, dugotrajni astmatični status), rjeđe sa "šok pluća", nepravilnim načinom vještačke ventilacije pluća. Kako se hiperkapnija povećava (vidi Razmjena plina) izgled pacijenta se mijenja: difuzna "siva" cijanoza zamjenjuje se "ružičastom", lice postaje natečeno, prekriveno velikim kapljicama znoja. Karakteristično je psihičko stanje bolesnika: u početku se primjećuju euforija, pričljivost, ponekad "ravni humor", kasnije - letargija, pospanost, koja prelazi u dublje poremećaje svijesti. Povećani minutni volumen daha postepeno se smanjuje; Pojava respiratorne aritmije ukazuje na značajnu inhibiciju respiratornog centra i smanjenje njegove osjetljivosti na CO 2 . Istovremeno, hipoksemija i hipoksija napreduju, što dovodi do metaboličke A. Zapažaju se tahikardija i srčane aritmije (često ventrikularna ekstrasistola). Uz neblagovremeno liječenje, razvija se respiratorna acidotična koma s relativno brzim smrtnim ishodom.
Na osnovu dostupnih informacija, možete predložiti patofiziološki lanac događaja koji su doveli do komplikacija koje je dao pacijent. Zanimljivo je i to da je u ovom slučaju crijevo moglo izvući dodatnu slobodnu vodu iz one nastale u bubregu, što je vjerovatno doprinijelo hipoosmolarnom poremećaju. Iz ovog jedinstvenog slučaja može se izvući nekoliko lekcija.
piće od limete
Slučaj predstavljen ovdje nudi jedinstven uvid u ulogu crijeva u obradi vode i elektrolita, kao iu patofiziologiju komplikacija urinarnog trakta. Međutim, važno je napomenuti da ova indirektna mjerenja mogu biti loša zamjena za direktna mjerenja. Rezultate anjonskog jaza u urinu i osmolarnog jaza treba tumačiti s oprezom. Autori se žele zahvaliti dr. Raymondu Gagnonu iz Opće bolnice u Montrealu na odličnim savjetima.
Potvrđeno je prisustvo acidoze laboratorijska istraživanja. Metaboličku A. karakteriše deficit puferskih baza (BE) koji prelazi 2,3 mmol/l, gasna acidoza - povećanje pCO 2 arterijske ili arterializirane kapilarne krvi (uzete iz zagrijane toplu vodu ili trljanjem prsta) iznad 45 mmHg Art. ili povećanje koncentracije CO 2 u izdahnutom zraku za 8% ili više. Ove promjene pri normalnim pH vrijednostima krvi ukazuju na kompenziranu fazu A., pri pH vrijednosti manjoj od 7,35 - o nekompenziranoj acidozi.
Evropsko udruženje za otkazivanja bubrega- Evropsko udruženje za dijalizu i transplantaciju. Bubrežna tubularna acidoza kod djece: suvremeni koncepti dijagnoze i liječenja. Bubrežna tubularna acidoza u djece: stanje tehnike, dijagnoza i liječenje.
Nedavno je otkrivena prekomjerna dijagnoza bubrežne tubularne acidoze kod meksičke djece, vjerovatno uz dijagnostičke greške i nedostatak molekularne i biohemijske patofiziologije bolesti. Često su dijagnostički kriteriji praćeni različitim simptomima kao što su anoreksija, poliurija, polidipsija, zastoj u rastu, rahitis, nefrokalcinoza, nefrolitijaza i rana ili kasna gluvoća.
Razvoj acidoze ukazuje na težinu osnovne bolesti, pa se takvi bolesnici moraju hitno hospitalizirati. Uz intenzivnu terapiju osnovne bolesti i uticaj na patogenetske mehanizme razvoja A. (davanje insulina kod dijabetičke ketoacidoze, terapija kiseonikom kod hipoksije i dr.), uz nekompenzovanu metaboličku acidozu, intravenski kap rastvora natrijum bikarbonata ili (sa zadržavanjem natrijuma u tijelu) provodi se rastvor trisamina. Kod gasa A., liječenje je prvenstveno usmjereno na obnavljanje plućne ventilacije upotrebom bronhodilatatora (ako je potrebno, glukokortikoidnih hormona), ekspektoransa, pozicione drenaže bronha i usisavanja sputuma iz respiratornog trakta. U slučaju dekompenzacije plinovite acidoze, hitno se provodi umjetna ventilacija pluća, zatim se uvode puferske otopine. Prije prebacivanja pacijenta na mehaničku ventilaciju, terapija kisikom i uvođenje natrijevog bikarbonata su kontraindicirani zbog opasnosti od zastoja disanja.
Ključne riječi: acidoza, bubrežna tubularna acidoza, transmembranski transporteri. Nedavno je otkrivena prevelika dijagnoza bubrežne tubularne acidoze kod meksičke djece, vjerovatno zbog dijagnostičkih grešaka, kao i nedostatka znanja o patofiziologiji i molekularnoj biohemiji uključenoj u EST bolest.
Bubrežna tubularna acidoza je patofiziološka promjena acidobaznog metabolizma koju karakterizira prisustvo hiperkloremične metaboličke acidoze uzrokovane renalnim gubitkom bikarbonata ili smanjenim izlučivanjem vodikovih jona putem bubrega. jedan.
Acidoza kod dece u osnovi ima iste razloge i Klinički znakovi kao kod odraslih. Međutim, kod djece rane godine postoji izražena sklonost ka A., posebno u neonatalnom periodu. To je zbog visokog intenziteta njihovih bioenergetskih procesa, ograničene funkcionalnosti bubrega i drugih organa i sistema uključenih u regulaciju acido-bazne ravnoteže.
Ovaj članak ima za cilj da izvještava o klasifikaciji, patofiziologiji, liječenju i liječenju zatajenja bubrega, kako bi uputio pedijatre i druge specijaliste u fiziološke osnove i složeni biohemijski procesi uključeni u ovu promjenu u acidobaznom metabolizmu.
U fiziološkim uslovima, ekstracelularni prostor se održava na alkalnom pH, sa uskim jazom od pH 40 ± 5 - malo naznaka prisustva slobodnih jona vodonika u navedenom tjelesnom prostoru, uprkos obilju vodonikovih jona koje tijelo svakodnevno prima kroz sposobnost bubrega da ih eliminira. Da bi se postigla acidobazna ravnoteža, uklanjanje vodonikovih jona mora biti jednako stopi proizvodnje koja se javlja tokom finog podešavanja u sabirnim kanalima. Sada, da bi bubrezi izlučili višak vodikovih jona u slobodnom obliku, biće potrebno smanjiti pH urina na 5, što se ne dešava jer će nastati nepopravljiva oštećenja tkiva urinarnog trakta.
Umjerena metabolička acidoza, uočena kod fetusa, svojevrsni je uvjet za njegov razvoj (povećava se otpornost fetusa na hipoksiju). Tokom normalnog porođaja, acidotični pomaci su blago pojačani zbog stimulacije anaerobne glikolize. Istovremeno, oni, zajedno sa drugim faktorima, izazivaju iritaciju respiratornog centra djeteta koje se rodi. Nakon porođaja pH vrijednosti krvi novorođenčadi fluktuiraju u rasponu od 7,24-7,38, što ukazuje na nestabilnost homeostatskih mehanizama za regulaciju ravnoteže kiselina i baza. Deficit potonjeg (BE) je (-4)-(-12) mmol/l. Krajem prvog - početkom drugog dana života novorođenčadi uočava se respiratorna kompenzacija acidoze, a pH vrijednosti prelaze 7,36. U narednih 3-5 dana pokazatelji acidobazne ravnoteže se po pravilu približavaju onima kod odraslih. Stepen postnatalne fiziološke acidoze određen je tokom i trajanjem porođaja (laktatemija), anestezijom i analgezijom, vremenom podvezivanja pupčane vrpce, brzinom adaptacije disanja i cirkulacije i temperaturom okoline. U nepovoljnim uslovima porođaja, novorođenčad razvija nekompenzovanu metaboličku acidozu, koja može biti mešovite (metaboličke i respiratorne) prirode. Prema njegovoj ozbiljnosti, uočava se jedna ili druga simptomatologija. Opasnost po život novorođenčeta nastaje kada pH padne ispod 7,0; u ovom slučaju ga može spasiti samo brz i energičan tretman.
Međutim, u fiziološkim uslovima, urin sadrži kiseli pH stabilan sa slobodnim jonima vodika koji vezuju molekule amonijaka za pufer, a zatim formiraju amonijum i izlučuju se ovim putem. Osim toga, slobodni joni vodika vezuju se za fosfate i sulfate.
Hiperkloremijska metabolička acidoza: značaj i ograničenja u korištenju Stewartovog modela
Izmjerena u urinu posljednja dva naziva se titrabilna kiselost. Defekt je lociran u konektoru tubula, početnom zaglavlju i vanjskoj kortikalnoj i medularnoj zbirci. Može biti sporadično ili genetski. Zauzvrat, genetski se prenosi autosomno dominantno ili recesivno. Neke od navedenih promjena predstavljaju rizik od napredovanja do terminalne uremije, kao što su tirozinemija i cistinoza. 11. Primarno se javlja uglavnom kod male djece i može biti sporadično ili naslijeđeno.
Kod „zdravih“ prevremeno rođenih beba, zbog nezrelosti organa i sistema, regulatorni hemostatski mehanizmi su još nesavršeniji. Kod njih se, češće nego kod donošenih, u prvim danima života uočava dekompenzacija acidoze, za koju se kaže da je pri pH nižoj od 7,32. Negativne BE vrijednosti (ispod - 3 mmol/l) ukazuju na metaboličke, visoke vrijednosti pCO 2 (više od 6,65 kPa - 50 mmHg Art.) - o respiratornoj prirodi acidoze. Jačanje metaboličke komponente acidoze u 2-4. nedelji života - kasno tzv. acidoza nedonoščad se češće opaža kod djece rođene s malom tjelesnom težinom koja ne odgovara gestacijskoj dobi. Razlozi za to nisu samo nezrelost, već i vještačko hranjenje namirnicama s visokim sadržajem proteina ili isključivo kiselo-mliječnim smjesama, značajan gubitak težine nakon porođaja i kasni početak hranjenja.
Kod novorođenčadi, posebno u nedonoščadi, prvi i najpatognomoničniji znak acidoze - veliko toksično disanje - obično se ne pojavljuje. Kod metaboličke acidoze ona postaje nepravilna, nepravilna u njima. Periodično disanje, karakteristično za male i prijevremeno rođene bebe, odlikuje se produženim periodi apneje(preko 5-7 sa). Kod respiratornog distres sindroma, praćenog teškim mješovitim tipom acidoze, paradoksalno disanje - asinkroni pokreti dijafragme (trbušnih mišića) i respiratornih (interkostalnih) mišića.
Postoje dokazi da su novorođenčad otpornija na acidozu od odraslih. Kod nedonoščadi se mogu odvijati višesmjerne reakcije okoline u krvnoj plazmi i unutar stanica ( acidoza-alkaloza). Kod zdravih odraslih osoba ovaj fenomen se ne opaža, a kao kompenzacijski mehanizam počinje djelovati samo u uvjetima teške patologije. Istovremeno, kako dijete raste, dolazi do formiranja adaptivnih sposobnosti i puferskih svojstava krvi i tkiva. Dakle, puferski kapacitet krvi kod djece dostiže vrijednosti odraslih tek u periodu puberteta.
U dojenčadi i starijoj dobi, kritične granice poremećaja acido-bazne ravnoteže također su određene stepenom promjene pH vrijednosti krvi. U akutnoj toksikozi, smanjenje pH na 7,25-7,20 dovodi do spazma krvnih žila plućne cirkulacije, praćeno insuficijencijom šant-difuzije i razvojem velikog toksičnog disanja; pri nižim pH vrijednostima (do 7,0) primjećuje se spazam arteriola bubrežnih glomerula, dolazi do kome; pri pH 6,9 dolazi do oštre inhibicije kontraktilnosti miokarda (energetsko-dinamička insuficijencija prema Hegglinu), toksično disanje nestaje; pri pH 6,6, moždana kora odumire (EEG signali su odsutni). Daljnji pad pH krvi nije kompatibilan sa životom.
Među nasljednim oblicima metaboličke patologije koje karakterizira teška metabolička acidoza, posebno mjesto zauzimaju urođene laktatne acidoza, koja je, za razliku od uobičajene laktacidoze povezane s oštećenjem tkiva kisikom ili opskrbom krvlju (na primjer, u šoku), uzrokovana defektima ključnih enzima glukoneogeneze ili katabolizma piruvata.
Liječenje acidoze kod djece treba biti sveobuhvatno i uključivati eliminaciju etiološkog faktora, korekciju disanja, hipovolemije, poremećaja elektrolita; normalizacija poremećene cirkulacije krvi; poboljšanje reoloških svojstava krvi, oksidativnih procesa tkiva; eliminacija hipoproteinemije, anemije itd. Zatim se propisuju alkalne otopine.
Za korekciju subkompenzirane metaboličke acidoze kod djece (pH 7,35-7,30) koriste se kokarboksilaza hidrohlorid, riboflavin mononukleotid, rastvor nikotinske kiseline, rastvor glutaminske kiseline, natrijum bikarbonat. Natrijum bikarbonat je uključen u oralnu rehidratacionu so, predloženu za oralnu rehidrataciju kod akutnih gastrointestinalnih bolesti. Djeci starijoj od 6-8 godina može se propisati otopina dimefosfona; lijek se koristi za akutne i egzacerbacije kronične bronhopulmonalne patologije, dijabetes melitusa, bolesti sličnih rahitisu itd. Dimefosfon može uzrokovati dispeptične poremećaje.
Liječenje teške, nekompenzirane metaboličke acidoze (pH 7,29 i niže) Zahtijeva obaveznu infuzionu alkalizirajuću terapiju (obično rastvor natrijum bikarbonata, koji se određuje Astrup formulom). Trisamin se koristi za ograničavanje unosa natrijuma prilikom korekcije acidoze natrijum bikarbonatom. U poređenju sa natrijum bikarbonatom, trisamin je dobar diuretik, ima jače alkalizirajuće dejstvo i u većoj meri smanjuje nivo pCO 2. Prikazuje se pri pH od oko 7,0. Međutim, kod novorođenčadi, posebno kod prijevremeno rođenih beba, ne preporučuje se upotreba, jer. deprimira disanje, izaziva intracelularni alkalizirajući efekat, predisponira hipoglikemiji i hipokalemiji. Rastvor natrijevog laktata, koji je ranije bio naširoko promoviran kao sastavni dio Darrowove mješavine, ne bi se trebao koristiti kao baza kod djece. Za liječenje laktacidoze koristi se dikloroacetat koji aktivira enzimski kompleks piruvat dehidrogenaze, kao i preparati lipoične kiseline, karnitin.
Prilikom propisivanja antiacidotika neophodna je stroga kontrola indikatora acido-bazne ravnoteže uz istovremeno određivanje jonograma. Kod metaboličke acidoze, koja je rezultat brzo razvijajućih patoloških procesa, rizik od komplikacija od alkalizirajućih otopina veći je od koristi od brze normalizacije pH krvi. Prije svega, ovo se odnosi na malu djecu. dakle, intravenozno davanje kokarboksilaza, koja ima blagi alkalizirajući učinak, može uzrokovati iznenadni srčani zastoj. Hipertonične otopine natrijevog bikarbonata, koje dovode do hipernatremije i hiperosmolarnosti krvne plazme, mogu doprinijeti razvoju intrakranijalnih krvarenja, posebno kod nedonoščadi.
Mlazno davanje ovih otopina može uzrokovati metaboličku alkalozu, što rezultira smanjenjem sadržaja joniziranog kalcija u krvi, praćeno tetanijom i apnejom. Stoga je kod novorođenčadi preporučljivo korigirati acidozu otopinom natrijum bikarbonata. Liječenje gasovite acidoze provodi se prema principima liječenja respiratorna insuficijencija. Pravovremeno započetim i sistematski sprovedenim tretmanom moguće je osigurati normalan razvoj djeteta.
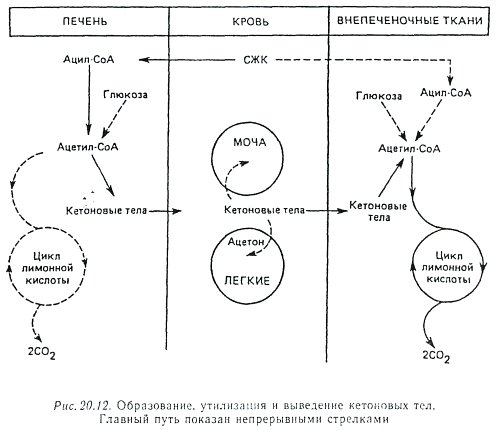
Tampon i fiziološki mehanizmi Obično održavaju konstantnu pH vrijednost krvi. Neravnoteža između formiranja i (ili) uklanjanja vodikovih iona, kada se gore navedeni mehanizmi za stabilizaciju njegove koncentracije ne nose u potpunosti sa situacijskim opterećenjem, dovodi do smanjenja ili povećanja pH. U prvom slučaju (sa smanjenjem pH) stanje se naziva acidoza. U drugom - (sa povećanjem pH) stanje se naziva alkaloza. I acidoza i alkaloza mogu biti metaboličke ili respiratorne prirode (slika 20.11).
metabolička acidoza
Metaboličku acidozu karakteriziraju metabolički poremećaji koji dovode do nekompenziranog ili djelomično kompenziranog smanjenja pH krvi.
Metabolička acidoza nastaje zbog:
- Prekomjerna primjena ili stvaranje perzistentnih kiselina (masovne transfuzije krvi, stvaranje velike količine keto kiselina za vrijeme gladovanja i dijabetesa, pojačano stvaranje mliječne kiseline u šoku, pojačano stvaranje sumporne kiseline pri pojačanom katabolizmu, intoksikacije itd.).
- Prekomjerni gubitak bikarbonata (proljev, ulcerozni kolitis, fistule tanko crijevo, duodenum, oštećenje proksimalnih bubrežnih tubula u akutnom i kroničnom obliku inflamatorne bolesti bubrezi).
- Nedovoljno uklanjanje perzistentnih kiselina (smanjenje glomerularne filtracije kod kronične bubrežne insuficijencije, s oštećenjem bubrežnog epitela itd.).
- Višak koncentracije ekstracelularnog kalija, koji se aktivno apsorbira u unutarćelijskom prostoru u zamjenu za vodikove ione.
Brojne varijante metaboličke acidoze popraćene su kršenjem normalnog omjera između glavnih ekstracelularnih iona - natrijuma, klora i bikarbonata, što utječe na vrijednost indeksa električne neutralnosti krvi - anionski jaz.
Anionski jaz, promjena njegovih vrijednosti na razne vrste metabolička acidoza
Natrijum, hlorid i bikarbonat su glavni anorganski elektroliti u ekstracelularnoj tečnosti. Uz uravnotežen metabolizam, koncentracija natrijuma premašuje zbir koncentracija klorida i bikarbonata za 9-13 mmol/l. Pri pH vrijednosti od 7,4, proteini krvne plazme imaju pretežno negativan naboj, što osigurava jaz između kationskog i anjonskog naboja - natrijuma i količine klorida i bikarbonata, respektivno, za 9-13 mmol / l. Ovaj jaz se naziva anjonski jaz. Gore navedeni uzroci metaboličke acidoze mogu se podijeliti na one koji povećavaju i ne povećavaju anionski jaz (tabela 20.2). [prikaži] ).
| Tabela 20.2. Priroda promjene vrijednosti anjonskog jaza pri razne opcije metabolička acidoza | |
| Uzrok | anionski jaz |
| I. Prekomjerno unošenje i (ili) stvaranje postojanih kiselina: | |
| 1. Ketoacidoza | |
| 2. Laktacidoza | |
| 3. Opijenost: | |
| salicilate | |
| etilen glikol | |
| metanol | |
| paraldehid | |
| amonijum hlorid | N |
| II. Višak gubitka HCO 3 - | |
| 1. Gastrointestinalni: | |
| dijareja i fistule | N |
| kolestiramin | N |
| ureterosigmoidostomija | N |
| 2. Bubrežni: | |
| otkazivanja bubrega | N |
| bubrežna tubularna acidoza (proksimalna) | N |
| III. Nedovoljno izlučivanje endogenog H+ | |
| 1. Smanjena proizvodnja NH3: zatajenje bubrega | ili N |
| 2. Smanjeno lučenje H+: | |
| bubrežna tubularna acidoza (distalna) | N |
| hipoaldosteronizam | N |
| - povećava se anjonski jaz; N - anjonski jaz se ne mijenja. | |
Određivanje vrijednosti anionskog jaza može se obaviti kao prvi korak diferencijalna dijagnoza metabolička acidoza.
Gubitak natrijum bikarbonata kroz gastrointestinalni trakt ili bubrege rezultira zamjenom ekstracelularnih bikarbonata hloridima (ekvivalentnim ekvivalentima) koje zadržavaju bubrezi zajedno s natrijem ili dolaze iz intracelularnog prostora. Ova vrsta acidoze, koja rezultira povećanjem koncentracije hlorida u plazmi, naziva se hiperhloremična acidoza. Naprotiv, ako se H + akumulira s bilo kojim jonom osim klorida, ekstracelularni bikarbonati će biti zamijenjeni neizmjerenim anionima (A -):
ON + NaHCO 3 --> NaA + H 2 CO 3 --> CO 2 + H 2 O + NaA
Kao rezultat toga, ukupna koncentracija klorida i bikarbonatnih jona će se smanjiti zbog povećanja anionskog jaza zbog akumulacije neizmjerenih aniona.
Kod acidoze sa povećanim anionskim jazom, specifična patološki procesčesto se nalazi pri određivanju koncentracije dušika ureje u serumu, kreatinina, glukoze, laktata i piruvata i proučavanju seruma na prisustvo ketona do toksičnih spojeva (salicilati, ponekad metanol ili etilen glikol). Slično promjeni vrijednosti anjonskog jaza, dolazi do povećanja vrijednosti osmotskog jaza, o čemu se detaljnije govori u dijelu o osmometriji.
Povećanje anionskog jaza ponekad se opaža kod respiratorne alkaloze, kada je povećana proizvodnja mliječne kiseline. U nastavku ćemo analizirati patobiohemijske mehanizme promjene vrijednosti anionskog jaza u kombinaciji s varijacijama drugih pokazatelja u različitim varijantama acidobaznih poremećaja.
Prekomjerna primjena i/ili stvaranje postojanih kiselina
Povećanje koncentracije vodikovih jona može biti uzrokovano širokim spektrom razloga, među kojima je najčešći disbalans između proizvodnje i iskorištavanja ketonskih tijela, mliječne kiseline, trovanja raznim tehničkim tekućinama, lijekovima, alkoholom. Patobiohemijski obrasci razvoja acidoze u svakom konkretnom slučaju imaju niz fundamentalnih karakteristika o kojima se govori u nastavku.
Prekomjeran gubitak HCO 3 bikarbonata - kroz gastrointestinalni trakt
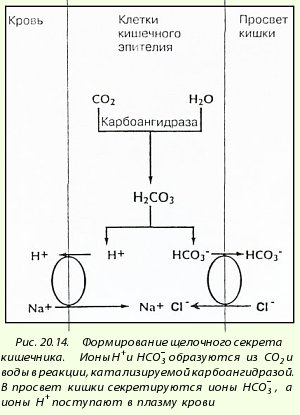
Tajne crijeva, uključujući pankreasnu i bilijarnu, imaju alkalno okruženje. Alkalnu reakciju crijevnog sekreta osigurava bikarbonat (HCO 3 -), koji nastaje kao rezultat reakcije između vode i ugljičnog dioksida u stanicama crijevnog epitela (slika 20.14).
Uklanjanje pankreasnog, bilijarnog ili crijevnog sekreta kroz crijevnu fistulu ili tijekom dijareje dovodi do gubitka bikarbonata, kompenzacijskog za njegovu proizvodnju u stanicama crijevnog epitela, što je, shodno tome, praćeno izlučivanjem vodikovih jona u krv i može dovesti do metaboličke acidoze.
Jedna od metoda liječenja pacijenata s gubitkom funkcije mjehura je implantacija uretera u sigmoid ili ileum. U ovoj situaciji može postojati hiperhloremična acidoza ako je vrijeme kontakta između urina i crijeva dovoljno za apsorpciju hlorida u urinu u zamjenu za bikarbonatne jone. Dodatni faktori metaboličke acidoze u ovim uslovima su apsorpcija NH4+ od strane crevne sluznice i bakterijski metabolizam uree u debelo crijevo sa formiranjem apsorbirajućeg H + . Implantacija uretera u kratku petlju ileuma čini razvoj metaboličke acidoze rjeđim smanjenjem vremena kontakta između crijevne sluznice i urina.
Nedovoljno izlučivanje endogenog H+ putem bubrega
Nedovoljno izlučivanje endogenog H+ bubrezima javlja se kod bolesti (lezija) bubrega, koje su praćene ili smanjenjem broja funkcionalno aktivnih nefrona kod kronične bubrežne insuficijencije (CRF) ili oštećenjem tubularnog aparata nefrona. Uzimajući u obzir osobitosti bolesti bubrega, razmotrit ćemo mehanizme razvoja metaboličke acidoze kod kroničnog zatajenja bubrega i oštećenja tubularnog aparata.
Metabolička acidoza kod kroničnog zatajenja bubrega
Metabolička acidoza se često dijagnosticira kod pacijenata sa kasne faze hronično zatajenje bubrega. Kod takvih pacijenata mogu se razlikovati tri klinički različita tipa metaboličke acidoze:
- povećana acidoza anjonskog jaza [prikaži]
Acidoza sa povećanim anjonskim jazom
Smanjenje ukupnog izlučivanja vodikovog jona (H +) kod kronične bubrežne insuficijencije nastaje uglavnom zbog smanjenja izlučivanja amonijaka (NH 4 +), koji se razvija kao rezultat kršenja procesa amoniogeneze. Izlučivanje titrabilnih kiselina i reapsorpcija bikarbonata su očuvanije funkcije kod kronične bubrežne insuficijencije od izlučivanja NH4+.
Smanjenje broja funkcionalnih bubrežnih glomerula dovodi do povećanja intenziteta proizvodnje amonijaka funkcionalno aktivnim bubrežnim glomerulima. Dakle, kod hronične bubrežne insuficijencije primećuje se povećanje količine izlučenog amonijaka, ali je ispod nivoa potrebnog za uklanjanje dnevne endogene proizvodnje H+. O stepenu insuficijencije proizvodnje amonijaka u bubrezima može se suditi po vrijednosti amonijevog koeficijenta, koji karakterizira intenzitet amoniogeneze. Izračunava se kao omjer E NH 4 + /E H + ili E NH 4 + /E TK (E NH 4 + - dnevno izlučivanje amonijum jona, E H + i E TK - dnevno ukupno izlučivanje vodikovih jona i titriranih kiselina, odnosno). Uz uravnotežen metabolizam kod zdravih osoba, u prosjeku, E NH 4 + /E H + = 0,645, E NH 4 + / E TK = 1,0-2,5. Kako napredujete bolest bubrega smanjenje intenziteta stvaranja amonijaka u ćelijama epitela tubula nadmašuje brzinu smanjenja izlučivanja vodikovih iona, što dovodi do smanjenja vrijednosti amonijum koeficijenta. Povećanje omjera E NH 4 + /E H + > 0,645 opaženo je u pozadini terapije kortikosteroidima i praćeno smanjenjem izlučivanja titriranih kiselina.
Zbog nesposobnosti tubularnih epitelnih stanica patološki izmijenjenih bubrega da adekvatno povećaju proizvodnju NH 3, određena količina organskih kiselina koje se dnevno formiraju mora se puferirati na drugačiji način, posebno zbog kiselina koje se izlučuju u neutralnom obliku (" titrabilne kiseline).
Titrabilna kiselost kod kroničnog zatajenja bubrega održava se na vrijednostima bliskim normalnim sve dok se ne ograniči unos fosfata iz hrane. U uslovima smanjenja količine fosfata filtriranih u tubularni fluid smanjuje se izlučivanje titriranih kiselina. Normalno, smanjenje izlučivanja titrabilnih kiselina treba nadoknaditi povećanjem sinteze NH 4 +, pa se stoga ukupno izlučivanje vodikovog jona ne mijenja. Kod kronične bubrežne insuficijencije, biosinteza NH 4 + je blago povećana, a smanjenje izlučivanja titrabilnih kiselina dovodi do smanjenja ukupnog oslobađanja vodikovog jona.
Kod kroničnog zatajenja bubrega dolazi do smanjenja sposobnosti zahvaćenog nefrona ne samo da luči ione vodika, već i da reapsorbuje bikarbonat. Da, u normalan nivo bikarbonata u plazmi kod pacijenata s kroničnim zatajenjem bubrega, reakcija urina je alkalna, što ukazuje na nepotpunu apsorpciju HCO 3 -. Nivo bikarbonata u plazmi koji se vidi kod acidoze (obično 12-20 mmol/L) odgovara kapacitetu reapsorpcije nefrona. Gotovo potpuna reapsorpcija HCO 3 iz tubularne tekućine u ovim uvjetima je dokazana kiselom reakcijom urina.
Acidoza kod hroničnog zatajenja bubrega obično se razvija u kasnijim stadijumima bolesti (brzina glomerularna filtracija jednako 25 ml/min).
U tim uslovima, zadržavanje anjona neorganskih kiselina, kao što su fosfati i sulfati, doprinosi povećanju anjonskog jaza. Acidozu kod kroničnog zatajenja bubrega često karakterizira povećani anionski jaz.
- hiperhloremična acidoza sa normokalemijom [prikaži]
Hiperhloremična acidoza sa normokalemijom
Kod kronične bubrežne insuficijencije zbog bolesti koje zahvaćaju intersticij bubrega, kao što su hiperkalcemija, medularna cistična bolest ili intersticijski nefritis, acidoza se razvija uglavnom zbog smanjenja stvaranja NH 3 za više od rana faza bolesti (sa višom brzinom glomerularne filtracije) nego kod drugih oblika kroničnog zatajenja bubrega. To je, očigledno, zbog dominantnog kršenja tubularnih funkcija, dok je brzina glomerularne filtracije više očuvana. U takvoj situaciji, brzina glomerularne filtracije je dovoljno visoka da spriječi značajnu akumulaciju različitih anjona kiseline. Lučenje kalija u bubrezima blago pati zbog kontinuirane aktivnosti mehanizma acidogeneze. U ovom slučaju, hiperhloremična acidoza se razvija s normokalemijom.
- hiperhloremična acidoza sa hiperkalemijom [prikaži]
Hiperhloremična acidoza sa hiperkalemijom
Hiperkloremična metabolička acidoza kod kronične bubrežne insuficijencije može se razviti u pozadini hiperkalijemije ako je njen uzrok smanjenje lučenja kalija od strane zahvaćenog bubrega. U ovoj skupini pacijenata često se opaža hiporenemija, hipoaldosteronizam i (ili) smanjenje afiniteta tubularnih epitelnih stanica za aldosteron. Poremećaji metabolizma aldosterona i (ili) reakcije na njega dovode do smanjenja lučenja kalija u bubrezima i hiperkalemije. Hiperkalijemija dodatno otežava izlučivanje kiseline zbog inhibicije stvaranja amonijaka iz glutamina. Hipoaldosteronizam također može smanjiti lučenje H+ i doprinijeti razvoju metaboličke acidoze. Koji faktor je dominantan u patogenezi metaboličke acidoze kod ovih pacijenata, hipoaldosteronizam ili smanjenje stvaranja NH 3 zbog oštećenja tubularnog epitela, nije jasno. Međutim, pH im se obično smanjuje na 5,5 ili niže, što ukazuje da je patogeneza acidoze u ovom slučaju karakterizirana smanjenjem sposobnosti lučenja H+, ali očuvanjem sposobnosti zakiseljavanja urina.
Potreba za liječenjem acidoze kod kronične bubrežne insuficijencije javlja se kada ona postane teška (pH< 7,2, [НСО 3 - ] < 15 ммоль/л).
Metabolička acidoza u bubrežnim tubulima
Funkcionalna specijalizacija stanica u različitim dijelovima bubrežnih tubula osigurava razvoj reakcija amoniogeneze u proksimalnom dijelu tubula, acidogenezu i metabolizam kalija u njihovom distalnom dijelu, određuje patogenezu acidobaznih poremećaja kod različitih ozljeda (bolesti) tubularni aparat. Prema prirodi promjene vrijednosti indikatora kiselinsko-baznog stanja i koncentracije kalija u krvnoj plazmi, razlikuju se sljedeće varijante bubrežne tubularne acidoze (RCA):
- bubrežna tubularna acidoza zbog malapsorpcije bikarbonata iz tubularne tekućine (proksimalni RCA) [prikaži]
Proksimalna bubrežna tubularna acidoza (proksimalni RCA)
Proksimalna bubrežna tubularna acidoza nastaje zbog nedovoljne reapsorpcije filtriranog bikarbonata iz tubularne tekućine bez narušavanja mehanizma acidifikacije urina. Slično stanje se razvija kod dominantne lezije (bolesti) proksimalnog tubularnog aparata, gdje se, uz normalnu funkciju bubrega, oko 85% filtrirane količine bikarbonata reapsorbira iz tubularne tekućine, ako njegova koncentracija u glomerularnom filtratu ne prelazi 26 mmol / l (od ove količine, cjevasti aparat u cjelini pruža reapsorpciju više od 99% HCO 3 -). Ako bikarbonat u plazmi pređe ovu razinu, počinje se pojavljivati u urinu.
Kod pacijenata sa proksimalnim RKA dolazi do smanjenja reapsorpcije bikarbonata u proksimalnim bubrežnim tubulima, što dovodi do njegovog pojačanog ulaska u distalne tubule, gdje je reapsorpcija HCO 3 vrlo mala. Kao rezultat toga, nereapsorbirani bikarbonat se izlučuje urinom. Nedovoljna reapsorpcija bikarbonata, odnosno njegov smanjeni povratak u krv, dovodi do smanjenja omjera bikarbonat/karbonska kiselina (HCO 3 - /H 2 CO 3) u krvnoj plazmi. Pri normalnom pH krvi, odnos HCO 3 - /H 2 CO 3 je 20:1. Povećanje udjela kisele komponente u bikarbonatnom pufer sistemu krvi dovodi do toga da HCO 3 - /H 2 CO 3 postaje manji od 20:1, što je tipično za nižu pH vrijednost. U odnosu na acido-bazno stanje, to znači manifestaciju metaboličke acidoze.
Pad kapaciteta reapsorpcije bikarbonata u proksimalnom bubrežnom tubulu uzrokuje smanjenje maksimalnog kapaciteta reapsorpcije sa normalne vrijednosti od 26 mmol/l na novu, više nizak nivo. Ako, međutim, smanjenje koncentracije bikarbonata u krvnoj plazmi ne utječe na omjer HCO 3 - / H 2 CO 3 zbog kompenzacijskih reakcija iz respiratornog sistema i intracelularnog prostora, onda će smanjenje količine reapsorbiranog bikarbonata rezultirati smanjenjem puferskog kapaciteta bikarbonatnog puferskog sistema krvi.
Sljedeći uvjetni proračuni pomažu u ilustraciji novi nivo uspostavljanje ravnoteže u bikarbonatnom pufer sistemu. Pretpostavimo da je prag tubularne reapsorpcije bikarbonata smanjen sa 26 na 13 mmol/l glomerularnog filtrata. U ovim uslovima, bikarbonat će se gubiti u urinu sve dok koncentracija u plazmi ne padne na 13 mmol/l, što će dovesti do novog stabilnog stanja, kada će se sav filtrirani bikarbonat reapsorbovati iz tubularne tečnosti. Ako je odnos HCO 3 - /H 2 CO 3 u bikarbonatnom puferskom sistemu krvi postavljen na 20:1, tada će sistem bikarbonatnog pufera stabilizovati pH na vrednosti od 7,4, ali će njegov puferski kapacitet biti smanjen za 2 puta.
Dakle, proksimalni RCA je patologija u kojoj se koncentracija bikarbonata u krvnoj plazmi postavlja na vrijednosti ispod normalne. Sa novim nivoom bikarbonata u krvnoj plazmi, njegova reapsorpcija će biti potpuna. Drugim riječima, bubrežni mehanizmi su u stanju da povrate bikarbonat koji se koristi za dnevno titriranje organskih kiselina, a reakcija urina će biti kisela.
Ako se bikarbonat daje pacijentima s proksimalnim RCA, stvarajući koncentraciju u plazmi iznad utvrđenog praga reapsorpcije u bubrezima, tada će reakcija urina postati alkalna. Korekcija metaboličke acidoze kod pacijenata sa proksimalnim RCA ima posebnost da zahteva velike, u poređenju sa drugim tipovima metaboličke acidoze, količine bikarbonata neophodne za formiranje njegove dovoljne koncentracije u krvnoj plazmi.
Osim defekta u reapsorpciji bikarbonata, pacijenti s proksimalnim RCA često imaju i druge proksimalne tubularne disfunkcije. Tako se kod pacijenata s proksimalnim RCA često kombiniraju defekti u reapsorpciji fosfata, mokraćne kiseline, aminokiselina i glukoze. Kao što je objašnjeno u nastavku, proksimalni RCA može biti uzrokovan raznim poremećajima. U mnogim stanjima, posebno onim toksičnog ili metaboličkog porijekla, kapilarni defekt se može preokrenuti u liječenju osnovne bolesti. Uzrok tubularne disfunkcije u ovim slučajevima nije utvrđen.
Uzroci proksimalnog RCA:
- Primarni - nasljedni ili sporadični
- cistinoza
- Wilsonova bolest
- hiperparatireoza
- Poremećaji metabolizma proteina zbog nefrotskog sindroma, multiplog mijeloma, Sjogrenovog sindroma, amiloidoze
- Medularna cistična bolest
- transplantacija bubrega
- Reception diakarba
- distalna bubrežna tubularna acidoza (distalni RCA) [prikaži]
Distalna bubrežna tubularna acidoza (distalni RCA)
Razvoj distalne bubrežne tubularne acidoze povezan je s dominantnim smanjenjem sekrecije H+ u distalnom tubularnom aparatu bubrega. Reapsorpcija bikarbonata u distalnom RCA je u granicama normale.
Smanjenje lučenja H+ u distalnom nefronu može biti uzrokovano više razloga, među kojima su najčešći:
- niska sekrecija H + u distalnom nefronu;
- povećanje permeabilnosti ćelija epitela distalnog nefrona za H + i, kao rezultat toga, njegov aktivni povratak duž gradijenta koncentracije od lumena tubula u ćelije ili ekstracelularni prostor (postojanje gradijenta koncentracije nastaje zbog izlučivanja H+ u tubularnu tečnost, što obezbeđuje višak jona vodonika u njoj u odnosu na tečnost ćelijskog i ekstracelularnog prostora).
Smanjenje koncentracije vodikovih iona u tubularnoj tekućini dovodi do smanjenja efikasnosti procesa redukcije HCO 3 i smanjenja količine reapsorbiranog bikarbonata i povećanja njegove količine izlučene urinom. Normalna filtracija bikarbonata i njegov smanjeni unos iz tubularne tečnosti u distalnom dijelu nefrona manifestuje se nesposobnošću tubularnog aparata da smanji pH urina na manje od 5,3 (minimalni normalni pH urina je 4,5-5,0).
Prekomjerno izlučivanje bikarbonata urinom i, naprotiv, nedovoljno zakiseljavanje mokraće, smanjuju doprinos bubrežnih mehanizama za stabilizaciju pH krvi kompenzacijskim reakcijama tijela kad god se poveća sadržaj nehlapljivih kiselina u plazmi.
Višak vodikovih jona u krvi može se neutralizirati primjenom natrijum bikarbonata (NaHCO 3). Doza bikarbonata potrebna za to je ekvivalentna dnevnom ne-izlučenom opterećenju nehlapljivih kiselina. Ova količina HCO 3 - , u pravilu je manja od one koja je potrebna za ispravljanje metaboličke acidoze u slučaju oštećenja (bolesti) proksimalnog tubula.
Distalni PCL često dovodi do razvoja nefrolitijaze, nefrokalcinoze i zatajenja bubrega zbog taloženja soli kalcijum fosfata u medularnoj regiji bubrega. Patogeneza razvoja nefrokalcinoze je dvostruka. Prvo, zbog stalno visokog pH urina (5,5 ili više), bubrežno izlučivanje citrata je smanjeno. Citrat je glavni inhibitor taloženja kalcijuma u urinu jer kelira ione kalcija u molarnom odnosu 4:1. Drugo, zbog dnevnog ukupnog pozitivnog balansa H+ kod pacijenata sa distalnim PCL-om, koštani karbonati se koriste kao glavni pufer za neutralizaciju dnevnog opterećenja organskim kiselinama, što dovodi do hiperkalciurije i daljeg pogoršanja nefrokalcinoze.
Distalni PCL treba razmotriti kod svakog pacijenta s metaboličkom acidozom i upornim pH urina iznad 5,5. U diferencijalnom dijagnostičkom planu treba isključiti leziju urinarnog trakta mikroorganizmi koji razgrađuju ureu u alkalizirajuće produkte urina, i proksimalni PCL, u kojem filtrirana količina plazma bikarbonata premašuje sposobnost tubula da je reapsorbuje.
- bubrežna tubularna acidoza zbog poremećene acidifikacije urina u kombinaciji s hipokalemijom
Proksimalni i distalni LCL mogu se razlikovati prema prirodi promjene pH urina do bikarbonatnog opterećenja. U bolesnika s proksimalnim RCA pH urina se povećava uvođenjem bikarbonata, ali to se ne događa kod pacijenata s distalnim RCA.
U slučaju acidoze blagi stepen može se izvršiti test sa amonijum hloridom (NH 4 Cl) koji se primenjuje u količini od 0,1 g/kg. Unutar 4-6 sati koncentracija bikarbonata u krvnoj plazmi se smanjuje za 4-5 mmol/l. pH urina kod pacijenata sa distalnim PCL-om će ostati iznad 5,5 uprkos smanjenju bikarbonata u plazmi. Međutim, u proksimalnom RCA (i u zdravi ljudi) pH urina pada na vrijednosti manje od 5,5, a obično ispod 5,0.
Defekt acidifikacije u distalnom RCA ne dovodi uvijek do metaboličke acidoze. Pacijenti s defektom acidifikacije urina zbog disfunkcije distalnog tubula, ali s normalnom koncentracijom bikarbonata u plazmi, imaju tzv. nepotpunu distalnu RCA. pH urina im je stalno povišen, ali nema metaboličke acidoze. Ovo stanje se održava povećanjem stvaranja amonijaka u ćelijama tubularnog epitela, što dovodi do povećanja vezivanja i uklanjanja vodikovih jona u sastavu amonijum jona, uprkos povećanom pH urina. Zašto takvi pacijenti mogu imati povećanu proizvodnju NH3, za razliku od pacijenata sa potpunim distalnim PCL, nije sasvim jasno.
Komorbiditet kod pacijenata sa nepotpunim distalnim PCL je sličan onome kod distalnog PCL - hiperkalciurija, nefrokalcinoza, nefrolitijaza i nisko izlučivanje citrata u urinu.
Natriurija, kaliurija i često hipokalemija nalaze se i u distalnom i u proksimalnom RCA. Međutim, mehanizmi ovih poremećaja imaju svoje karakteristike u svakoj vrsti PKA. Tako je analizom promjena u izlučivanju natrijuma, kalija i aldosterona tokom alkalne pH korekcije kod pacijenata sa distalnim RCA utvrđeno smanjenje izlučivanja putem bubrega. Ovi rezultati sugeriraju da se renalna deplecija natrijuma i kalija kod pacijenata s distalnim RCA razvija zbog smanjenja ukupne izmjene Na + H + u distalnom tubulu, što ograničava postizanje gradijenta koncentracije H + između tubularnog lumena i peritubularnog. svemir. Smanjenje kursa Na + H + dovodi do kompenzacionog povećanja kursa Na + K + . Međutim, kompenzacijski kapacitet natrijum/kalijum pumpe je ograničen i gube se i natrijum i kalijum. Pad sadržaja natrijuma u krvnoj plazmi dovodi do oslobađanja aldosterona, što zauzvrat povećava intenzitet izmjene Na + K + između tubularne tekućine i tubularnih epitelnih stanica. Aldosteron, dok povećava reapsorpciju natrijuma kroz sistem transportera kalijuma, ipak ga ne vraća na nivo koji je uporediv sa funkcionalno kompletnim mehanizmom razmene Na + H +. Predloženi mehanizmi objašnjavaju uzrok natriurije, kaliurije, hipokalemije i hiperaldosteronizma u distalnom RCA.
Podešavanje alkalne pH vrijednosti u distalnom RCA povećava količinu filtriranog bikarbonata, moguće povećavajući neto negativni naboj u tubularnoj tekućini. Uz povećanu permeabilnost ćelija epitela distalnog nefrona za H+, višak negativnog naboja koji stvara filtrirani bikarbonat sprečava aktivni obrnuti protok vodikovih jona duž gradijenta koncentracije iz lumena tubula u ćelije ili ekstracelularni prostor. , čime se uklanjaju ograničenja u razmjeni Na + H + u distalnom dijelu tubula, te se shodno tome smanjuje količina natrijuma koji se izlučuje urinom.
Smanjen gubitak natrijuma u mokraći ublažava stimulans lučenja aldosterona, stimulira metabolizam Na + K + i, posljedično, izlučivanje kalija putem bubrega. Međutim, normalizacija sadržaja kalija i aldosterona u krvnoj plazmi, količine natrijuma i kalija izlučenih u urinu je privremena i vraća se na vrijednosti koje su se dogodile prije korekcije acidoze.
Podešavanje alkalne pH vrijednosti u proksimalnom RCA povećava gubitak kalija. Ovaj fenomen se može objasniti prekomjernim protokom natrijum bikarbonata u distalne tubule i njegovim indukcijskim djelovanjem na mehanizam reapsorpcije natrijuma, odnosno razmjenu Na + K +. Moguće je da su natriureza i kaliureza u proksimalnom RCA povezane sa smanjenjem sposobnosti lučenja H+ uz normalnu permeabilnost epitelnih stanica za vodikove ione.
- bubrežna tubularna acidoza s poremećenom apsorpcijom bikarbonata iz tubularne tekućine i acidifikacijom urina u kombinaciji s hiperkalemijom [prikaži]
Bubrežna tubularna acidoza s hiperkalemijom
Bubrežna tubularna acidoza (RKA), praćena hiperkalemijom, može se razviti u kroničnom zatajenju bubrega u kombinaciji s nedovoljnim lučenjem aldosterona (hipoaldosteronizam) i (ili) smanjenjem osjetljivosti epitelnih stanica distalnih bubrežnih tubula na njega. Razvoj metaboličke acidoze u kombinaciji s hiperkalemijom u hipoaldosteronizmu moguć je i u odsustvu kroničnog zatajenja bubrega. Djelovanje aldosterona na ciljne ćelije tubulnog epitela u distalnom nefronu povećava sekreciju K+ i H+ u tubularnu tekućinu u zamjenu za Na+. Uz uravnotežen metabolizam, dnevno se luči 100-200 mcg aldosterona. Nedostatak aldosterona dovodi do smanjenja lučenja H+ u distalnom nefronu i poremećene acidifikacije urina.
U situaciji kada je hipoaldosteronizam u kombinaciji s normalnim volumenom glomerularne filtracije, pacijenti imaju povišen pH urina i poremećen odgovor na amonijum hlorid, kao u distalnom RCA. Uz kombinaciju kronične bubrežne insuficijencije s hipoaldosteronizmom u većine pacijenata, utvrđuje se kisela (pH 5,0) reakcija urina. U patogenezi razvoja metaboličke acidoze kod njih ključnu ulogu igra nedovoljno uklanjanje kalija u urinu i, kao rezultat, apsorpcija viška kalija unutarćelijskim prostorom u zamjenu za vodikove ione koji ulaze u krv.
Pacijenti s RKA i hiperkalemijom reagiraju na zamjenu mineralokortikoida prvo ispravljanjem hiperkalemije (najvažnijeg faktora) i sporije reverzijom metaboličke acidoze.
Dinamika promjena vrijednosti parametara acido-baznog stanja kod metaboličke acidoze nebubrežnog i bubrežnog porijekla prikazana je u tabeli. 20.3 [prikaži] .
| Tabela 20.3 Laboratorijski podaci za različite etiološke oblike metaboličke acidoze (prema Mengele, 1969.) | |||||||||||
| Etiološki oblici | krvna plazma | Urin | |||||||||
| pH | Ukupan sadržaj CO 2 | R CO 2 | Bikarbonati | Baferske baze | Anioni | K | Cl | P | pH | K | |
| With normalna funkcija bubreg | |||||||||||
| dijabetička acidoza | (ketonska tijela) | ~ | N | ||||||||
| Acidoza natašte, groznica, tireotoksikoza, ćelijska hipoksija | (ketonska tijela) | N~ | ~ | N | N | ||||||
| Acidoza sa uvođenjem amonijum hlorida, kalcijum hlorida, arginina i lizin hlorida | N | ~ | N | N~ | |||||||
| Acidoza zbog trovanja metil alkoholom | (mravlja kiselina) | ~ | N | N~ | |||||||
| Acidoza zbog gubitka alkalne tečnosti | N | ~ | N~ | N | N~ | ||||||
| Sa oštećenom funkcijom bubrega | |||||||||||
| Bubrežna tubularna acidoza | N | N | |||||||||
| Kada se liječi inhibitorima karboanhidraze | N | N | |||||||||
| Bolest bubrega bez većeg ograničenja glomerularne filtracije | N | N~ | N | ||||||||
| Acidoza kod akutnog zatajenja bubrega | ~ | ~ | oligurija | ||||||||
| Hiperhloremijska acidoza | N | N~ | N | N~ | |||||||
| Acidoza sa zadržavanjem dušikovog otpada kod kronične bubrežne insuficijencije | N~ | N~ | N~ | ||||||||
| Oznake: N - norma; - smanjenje; - povećati; ~ - tendencija povećanja ili smanjenja. | |||||||||||
Kompenzacijske reakcije tijela kod metaboličke acidoze
Kompleks kompenzacijskih promjena u tijelu tokom metaboličke acidoze, usmjerenih na vraćanje fiziološkog pH optimuma, sastoji se od:
- djelovanje ekstracelularnih i intracelularnih pufera [prikaži]
Djelovanje ekstracelularnih i intracelularnih pufera
Interakcija viška vodonikovih jona sa glavnim komponentama puferskih sistema je najbrža kompenzatorna reakcija kod metaboličke acidoze. Rezultati pH mjerenja i određivanja nivoa komponenti u pufer sistemima ukazuju na vodeću ulogu bikarbonatnog pufera, u kojem svako smanjenje HCO 3 - za 1 mmol/l dovodi do smanjenja P CO 2 za 1,2 mm Hg. Iznad smo razmotrili primjer puferske kompenzacije sa bikarbonatom sa jednom injekcijom od 12 mmol H+ za svaki litar krvi. Na početnoj vrijednosti R CO 2 40 mm Hg. Art. pH krvi će biti 7,1. Naknadna normalizacija pH dolazi zbog činjenice da se višak vodikovih jona apsorbira unutarćelijski prostor, gdje se vežu za proteine i različite molekularne oblike fosfata (dihidrofosfat, pirofosfat, itd.).
U koštanom tkivu neutralizaciju vodikovih iona vrše soli ugljične kiseline.
Sposobnost H+ da prodre u ćeliju ima važan uticaj na koncentraciju kalijuma (K+) u plazmi. Uklanjanje vodikovih jona iz intracelularnog prostora je praćeno suprotnom promjenom koncentracije K+ u plazmi za približno 0,6 mmol/l za svakih 0,1 pH. U analiziranoj varijanti metaboličke acidoze, gdje se pH smanjuje sa 7,4 na 7,1, treba očekivati povećanje koncentracije K+ u plazmi za 1,8 mmol/l.
Hiperkalijemija se javlja čak i kod manjka ukupnog K+ u tijelu. Ako pacijent s metaboličkom acidozom ima normokalemiju ili hipokalemiju, onda to ukazuje na ozbiljan nedostatak kalija.
Terapija metaboličke acidoze kod pacijenata sa hipokalemijom treba da uključi obavezno nadoknađivanje nedostatka kalijuma. Sa stabilnim viškom metaboličkog opterećenja vodoničnim jonima, kompenzacijske sposobnosti puferskih sistema su potencirane kompenzatornom reakcijom respiratornog sistema.
- reakcije respiratornog sistema [prikaži]
Kompenzacijski odgovor respiratornog sistema
Pri pH vrijednostima ispod fiziološkog optimuma dolazi do direktne stimulacije hemoreceptora respiratornog centra jonima vodika i povećanju alveolarne ventilacije. Sa padom pH krvi sa 7,4 na 7,1, volumen alveolarne ventilacije može se povećati sa 5 l / min u normi na 30 l / min ili više. Alveolarna ventilacija se povećava povećanjem plimnog volumena, a ne brzine disanja. Teška hiperventilacija se naziva Kussmaulovo disanje. Ako se tokom pregleda pacijenta otkrije Kussmaulovo disanje, to ukazuje na prisutnost metaboličke acidoze.
Kao rezultat hiperventilacije, omjer P CO 2 u krvi opada [HCO 3 - / H 2 CO 3 ] se vraća na vrijednost od 20:1, što odgovara normalna vrijednost pH. Posljedica novog ravnotežnog nivoa HCO 3 - i H 2 CO 3 je smanjenje kapaciteta bikarbonatnog pufera za neutralizaciju kiseline \u003d P CO 2 · 0,03 (0,03 - koeficijent rastvorljivosti P CO 2 - mmol / mm Hg)]. Rezultati kliničkih opažanja omjera HCO 3 - i P CO 2 ukazuju da u slučaju nezavisne varijante CBS poremećaja u obliku metaboličke acidoze:
P CO 2 \u003d 40 - 1.2 · [HCO 3 - ],
gdje je [HCO 3 - ] vrijednost koja odgovara količini bikarbonata koja nedostaje normalnoj vrijednosti, koja se izračunava po formuli;
24 - određena vrijednost [HCO 3 - ],
1.2 - faktor konverzije za količinu P CO 2U analiziranom primeru, sa nezavisnom varijantom metaboličke acidoze, izmerena vrednost R CO 2 treba da bude jednaka 26 mm Hg. Art. ili blizu ove vrijednosti.
Ako je P CO 2< 40-1,2 · [NSO 3 - ], tada je moguća varijanta mješovitog kršenja CBS-a. Na primjer, u slučaju trovanja salicilatima P CO 2< 40 - 1,2 · [HCO 3 - ]. U analiziranom primjeru pad HCO 3 - iznosio je 12 mmol/l, a izmjerena vrijednost R CO 2 10 mm Hg. čl., što je 16 mm Hg. Art. ispod izračunate vrijednosti, karakteristične za varijantu kršenja CBS-a u obliku metaboličke acidoze.
Ovakva razlika između izračunatih i izmjerenih pokazatelja ukazuje na kombinaciju metaboličke acidoze s respiratornom alkalozom.
Ako je P CO 2 > 40 - 1.2 · [HCO 3 - ], onda ovo takođe ukazuje na mešoviti prekršaj. U analiziranom primjeru pad HCO 3 - iznosio je 12 mmol/l, a izmjerena vrijednost R CO 2 - 46 mm Hg. čl., što je 20 mm Hg. Art. više od vrijednosti karakteristične za varijantu kršenja acido-bazne ravnoteže u obliku metaboličke acidoze. Ovakva razlika između izračunatih i izmjerenih pokazatelja ukazuje na kombinaciju metaboličke i respiratorne acidoze.
Kompenzatornu reakciju respiratornog sistema za normalizaciju pH vrijednosti dopunjuju bubrežni mehanizmi stabilizacije fiziološki optimalne koncentracije vodonikovih jona.
- bubrežni procesi izlučivanja viška vodikovih jona i sinteze bikarbonata koji se koriste za neutralizaciju H+ [prikaži]
Renalne kompenzacijske reakcije
Kod metaboličke acidoze, oni su usmjereni na:
- uklanjanje suvišnih količina vodikovih jona;
- maksimalna reapsorpcija glomerularno filtriranog bikarbonata;
- stvaranje rezerve bikarbonata kroz sintezu HCO 3 - u reakcijama acido- i amoniogeneze.
Kao odgovor na povećano opterećenje vodikovih jona u stanicama bubrega, povećava se aktivnost glutaminaze i povećava se stvaranje NH 3, koji zajedno sa izlučenim viškom H+ ulazi u tubulnu tekućinu. U cevastom fluidu, joni vodonika vezuju se za NH 3 i formiraju NH 4 . Paralelno, dolazi do neutralizacije H+ pufera tubularne tekućine i naknadnog izlučivanja svih ovih oblika u urinu. Svaki izlučeni amonijum ion osigurava da jedan bikarbonatni ion uđe u alkalnu rezervu krvi.
- Jedinice SI u medicini: Per. sa engleskog. / Rev. ed. Menshikov V. V. - M.: Medicina, 1979. - 85 str.
- Zelenin K. N. Hemija - Sankt Peterburg: Spec. Književnost, 1997.- S. 152-179.
- Osnovi fiziologije čovjeka: Udžbenik / Ed. B.I.Tkačenko - Sankt Peterburg, 1994.- T. 1.- S. 493-528.
- Bubrezi i homeostaza u normalnim i patološkim stanjima. / Ed. S. Clara - M.: Medicina, 1987, - 448 str.
- Ruth G. Acid-bazni status i ravnoteža elektrolita.- M.: Medicina 1978.- 170 str.
- Ryabov S. I., Natochin Yu. V. Funkcionalna nefrologija.- Sankt Peterburg: Lan, 1997.- 304 str.
- Hartig G. Moderna infuzijska terapija. Parenteralna ishrana.- M.: Medicina, 1982.- S. 38-140.
- Shanin V.Yu. Tipični patološki procesi - Sankt Peterburg: Spec. književnost, 1996. - 278 str.
- Sheiman D. A. Patofiziologija bubrega: Per. s engleskog - M.: Eastern Book Company, 1997. - 224 str.
- Kaplan A. Clinical chemistry.- London, 1995.- 568 str.
- Siggard-Andersen 0. acidobazni status krvi. Kopenhagen, 1974.- 287 str.
- Siggard-Andersen O. Vodikovi joni i. plinovi u krvi - U: Hemijska dijagnoza bolesti. Amsterdam, 1979.- 40 str.
Izvor: Medicinski laboratorijska dijagnostika, programe i algoritme. Ed. prof. Karpishchenko A.I., Sankt Peterburg, Intermedica, 2001


