17.02.2018
Ltd. institutul de introducere a noilor tehnologii medicale ramen
Diagnosticul problemelor cardiace este mult simplificat cele mai recente metode cercetare sistem vascular persoană. În ciuda faptului că inima este un organ independent, este destul de grav afectată de activitate sistem nervos, ceea ce poate duce la întreruperi în funcționarea acestuia.
Studii recente au scos la iveală relația dintre bolile de inimă și sistemul nervos, provocând moartea subită frecventă.
Ce este VSR?
Intervalul normal de timp dintre fiecare ciclu de bătăi ale inimii este întotdeauna diferit. La persoanele cu inimă sănătoasă se schimbă tot timpul chiar și în repaus staționar. Acest fenomen se numește variabilitate. ritm cardiac(abreviat HRV).
Diferența dintre contracții este în cadrul unei anumite valori medii, care variază în funcție de starea specifică a organismului. Prin urmare, HRV este evaluată doar în poziție staționară, deoarece diversitatea activității organismului duce la o modificare a ritmului cardiac, ajustându-se de fiecare dată la un nou nivel.
Citirile HRV indică fiziologia în sisteme. Analizând HRV, se pot evalua cu precizie caracteristicile funcționale ale corpului, se pot monitoriza dinamica inimii, se poate identifica o scădere bruscă a ritmului cardiac, ceea ce duce la moarte subita.
Metode de determinare
Studiul cardiologic al contracțiilor inimii a determinat metodele optime de HRV, caracteristicile acestora în diferite condiții.
Analiza se efectuează pe studiul succesiunii de intervale:
- R-R (electrocardiograma contractiilor);
- N-N (intervale dintre contracțiile normale).
Metode statistice. Aceste metode se bazează pe obținerea și compararea intervalelor „N-N” cu o estimare a variabilității. Cardiointervalograma obținută în urma examinării arată un set de intervale „R-R” care se repetă unul după altul.
Indicatorii acestor lacune includ:
- SDNN reflectă suma indicatorilor HRV la care sunt evidențiate abaterile N-N intervaleși Variabilitatea R-R goluri;
- Comparație RMSSD N-N secvențe intervale;
- PNN5O arată procent N-N intervale care diferă cu mai mult de 50 de milisecunde pentru întreg intervalul de studiu;
- Evaluarea CV a indicatorilor variabilității amplitudinii.
Metode geometrice izolate prin obținerea unei histograme, care înfățișează cardiointervale cu durate diferite.
Aceste metode calculează variabilitatea ritmului cardiac folosind anumite valori:
- Mo (Mode) înseamnă intervale cardio;
- Amo (Mode Amplitude) - numărul de intervale cardio care sunt proporționale cu Mo ca procent din volumul selectat;
- VAR (variation range) este raportul dintre gradul dintre intervalele cardio.
Analiza autocorelației evaluează ritmul cardiac ca o dezvoltare aleatorie. Acesta este un grafic de corelație dinamică obținut cu o deplasare treptată a unei unități a seriei dinamice în raport cu seriile proprii.
Această analiză calitativă ne permite să studiem influența verigii centrale asupra activității inimii și să determinăm latența periodicității ritmului cardiac.
Ritmografie corelativă(dispersiunea). Esența metodei constă în afișarea intervalelor cardio succesive într-un plan grafic bidimensional.
În timpul construcției scatterogramei, este selectată o bisectoare, în centrul căreia există un set de puncte. Dacă punctele sunt deviate spre stânga, puteți vedea cât de mult este ciclul mai scurt, deplasarea spre dreapta arată cât de mult este mai lung cel precedent.
Pe ritmograma rezultată, zona corespunzătoare abaterea N-N intervale. Metoda vă permite să identificați munca activă sistemul vegetativși efectul său ulterior asupra inimii.
Metode de studiere a HRV
Standardele medicale internaționale definesc două moduri de a studia ritmul cardiac:
- Înregistrarea înregistrării intervale „RR” - timp de 5 minute este utilizat pentru o evaluare rapidă a HRV și a anumitor teste medicale;
- Înregistrarea zilnică a intervalelor „RR” - evaluează mai precis ritmurile înregistrării vegetative a intervalelor „RR”. Cu toate acestea, la descifrarea înregistrării, mulți indicatori sunt evaluați prin intervalul de cinci minute de înregistrare HRV, deoarece segmentele sunt formate pe o înregistrare lungă care interferează cu analiza spectrală.
Pentru a determina componenta de înaltă frecvență într-un ritm cardiac, este nevoie de o înregistrare de aproximativ 60 de secunde, iar pentru a analiza componenta de frecvență joasă sunt necesare 120 de secunde de înregistrare. Pentru a evalua corect componenta de joasă frecvență, este necesară o înregistrare de cinci minute, care este aleasă pentru studiul standard HRV.
HRV a unui corp sănătos
Variabilitatea ritmului median în oameni sanatosi face posibilă determinarea rezistenței lor fizice în funcție de vârstă, sex, moment al zilei.
Fiecare persoană are un scor HRV diferit. Femeile au o frecvență cardiacă mai activă. Cel mai mare HRV este urmărit în copilărie și adolescență. Componentele de înaltă și joasă frecvență scad odată cu vârsta.
HRV este afectată de greutatea unei persoane. Greutatea corporală redusă provoacă puterea spectrului HRV, la persoanele supraponderale se observă efectul opus.
Sportul și activitatea fizică ușoară au un efect benefic asupra VRC: puterea spectrului crește, ritmul cardiac devine mai puțin frecvent. Încărcările excesive, dimpotrivă, cresc frecvența contracțiilor și reduc HRV. Aceasta explică frecventele decese subite în rândul sportivilor.
Utilizarea metodelor de determinare a variației ritmului cardiac vă permite să controlați antrenamentul, crescând treptat sarcina.
Dacă HRV este scăzut
O scădere bruscă a variației ritmului cardiac indică anumite boli:
Ischemic și hipertensiune;
. infarct miocardic;
· Scleroză multiplă;
· Diabet;
· Boala Parkinson;
Recepția anumitor medicamente;
Tulburări nervoase.
Cercetarea HRV în activitati medicale sunt printre metodele simple și accesibile care evaluează reglarea autonomă la adulți și copiii cu o serie de boli.
În practica medicală, analiza permite:
· Evaluează reglarea viscerală a inimii;
Determinați activitatea generală a corpului;
Evaluează nivelul de stres și activitate fizica;
Monitorizați eficacitatea terapiei medicamentoase;
Diagnosticați boala într-un stadiu incipient;
· Ajută la alegerea unei abordări pentru tratamentul bolilor cardiovasculare.
Prin urmare, atunci când examinăm corpul, nu trebuie să neglijăm metodele de studiu a contracțiilor inimii. Indicatorii HRV ajută la determinarea severității bolii și la alegerea tratamentului potrivit.
Pentru a evalua riscul de apariție a evenimentelor cardiace adverse, este utilizată pe scară largă analiza variației frecvenței cardiace (HRV), care reprezintă o fluctuație temporală a intervalelor dintre bătăile succesive ale inimii (intervale RR) și este considerată ca un marker al activității sistemul nervos autonom (SNA). HRV este o expresie cantitativă, o măsură a aritmiei sinusale. În ultimii ani, interesul a crescut pentru studiul HRV ca indicator care reflectă reglarea autonomă a inimii și determină riscul de moarte subită cardiacă. În prezent, HRS este recunoscut ca fiind cel mai informativ și metoda accesibila evaluarea reglării autonome a ritmului cardiac și este parte integrantă a examinării pacienților cardiaci.
În ciuda unui număr mare de studii care indică relația dintre sistemul simpatic, parasimpatic, baroreflex, termoreglator, influențe umorale cu anumiți indicatori temporali și spectrali ai HRV, s-a acumulat până în prezent o mare cantitate de material factual, ceea ce nu permite să se ia în considerare fără ambiguitate. HRV ca metodă de evaluare a echilibrului vagosimpatic. Astfel, experții de la Clinica Mayo (SUA), după ce au analizat activitatea pe o perioadă de 20 de ani în domeniul HRV, au remarcat că, având în vedere natura multiplă a endo- și factori exogeni care afectează formarea structurii ritmului cardiac, parametrii HRV nu reflectă starea adevărată a SNA la pacienții cu patologie cardiovasculară.
Scopul principal al studiului HRV în timpul monitorizării zilnice ECG (pentru perioade lungi de timp) este acela de a evalua starea funcțională a pacientului. Starea funcțională a pacientului este capacitatea și disponibilitatea corpului de a îndeplini diverse funcții (conform I.K. Anokhin, 1975), în special, menținând homeostazia și starea intelectuală. O măsură comună pentru toate aceste funcții poate fi considerată energia cheltuită pentru performanța lor. Un organism viu, atunci când interacționează cu mediul extern, caută să obțină un rezultat util cu cele mai mici costuri energetice.
Unul dintre indicatorii funcționării normale a sistemelor este HRV normal. Ritmul cardiac ridicat, scăderea HRV și aritmia sinusală sunt factori nefavorabili în aprecierea stării funcționale a pacientului. Predominanța activității simpatice este caracteristică unei stări de stres și afectează negativ activitatea. a sistemului cardio-vascular, duce la dezvoltarea tahicardiei, aritmiilor cardiace, ischemiei miocardice, crizelor hipertensive. La pacienții cu hipertensiune arterială și boli cerebrovasculare, există modificări ale HRV cu o predominanță a activității sistemului nervos simpatic. Scăderea HRV este asociată cu vârsta.
Un accident vascular cerebral duce nu numai la o creștere a nivelului de catecolamine plasmatice, ci și la modificări în reglarea autonomă a sistemului cardiovascular, afectarea HRV, care poate afecta negativ instabilitatea electrică a miocardului, poate provoca aritmii, care pot agrava hemodinamica și afectează negativ procesele reparatorii din zona ischemiei cerebrale. Odată cu dezvoltarea accident vascular cerebral ischemic a existat o corelație pozitivă între indicatorii de frecvență ai HRV și nivelurile tensiunii arteriale sistolice și diastolice în timpul zilei și pe timp de noapte, ceea ce indică un singur mecanism implicat în reglarea sistemului cardiovascular și încălcarea acestuia la pacienții în perioada acută. de IS. Disfuncția reglării autonome a sistemului cardiovascular afectează supraviețuirea după un accident vascular cerebral.
LA perioada acuta IS inhibă reglarea autonomă a inimii cu o scădere a tuturor parametrilor HRV și circadian
indicele (CI) ritmului cardiac. S-a găsit o relație directă între activitatea autonomă totală (SDNN) și severitatea deficitului neurologic la începutul și la sfârșitul perioadei acute. Riscul de accident vascular cerebral este corelat cu SDNN scăzut pe timp de noapte. În prezența depresiei la pacienții cu AVC, SDNN a fost semnificativ.
considerabil mai jos.
În accident vascular cerebral, a fost mai mult decât la pacienții cu criza hipertensivă, scăderea indicatorilor de timp ai HRV și CI. O scădere a VRC a fost observată la pacienții cu hipertensiune arterială în perioada acută de IS. Până la sfârșitul perioadei acute, severitatea deficienței vegetative la pacienții cu ICC crește, ceea ce se datorează modificări difuze mușchiul inimii, ducând la restructurarea aparatului vegetativ intracardiac.
În prezența unui deficit neurologic pronunțat la sfârșitul perioadei de recuperare precoce a unui accident vascular cerebral la pacienții cu insuficiență cardiacă cronică de I-II FC în dinamică, în comparație cu perioada acută (7-10 zile de boală), o valoare semnificativă statistic scăderea HRV, o creștere a activității sistemului simpatico-suprarenal. Regresia simptomelor neurologice devreme perioada de recuperare IM ischemic este însoțit de o scădere disfuncție autonomă conform WRS.
Accident vascular cerebral lacunarîn perioada acută este însoțită de modificări ale HRV. Scăderea activității parasimpatice se corelează cu un prognostic precoce prost la persoanele cu aterotromboză.
accident vascular cerebral.
În perioada acută a unui accident vascular cerebral, există o scădere a HRV din cauza leziunilor anumitor structuri ale creierului. Până la sfârșitul perioadei acute, deficitul maxim de influențe autonome asupra ritmului cardiac persistă la pacienții cu AVC în sistemul vertebrobazilar și cu o leziune focală mare. Observarea prospectivă timp de 1 an a stării vegetative la pacienți după un AVC în bazinul vertebrobazilar indică o persistență semnificativă a tulburărilor HRV identificate. Scăderea HRV este mai pronunțată în localizarea pe partea dreaptă a leziunii cerebrale. În același timp, cele mai scăzute valori ale HRV au fost înregistrate atunci când insula dreaptă a fost implicată în focalizarea patologică. Cu localizarea pe partea dreaptă a unui AVC, indiferent de leziunea lobului insular, există un deficit persistent în reglarea autonomă, în Mai mult datorită componentei parasimpatice, care poate fi asociată cu un prognostic mai nefavorabil.
În perioada cea mai acută a IS la pacienții cu o leziune predominantă a bazinului carotidian cu formarea de focare mari și medii, există o încălcare persistentă a reglării autonome cardiovasculare.
Interrelațiile dintre hemodinamica cerebrală și centrală în perioada acută a accidentului vascular cerebral vertebrobazilar de origine ischemică, exprimată într-o scădere a fluxului sanguin cerebral, nu numai în bazin. arterelor vertebrale, dar în general, cu o creștere simultană a indicatorilor funcției de pompare a inimii în prima zi a unei catastrofe cerebrale și cu scăderea ei ulterioară până la sfârșitul celei de-a 3-a săptămâni; în același timp, o scădere a indicelui cardiac sub 1,8 a fost prognostic nefavorabil.
Până la sfârșitul perioadei acute de accident vascular cerebral, severitatea deficitului autonom crește la pacienții cu insuficiență cardiacă cronică (ICC), care se datorează modificărilor difuze ale mușchiului cardiac, ducând la o restructurare a aparatului autonom intracardiac. Regresia simptomelor neurologice în perioada de recuperare timpurie a IS este însoțită de o scădere a disfuncției autonome conform datelor HRV.
HR CI caracterizează variabilitatea ritmului în timpul zilei și este o caracteristică importantă proces patologic. Fluctuațiile circadiene ale frecvenței crizelor cardiace sunt strâns legate de bioritmurile modificărilor proprietăților electrofiziologice la nivelul miocardului. În prima zi de IS, există o scădere semnificativă a CI, care persistă în următoarele trei săptămâni. Când focalizarea este situată în sistemul vertebrobazilar o scădere a CI este persistentă și indică stabilitatea încălcărilor rezervelor funcționale ale sistemului cardiovascular, o leziune a sistemului carotidian este însoțită de un răspuns adecvat al CI în procesul de recuperare. Pacienții cu cursuri diferite de accident vascular cerebral au diferite variante modificări ale reglementării autonome și gradul inegal de severitate a acestora, ceea ce permite utilizarea evaluării modificărilor din ambele părți ale ANS pentru a prezice severitatea și rezultatul bolii.
Cele mai informative criterii pentru HRV, care sunt asociate cu un risc ridicat de deces în accident vascular cerebral cu o probabilitate de 70-82%: SDNN< 60 мс, SDANN < 45 мс, rMSSD < 15 мс . Выдвинута гипотеза о том, что параметры ВРС наряду с caracteristici clinice pot fi predictori de progresie curs clinic AI .
La pacienții cu IS sever, analiza HRV în primele trei zile de boală a relevat mai multe rate mici SDNN. La pacienții cu accident vascular cerebral sever (inclusiv deces), activitate crescută departament simpatic ANS, în timp ce ECG prezintă semne de afectare sau ischemie a subendo- sau subepicardului. Cu aproximativ o zi înainte de moarte, la pacienții cu o evoluție nefavorabilă a bolii, în ciuda terapiei în curs, HRV a scăzut și mai mult, ceea ce a indicat încetarea aproape completă a controlului autonom asupra funcțiilor sistemului cardiovascular.
Conform datelor din literatură, tulburările HRV în AVC moderat și sever sunt persistente, în timp ce în AVC ușor, datele privind dinamica HRV sunt contradictorii. La curs usor accident vascular cerebral, tensiunea diviziunii simpatice a sistemului nervos autonom, de regulă, este observată numai în prima zi a bolii, urmată de o predominanță a tonusului departament parasimpatic. Modificările ECG la astfel de pacienți de obicei nu apar. La pacienţii cu focare ischemice mici, apariţia dereglării autonome apare abia spre sfârşitul perioadei acute.
1.1.1. Variabilitatea ritmului cardiac în perioada acută a accidentului vascular cerebral
În studiu, HRV a fost evaluată în conformitate cu recomandările.
Au fost evaluați următorii indicatori de timp:
♦ SDNN (ms) - abaterea standard (rădăcină medie pătrată) a întregii game de intervale RR consecutive (NN), care reprezintă efectul total al reglării autonome a inimii;
♦ SDNNi (ms) - indice SDNN, valoarea medie a abaterilor standard a segmentelor consecutive de 5 minute ale înregistrării zilnice a intervalelor RR, reflectând variabilitatea cu un ciclu de 5 minute;
♦ RMSSD (ms) - Rădăcină pătrată suma medie a diferenţelor dintre perechile consecutive de intervale RR sau diferenţa pătratică medie dintre intervalele RR adiacente, reflectând activitatea verigii parasimpatice de reglare autonomă;
♦ pNN50 (%) - numărul de intervale RR consecutive, diferenţa dintre care depăşeşte 50 ms, exprimat ca procent din numărul total de cardiointervale, reflectând gradul de predominanţă a verigii parasimpatice de reglare asupra celei simpatice.
Profilul circadian al ritmului cardiac a fost evaluat prin indicele circadian. CI a fost calculat ca raportul dintre frecvența cardiacă medie pe timp de zi și frecvența cardiacă medie pe timp de noapte. Profilul circadian a fost considerat corect cu CI de la 1,24-1,42, rigid - cu CI< 1,2, усиленным - при ЦИ >1,45 (Makarov L.M., 2011). O ușoară abatere a profilului circadian de la normă (valoarea de frontieră) a fost considerată la o valoare CI în intervalul 1,2-1,23.
Pe lângă indicatorii de timp ai HRV, a fost utilizată metoda „analizei secțiunilor scurte”. O concluzie integrală cu privire la HRV a fost efectuată asupra proporției zonelor cu variabilitate scăzută: dacă este mai mare de 60%, atunci „Redus brusc”, de la 30 la 60% - „Redus moderat”, mai puțin de
30% - „Norma”.
Cu ajutorul studiului HRV, este posibil să se obțină noi criterii de diagnostic diferențial pentru disfuncția sistemului cardiovascular, inclusiv ca urmare a leziunilor vasculare cerebrale. HRV este un indicator obiectiv și sensibil al funcției cerebrale în accidentul vascular cerebral.
În tabel. 1.1.1 prezintă o descriere comparativă a indicatorilor de frecvență cardiacă, HRV și CI a pacienților incluși în studiu. Frecvența cardiacă medie în loturile studiate a fost aproximativ aceeași. Scăderea maximă a SDNN a fost observată la pacienții cu OH: cu 11,36% (P< 0,01) ниже, чем в ГК и на 18,07 % (P < 0,001) ниже, чем в ГЗК. SDNNi в ОГ был минимальным, однако разница была статистически незначима. Межгрупповых различий показателей rMSSD и pNN50 не было. Известно, что показатели SDNN и SDNNi отражают суммарный эффект вегетативной регуляции сердца, поэтому их снижение свидетельствует об ослаблении вегетативной регуляции сердечно-сосудистой системы в целом (как симпатической, так и парасимпатической) и снижении адаптационных возможностей сердечно-сосудистой системы, что является factor nefavorabil.
CI la pacienții cu OH a fost cel mai scăzut și a fost de 1,12: mai mic decât în GC - cu 5,08% (P< 0,001) и ниже, чем в ГЗК - на 11,11 % (P < 0,001). При индивидуальной оценке ЦИ оказалось, что у больных ОГ ригидный циркадный профиль ритма встречался на 28,78 % чаще (Р < 0,001), чем в ГК (в 85,19 % случаев против 56,41 %) и на 61,86 % чаще (P < 0,001), чем в ГЗК (в 85,19 % случаев против 23,33 %).
Variabilitatea circadiană a parametrilor ritmului cardiac este o manifestare originală a HRV și reflectă rezervele funcționale ale sistemului cardiovascular în timpul adaptării la ciclul zilnic al activității zilnice.
O scădere semnificativă a CI la pacienții cu OH indică o încălcare pronunțată a reglării centrale și autonome a ritmului cardiac, care poate fi asociată cu un prognostic nefavorabil și un risc ridicat de sincopă aritmogenă și moarte subită.
Tabelul 1.1.1
Variabilitatea ritmului cardiac (M ± m; n, %)
|
Indicatori |
OG (n = 108) |
GC (n = 78) |
GZK (n = 30) |
|
Ritmul cardiac pe zi |
69,21±0,98 |
69,61 ± 1,12 |
71,10 ± 1,45 |
|
S DNN, ms |
112,00±3,45 |
12 6,35 ± 4,21 P1< 0, 01 |
136,70±5,58 P1< 0,001 |
|
SDNNi, ms |
48,81 ± 1,67 |
49,82 ± 2,06 |
51,27 ± 1,94 |
|
rMSSD, ms |
27,53 ± 1,42 |
27,71 ± 1,91 |
25,83 ± 1,63 |
|
pNN 50, ٪ |
6,18 ± 0,73 |
6,47 ± 0,82 |
5,7 0 ± 1,09 |
|
1,12±0,01 |
1,18±0,01 P1< 0,001 |
1,26±0,01 P1< 0,001 ; P 2< 0,001 |
|
|
Evaluarea integrală a HRV(n, ٪) |
|||
|
Normal |
39 (36,11 ٪ ) |
31 (39,74 ٪ ) |
15 (50 ٪ ) |
|
Moderat redus |
26 (24,07 ٪ ) |
2 7 (3 4,62 ٪ ) |
12 (40 ٪ ) |
|
Redus dramatic |
43 (39,82 ٪ ) |
20 (25,64 ٪ ) P1< 0, 05 |
3 (10 ٪ ) R١< 0, 001; Р٢ < 0, 001 |
|
aritmie sinusală |
35 (32,41 ٪ ) |
44 (56,41 ٪ ) P1< 0,002 |
28 (90,33 ٪ ) P1< 0,001; P 2< 0,001 |
Notă. P1 este eroarea semnificației diferențelor în comparație cu OG; P2 - cu GC.
La evaluarea HRV prin metoda „analiza secțiunii scurte”, scăderea variabilității la pacienții cu OH și GC a fost mai vizibilă. Astfel, în MG, numărul de pacienți cu o HRV puternic redusă a fost de 1,55 ori mai mare (P< 0,05), чем в ГК и в 3,98 раза больше (P < 0,001), чем в ГЗК.
O observație interesantă a fost că, odată cu scăderea HRV, prevalența aritmiei sinusale în MG și GC a scăzut în comparație cu pacienții practic sănătoși, iar incidența aritmiei sinusale în MG a fost de 1,74 ori mai mică (P< 0,002), чем в ГК и в 2,79 раза (P < 0,001), чем в ГЗК.
Aritmia sinusală este inerentă atât persoanelor sănătoase, cât și celor bolnave. La persoanele sănătoase, aritmia sinusală este asociată cu acte respiratorii. Aritmia respiratorie indică functionare normala a sistemului nervos autonom și este privit ca un factor favorabil, iar dispariția aritmiilor respiratorii și a aritmiilor sinusale în general se datorează scăderii funcției sistemului nervos autonom și are un prognostic nefavorabil.
Rezultatele studiului au arătat că în perioada cea mai acută de scădere a IS, HRV și HR CI scade prevalența sinus artia, ceea ce indică o scădere a mecanismelor de adaptare a organismului și este un factor de prognostic nefavorabil.
1.1.2. Variabilitatea ritmului cardiac în funcție de severitatea și localizarea focarului accidentului vascular cerebral
Caracteristicile clinice și demografice ale pacienților cu OH, în funcție de severitate, sunt prezentate în tabel. 1.1.2.1. Pacienții cu AVC sever au fost mai severi în ceea ce privește gradul de HA și prevalența DZ în rândul lor.
Tabelul 1.1.2.1
Caracteristicile comparative ale pacienţilor în funcţie de
severitatea IS (n, %; M ± m) (n = 108)
|
Caracteristicile pacientilor |
Severitatea accidentului vascular cerebral |
||
|
(n=20) |
(n=80) |
(n=8) |
|
|
Varsta medie, ani |
57,46 ± 2,71 |
62,16 ± 1,27 |
62,63 ± 4,41 |
|
AH, am diplomă AH, gradul II AH, gradul III |
9 (45 ٪ ) 9 (45 ٪ ) 2 (10 ٪ ) |
13 (16 ,25 ٪ ) P1< 0,0 2 41 (51,25 ٪ ) 26 (32 ,5 ٪ ) P1< 0,0 05 |
1 (12,5 ٪ ) P2< 0,0 5 4 (50 ٪ ) 3 (37,5 ٪ ) |
|
angină pectorală Istoric de infarct miocardic |
4 (30,7 ٪ ) 1 (7,7 ٪ ) 1 (7,7 ٪ ) |
43 (49,4 ٪ ) 10 (11,5 ٪ ) 19 (21,8 ٪ ) |
2 (25 ٪ ) 4 (50 ٪ ) P1< 0,0 5 |
|
Circumferința taliei (FROM), cm |
9 4,25 ± 5,31 |
102,26 ± 2,42 |
99,23 ± 6,31 |
|
IMC, kg/m2 |
26,93 ± 0,81 |
29,41±0,69 P1< 0,05 |
25,26 ± 1,94 |
|
Glicemia a jeun, mmol/l |
4,88±0,33 |
5,94±0,24 P1< 0,01 |
7,68 ± 1,04 P1< 0, 02 |
|
colesterol total, mmol/l |
4,21±0,38 |
5,47 ± 0,22 P1< 0,01 |
4,42 ± 0,37 |
|
Colesterol HDL, mmol/l |
1,17±0,39 |
0,97 ± 0,09 |
0,81 ± 0,10 |
|
TG, mmol/l |
1,13 ± 0,28 |
1,36 ± 0,16 |
0,87 ± 0,17 P2< 0,05 |
|
Colesterol LDL, mmol/l |
1,91±0,38 |
4,15±0,47 P1< 0,001 |
4,20±0,42 P1< 0,001 |
|
Potasiu, mmol/l |
4,2±0,50 |
4,22 ± 0,09 |
4,63 ± 0,61 |
|
Magneziu, mmol/l |
0,86±0,06 |
0,90±0,01 |
0,93±0,02 |
Notă. Eroarea de semnificație a diferențelor în comparație cu indicatorii în AVC: P1 - plămân, P2 - moderat.
Nivelurile lipidelor plasmatice la pacienții cu AVC ușor au fost normale. Odată cu creșterea severității accidentului vascular cerebral, spectrul lipidic a avut o schimbare mai proaterogenă: nivelul LDL-C în accidentul vascular cerebral moderat și sever a fost de 2,2 ori mai mare (P< 0,001), чем при легком. Уровень ХС ЛПВП снижался с увеличением тяжести инсульта. ИА при средней тяжести и тяжелом инсульте был соответственно
în 3 (pag< 0,001) и 2, 1 (P < 0,02) раза выше, чем при легком.
Paralel cu creșterea numărului de pacienți cu diabet și severitatea accidentului vascular cerebral, a crescut și nivelul glicemiei a jeun. Nivelurile de potasiu și magneziu la diferite severități ale accidentului vascular cerebral au fost aproximativ aceleași și au fost în intervalul normal.
Severitatea accidentului vascular cerebral a corelat direct și slab cu vârsta pacientului (r = 0,188; P< 0,05), уровнем ХС ЛПНП (r = 0,223; P < 0,05), ИА (r = 0,201; P < 0,05), уровнем глюкозы крови (r = 0,273; P < 0,01).
La studierea caracteristicilor HRV în funcție de severitatea accidentului vascular cerebral (Tabelul 1.1.2.2), s-a dovedit că odată cu creșterea severității, severitatea tulburărilor HRV a crescut. Astfel, frecvența cardiacă medie zilnică în accidentul vascular cerebral sever a fost mai mare cu 13,3% (P< 0,05) в сравнении с легким и на 11 % выше (P < 0,05) в сравнении с инсультом средней тяжести. Известно, что синусовая тахикардия в состоянии покоя свидетельствует о нарушении автономной регуляции сердца с преобладанием симпатических влияний на сердце .
Aproape toți indicatorii temporali ai HRV au scăzut odată cu creșterea severității accidentului vascular cerebral, în timp ce diferențele dintre severitatea ușoară și moderată au fost nesemnificative statistic, iar în cazurile severe, scăderea indicatorilor a fost semnificativă.
SDNN și SDNNi la pacienții cu AVC sever au fost reduse cu 1,4, respectiv (P< 0,05) и в 1,5 (P < 0,005) раза в сравнении с пациентами с легким инсультом и в 1,2 (P < 0,05) и 1,3 (P < 0,005) раза в сравнении с пациентами средней тяжести. rMSDD и pNN50 при тяжелом инсульте были соответственно ниже таковых в 1,7 (P < 0,01) и 7 (P < 0,02) раз в сравнении с легким инсультом и в 1,7 (Р < 0,001) и 6,4 (Р < 0,001) раза в сравнении с пациентами средней тяжести.
Când se compară indicatorii temporali ai HRV ai OH cu severitate diferită a accidentului vascular cerebral cu indicatorii GC, s-a dovedit că, în cazul accidentului vascular cerebral ușor, indicatorii nu diferă semnificativ și, deja, în cazul accidentului vascular cerebral moderat, a existat o scădere semnificativă a SDNN cu 11,7% (P< 0,001).
Datele obținute indică o scădere semnificativă a HRV la pacienții cu AVC sever, atât datorită scăderii reglării generale autonome, cât și a slăbirii efectelor parasimpatice asupra inimii.
Tabelul 1.1.2.2
Variabilitatea ritmului cardiac în funcție de
asupra severității accidentului vascular cerebral (M ± m; n, %)
|
Indicatori |
GK(n = 78) |
Severitatea accidentului vascular cerebral |
||
|
(n=20) |
(n=80) |
(n=8) |
||
|
Ritmul cardiac pe zi |
69,61 ± 1,12 |
67,75 ± 2,26 |
68,91±1,1 |
76,50±3,65 P1< 0,05 R٢< 0,05 |
|
12 6,35 ± 4,21 |
126,0 ± 9,76 |
111,51 ± 3,78 P3< 0,001 |
91,00 ± 9,22 P1< 0,05 P2< 0,05 |
|
|
49,82 ± 2,06 |
53,83 ± 4,73 |
48,94 ± 1,86 |
36,83 ± 3,49 P1< 0,0 05 P2< 0,00 5 P3< 0,001 |
|
|
rMSSD, ms |
27,71 ± 1,91 |
27,92 ± 4,08 |
28,25 ± 1,60 |
16,67 ± 1,43 P1< 0,01 R 2< 0,001 P3< 0,001 |
|
6,47 ± 0,82 |
7,00±2,40 |
6,44±0,81 |
1,00±0,26 P1< 0,02 R٢< 0,001 P3< 0,001 |
|
|
1,18±0,01 |
1,12 ± 0,03 |
1,13±0,01 P3< 0,001 |
1,06 ± 0,04 P3< 0,001 |
|
|
Evaluarea integrală a HRV ( n, ٪) |
||||
|
Normal |
31 (4 9,8 ٪ ) |
9 (45 ٪ ) |
30 (37,50 ٪ ) |
|
|
Moderat redus |
2 7 (3 4,6 ٪ ) |
8 (40 ٪ ) |
16 (20 ٪ ) |
2(25,00 ٪ ) |
|
Redus dramatic |
20 (25,6 ٪ ) |
3 (15 ٪ ) |
34 (42,50 ٪ ) P1< 0, 05 P3< 0,05 |
6 (75,00 ٪ ) P1< 0,05 P2< 0,05 P3< 0,05 |
|
aritmie sinusală |
44 (56,4 ٪ ) |
16 (80,00 ٪ ) |
19 (23,75 ٪ ) P1(P< 0,001) P 3 (pag< 0,001) |
|
Notă. Eroarea de semnificație a diferențelor în comparație cu parametrii pacienților: P1 - AVC ușor, P2 - AVC moderat, P3 - cu GC.
CI în accidentul vascular cerebral ușor a avut tendința de a scădea, iar în accidentul vascular cerebral moderat și sever a fost mai mic decât în GC cu 5,1% (P< 0,001) и на 10,2 % (P < 0,001) соответственно.
Analiza HRV de către evaluare integrală a arătat, de asemenea, o creștere a prevalenței HRV redusă brusc cu creșterea severității accidentului vascular cerebral. În accidentul vascular cerebral sever, o VFC redusă brusc a fost mai frecventă cu 60% (P< 0,05) в сравнении с легким и на 32,5 % в сравнении с инсультом средней тяжести (P < 0,05). Кроме этого, при инсульте средней тяжести отмечалось достоверное уменьшение распространенности выраженной синусовой аритмии в сравнении с пациентами ГК и легким инсультом (на 32,65 %; P < 0,001 и 56,25 %; P < 0,001 соответственно) и ее исчезновение у пациентов с тяжелым инсультом.
Analiza comparativă a HRV în funcție de evaluarea integrală a pacienților cu OH cu GC a arătat că în accidentul vascular cerebral ușor, indicatorii nu diferă semnificativ, iar în accidentul vascular cerebral moderat, a existat o scădere semnificativă a numărului de pacienți cu HRV normal - 37,5% față de 49,8% (P< 0,05) и увеличение количества пациентов с резко сниженной ВРС - 42,5 % против 25,6 % (P < 0,05).
Cele de mai sus arată că scăderea HRV în cea mai acută perioadă a unui AVC depinde de severitatea acestuia: în AVC ușor, HRV nu scade, în AVC moderat și mai ales sever, scade semnificativ, ceea ce este un factor nefavorabil. Luând în considerare absența diferențelor în aproape toți indicatorii HRV folosiți de noi la pacienții cu AVC ușor cu HC, apariția diferențelor în SDNN, CI și concluzia integrală prin analiza „secțiunilor scurte” în comparație cu indicatorii HC la pacienți cu severitate moderată a AVC, am presupus că acești trei indicatori au cea mai mare sensibilitate în evaluarea HRV. Odată cu creșterea severității scăderii HRV (în accidentul vascular cerebral sever), toți indicatorii folosiți de noi au scăzut (au reacționat).
Se știe că sistemele nervoase central și autonom sunt implicate în reglarea ritmului cardiac, astfel încât deteriorarea diferitelor structuri ale creierului poate afecta activitatea bioelectrică a inimii, adică localizarea unui accident vascular cerebral poate avea propriul efect asupra parametrii de reglare autonomă și prognosticul bolii. Prin urmare, a fost efectuată o analiză a HRV în funcție de localizarea focarului accidentului vascular cerebral.
Pentru a studia efectul localizării focalizării AVC asupra activității bioelectrice a inimii, pacienții cu OH cu AVC moderat au fost împărțiți în 3 subgrupe: cu localizare pe partea dreaptă în sistemul carotidian - 34 (42,50%), pe partea stângă - 36 (45%) iar în sistemul vertebrobazilar.sistemul - 10 (12,5%). Pacienții din aceste subgrupe au fost aproximativ comparabili în ceea ce privește sexul, vârsta, durata și severitatea hipertensiunii arteriale, patologie concomitentă, severitatea tulburărilor metabolice și medicamentele luate.
În tabel. 1.1.2.3 arată indicatorii HRV și CI în funcție de locația focalizării accidentului vascular cerebral. Frecvența cardiacă medie la diferite locații ale focalizării a fost aproximativ aceeași. Parametrii de timp HRV nu au diferit semnificativ, cu toate acestea, cu localizarea pe partea dreaptă și vertebrobazilară a focarului de accident vascular cerebral, a existat o tendință de scădere a indicatorilor care reflectă HRV total, cum ar fi SDNN (la 107,38 ± 5,68 și, respectiv, 103,50 ± 6,76 ms). vs. 118,47 ± 6,29 ms pentru localizarea pe partea stângă) și SDNNi (până la 46,91 ± 2,91 și, respectiv, 45,75 ± 3,51 ms, față de 51,92 ± 3,05 ms).
Tabelul 1.1.2.3
Variabilitatea ritmului cardiac în funcție de locația focarului accidentului vascular cerebral (n = 80) (M ± m; n, %)
|
Indicatori |
sistemul carotidian |
Vertebral - sistem bazilar ( n = 10) |
|
|
Dreapta (n=34) |
Stânga (n = 36) |
||
|
Ritmul cardiac pe zi |
69,53 ± 1,77 |
68,87 ± 1,83 |
6 7,00 ± 1,53 |
|
107,38±5,68 |
118,47 ± 6,29 |
103,50 ± 6,76 |
|
|
46,91 ± 2,91 |
51,92 ± 3,05 |
45,75 ± 3,51 |
|
|
rMSS D, ms |
27,09 ± 2,01 |
27,00 ± 2,07 |
30,33±5,33 |
|
pNN50, ٪ |
5,74 ± 1,14 |
6,82 ± 1,25 |
7,17 ± 2,75 |
|
1,12±0,01 |
1,12±0,01 |
1,09±0,02 |
|
|
Evaluarea integrală a HRV ( n, ٪) |
|||
|
Normal |
11 (32,35 ٪ ) |
14 (38,89 ٪ ) |
5 (50 ٪ ) |
|
Moderat redus |
10 (29,41 ٪ ) |
5 (14,70 ٪ ) |
1 (10 ٪ ) |
|
Redus dramatic |
13 (38,24 ٪ ) |
17 (47,22 ٪ ) |
4 (40 ٪ ) |
|
aritmie sinusală |
9 (26,47 ٪ ) |
8 (22,22 ٪ ) |
2 (20 ٪ ) |
CI la pacienții cu localizare vertebrobazilară a focarului a fost cel mai scăzut și a fost de 1,09 ± 0,02, în timp ce la pacienții cu stânga și partea dreaptă a fost ușor mai mare - 1,12 ± 0,01.
La evaluarea HRV în conformitate cu concluzia integrală, sa dovedit că numărul de pacienți cu HRV normal a fost ușor mai mic cu localizare pe partea dreaptă - 11 (32,35%) comparativ cu localizarea pe partea stângă și vertebrobazilară - 14 (38,89%) și 5 (50%). Detectarea aritmiei sinusale severe a fost aproximativ aceeași.
Conform literaturii de specialitate, ratele HRV scăzute sunt detectate în localizarea pe partea dreaptă a leziunilor cerebrale,
si in sistemul vertebrobazilar, mai ales cand este afectata insula dreapta (insula Rail).
Datele noastre nu confirmă datele din literatură, probabil din cauza numărului insuficient de pacienți cu AVC sever din studiu, în care tulburările HRV sunt mai pronunțate.
Astfel, în perioada cea mai acută a IS cu o evoluție ușoară a accidentului vascular cerebral, HRV și CI nu scad semnificativ, în timp ce în IS moderat și sever, o scădere a HRV și CI, o scădere a prevalenței aritmiei sinusale crește cu o creștere. în severitatea accidentului vascular cerebral. Nu a fost evidențiat un efect semnificativ al localizării focalizării accidentului vascular cerebral asupra HRV și CI, doar o tendință la o scădere a HRV în localizarea pe partea dreaptă și o scădere a CI în localizarea vertebrobazilară, ceea ce nu ne permite să vorbim fără ambiguitate. despre efectul localizării focalizării AVC asupra HRV.
1.1.3. Analiza corelației
Analiza corelației a evidențiat o relație semnificativă statistic între parametrii HRV și severitatea accidentului vascular cerebral, vârstă, nivelurile de glucoză din sânge și potasiu, IMC și WC (Tabelul 1.1.3).
Tabelul 1.1.3
Coeficienții de corelație ai parametrilor HRV cu severitatea accidentului vascular cerebral, vârsta, glicemia, IMC, WC și nivelul de potasiu seric (r) (n = 108)
|
Indicatori |
rMSS D |
HRV conform evaluării integrale |
|||
|
Severitatea accidentului vascular cerebral |
P< 0,05 |
0,189 R< 0,05 |
|||
|
P< 0,02 |
R< 0,005 |
||||
|
glucoza din sange |
0,3 88 P< 0, 001 |
0,4 15 P< 0, 001 |
0,28 0 P< 0, 00 5 |
0,2 39 P< 0, 02 |
R< 0,005 |
|
P< 0, 002 |
|||||
|
P< 0, 001 |
P< 0, 001 |
R< 0,05 |
|||
|
Potasiu (n=40) |
0,400 R< 0 ,05 |
0,310 R< 0 ,05 |
0,3 77 R< 0,02 |
SDNN a fost negativ și slab corelat cu severitatea accidentului vascular cerebral (r = -0,203; P< 0,05), умеренно - с уровнем глюкозы крови (r = -0,388; P < 0,001), ИМТ (r = -0,313; P < 0,002) и ОТ (r = -0,395; P < 0,001).
SDNNi a fost negativ și slab corelat cu vârsta (r = -0,231; P< 0,02), умеренно - с уровнем глюкозы крови (r = -0,415; Р < 0,001), ОТ (r = -0,372; P < 0,001), положительно и умеренно - с уровнем калия сыворотки крови (r = 0,400; P < 0,05).
rMSSD a fost slab corelat cu nivelurile de glucoză (r = -0,280; P< 0,005), положительно и умеренно - с уровнем калия (r = 0,310; P < 0,05), pNN50 отрицательно и слабо - с уровнем глюкозы (r = -0,239; P < 0,02).
Severitatea scăderii VRC conform evaluării integrale prin analiza „secțiunilor scurte” a corelat pozitiv cu severitatea AVC (r = 0,189; P< 0,05), возрастом (r = 0,285; P < 0,005), уровнем глюкозы крови (r = 0,271; P < 0,005), ОТ (r = 0,251; Р < 0,05) и отрицательно и умеренно с уровнем калия сыворотки крови (r = -0,377; P < 0,02).
Este de remarcat faptul că toți indicatorii HRV au corelat cu nivelurile de glucoză. În studiu, 25 (23,2%) pacienți cu accident vascular cerebral au avut diabet de tip 2 concomitent. Probabil, această relație este mediată prin catecolamine, a căror eliberare crește în timpul stresului în prima zi a unui accident vascular cerebral, care cresc nivelul de glucoză din sânge, ritmul cardiac și reduc HRV. Nu este exclusă prezența neuropatiei cardiace diabetice la pacienți, care duce la o scădere a reglării autonome (o scădere a vagalului și predominanța relativă a efectelor simpatice asupra inimii).
Relația directă între nivelurile de glucoză din sânge și WC (r = 0,472; P< 0,001) была более высокой, чем взаимосвязь уровня глюкозы и ИМТ (r = 0,224; P < 0,05), что подтверждает данные литературы о большем значении висцерального жирового депо в развитии толерантности тканей к глюкозе в сравнении с подкожным жировым депо.
Nu a existat o relație semnificativă între parametrii HRV și lipidele plasmatice din sânge, probabil datorită faptului că perioada acută de AVC, fiind un stres, poate duce la scăderea lipidelor.
Cele de mai sus arată că, alături de severitatea accidentului vascular cerebral, factorii de risc suplimentari pentru scăderea HRV sunt vârsta, tulburările metabolice precum hiperglicemia și obezitatea abdominală, precum și scăderea nivelului de potasiu seric.
1.1.4. Dinamica variabilității ritmului cardiac
După 10 zile de tratament, severitatea scăderii VRC a crescut, atât conform indicatorilor de timp, cât și conform concluziei integrale.
Frecvența cardiacă medie zilnică nu s-a schimbat semnificativ. Scădere semnificativă: SDNNi - cu 9,62% (P< 0,001), свидетельствующий об ослаблении регулирующего влияния ВНС на синусовый узел, rMSSD - на 10,96 % (P < 0,02), свидетельствующий об уменьшении вагусных влияний на сердце (рис. 1.1.4.1). Показатель, отражающий степень преобладания вагуса (pNN50), имел отчетливую тенденцию к снижению
cu 21,13% (P< 0,1).
Orez. 1.1.4.1. Dinamica indicatorilor de timp ai HRV (∆, %)
Notă. Fiabilitatea dinamicii indicatorului: * - P< 0,05; # - P < 0,1.
Dinamica HRV conform evaluării integrale a fost similară cu cea din punct de vedere al indicatorilor de timp ai HRV. A existat o tendință negativă semnificativă: numărul pacienților cu HRV normal a scăzut cu 16,30% (P< 0,02), а количество больных с умеренно сниженной и резко сниженной ВРС увеличилось соответственно на 10,87 и 5,43 % (рис. 1.1.4.2).

Orez. 1.1.4.2. Dinamica HRV conform evaluării integrale (∆, %)
Notă. * Fiabilitatea dinamicii indicatorului (P< 0,02).
În ciuda scăderii indicatorilor HRV, CI a avut un trend pozitiv (Fig. 1.1.4.3), crescut cu 1,79% (R< 0,01) (с 1,12 ± 0,01 до 1,14 ± 0,01), оставаясь при этом существенно ниже чем в ГК (1,14 ± 0,01 против 1,18 ± 0,01) (Р = 0,005), что свидетельствует о начинающем
restabilirea adaptării organismului la ciclul zilnic de activitate
după 10 zile de tratament
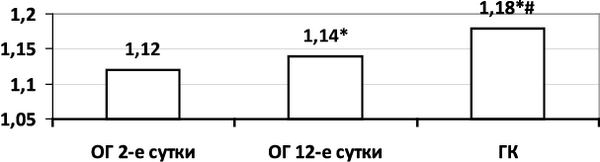
Orez. 1.1.4.3. Dinamica CI (∆, %)
Notă. Fiabilitatea diferențelor: * - în comparație cu indicele OH (ziua 2) (P< 0,01), # - в сравнении с показателем ОГ (12-е сутки) (P < 0,005)
Conform literaturii de specialitate, tulburările HRV pot persista după încheierea perioadei acute de accident vascular cerebral.
Se poate presupune că dinamica negativă a HRV se datorează unei creșteri a efectului patologic al focalizării accidentului vascular cerebral asupra nodului sinusal sau scăderea HRV este de natură întârziată. Probabil, indicatorii HRV în perioada cea mai acută de accident vascular cerebral la pacienții cu capacități de adaptare păstrate (la pacienții cu AVC nesever) nu se modifică semnificativ din cauza creșterii intensității mecanismelor de adaptare a sistemelor de reglementare, iar după 10 zile, mecanismele de adaptare sunt epuizate, ceea ce duce la o scădere a HRV, apoi apare o scădere a HRV la acești pacienți este de natură întârziată, iar terapia în curs nu poate preveni o tendință negativă. La pacienții cu AVC sever sau la pacienții cu capacitate adaptativă inițial scăzută (pacienți mai în vârstă, cu diabet), mecanismele de adaptare sunt epuizate mai devreme (încă în perioada cea mai acută de AVC) și HRV redusă persistă pe parcursul terapiei de 10 zile.
Pentru a confirma această ipoteză, am analizat dinamica HRV și CI în funcție de severitatea accidentului vascular cerebral (Fig. 1.1.4.4).
Cea mai mare dinamică negativă a parametrilor temporali HRV a fost observată în accidentul vascular cerebral ușor. Următorii indicatori s-au modificat semnificativ: SDNNi și rMSDD au scăzut cu 19,57 (P = 0,031) și, respectiv, 30,89% (P = 0,042), s-a observat o tendință clară de scădere a pNN50 - cu 64,45% (P = 0,054). Frecvența cardiacă medie zilnică a crescut cu 14,37% (de la 65,67 ± 2,35 la 75,11 ± 3,73 pe minut) (P = 0,034), ceea ce se datorează probabil activării sistemului simpatico-suprarenal.

Orez. 1.1.4.4. Dinamica indicatorilor de timp ai HRV în funcție de severitatea accidentului vascular cerebral (∆, %)
< 0,05; # - P < 0,1.
În accidentul vascular cerebral moderat, dinamica negativă a fost mai puțin pronunțată decât în accidentul vascular cerebral ușor. SDNNi a scăzut cu 8,24% (P = 0,001), a existat o tendință clară către o scădere a rMSDD cu 8,84% (P = 0,064). pNN50 a scăzut cu 14,86%, dar diferența nu a fost semnificativă statistic. Frecvența cardiacă medie zilnică a crescut ușor - cu 1,36% (de la 69,27 ± 1,09 la 70,21 ± 1,22 pe minut).
În accidentul vascular cerebral sever, nu au existat modificări semnificative ale parametrilor de timp HRV, ceea ce indică persistența tulburărilor HRV la această categorie de pacienți.
Dinamica negativă a HRV în termeni de timp a coincis cu cea a evaluării integrale: în accidentul vascular cerebral ușor, numărul pacienților cu HRV normal a scăzut cu 33% (de la 44,44 la 11,11%) (P< 0,05), а больных с умеренно сниженной и резко сниженной ВРС - увеличилось соответственно на 11,11 и 22,22 % (рис. 1.1.4.5).
În accidentul vascular cerebral moderat, dinamica negativă a fost mai puțin pronunțată decât în accidentul vascular cerebral ușor. A existat o scădere semnificativă a pacienților cu HRV normal cu 16,46% (R< 0,05), а количество больных с умеренно сниженной и резко сниженной ВРС увеличивалось соответственно на 12,66 и 3,80 %. При тяжелом инсульте динамики ВРС не выявлено.
După 10 zile, diferența parametrilor HRV ai pacienților în funcție de severitatea accidentului vascular cerebral a rămas, deși mai puțin semnificativă: numărul de pacienți cu o HRV puternic redusă a fost de 33,33% în cursul ușor, 45,57% în severitate moderată și 75% în severă.
În paralel cu scăderea VRC în accidentul vascular cerebral ușor și moderat, a existat o tendință de scădere a depistarii episoadelor de aritmie sinusală în dinamică, cu 92,4 (P = 0,181) și respectiv 66,83% (P = 0,085), care poate confirma scăderea crescândă a adaptării organismului la 10-12 zile a perioadei acute de accident vascular cerebral. În AVC sever, episoade de aritmie sinusală nu au fost înregistrate nici în perioada acută, nici în dinamică după 10 zile de tratament, ceea ce confirmă persistența scăderii HRV la acești pacienți.
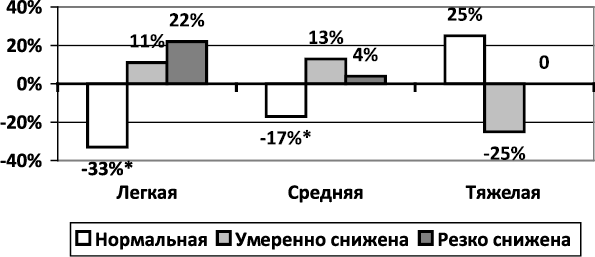
Orez. 1.1.4.5. Dinamica HRV conform evaluării integrale
în funcție de severitatea accidentului vascular cerebral (∆, %)
Notă. Fiabilitatea dinamicii indicatorului: * - P< 0,05.
CI s-a îmbunătățit semnificativ cu orice severitate a AVC, ceea ce indică o creștere a mecanismelor de adaptare a organismului la ciclul zilnic de activitate, ceva mai bine cu AVC ușor (Fig. 1.1.4.6). Dinamica de la valoarea inițială a fost 5,31; 1,80 și 2,65% (P< 0,05) соответственно нарастанию тяжести инсульта.
De remarcat că la un AVC ușor, CI a revenit la cel al GC, iar la AVC moderat și sever a rămas
mai mic decât în GC.
Astfel, analiza dinamicii HRV a arătat că în AVC ușor și moderat, tulburările HRV progresează, în timp ce în AVC sever persistă și nu se corectează în decurs de 10 zile de la tratament. Adaptarea organismului la ciclul zilnic de activitate în AVC ușor este restabilită, manifestată printr-o creștere a CI la cea din GC, și începe să crească la pacienții cu AVC moderat și sever.

Orez. 1.1.4.6. Dinamica CI în funcție de severitatea accidentului vascular cerebral (∆, %)
Notă. Fiabilitatea dinamicii indicatorului: * - P< 0,05.
Studiul arată că în cea mai acută perioadă de scădere a IS, HRV și HR CI scade prevalența sinus artia, ceea ce indică o scădere a mecanismelor de adaptare a organismului și este un factor de prognostic nefavorabil.
Severitatea afectării depinde de severitatea accidentului vascular cerebral. În cazurile ușoare, HRV și CI nu scad semnificativ, în timp ce în cazurile moderate și severe, o scădere a HRV și CI, o scădere a prevalenței aritmiei sinusale crește odată cu creșterea severității accidentului vascular cerebral. Nu a fost evidențiat un efect semnificativ al localizării focalizării accidentului vascular cerebral asupra HRV și CI, doar o tendință la o scădere a HRV în localizarea pe partea dreaptă și o scădere a CI în localizarea vertebrobazilară, ceea ce nu ne permite să vorbim fără ambiguitate. despre efectul localizării focalizării AVC asupra HRV.
Odată cu severitatea accidentului vascular cerebral, au fost observați factori de risc suplimentari pentru o scădere a HRV: vârsta, tulburări metabolice precum hiperglicemia și obezitatea abdominală, precum și scăderea nivelului de potasiu seric.
S-a demonstrat că în dinamica tulburărilor HRV progresează în AVC ușor și moderat, rămân reduse în AVC sever și nu sunt corectate în decurs de 10 zile de tratament. S-a observat o dinamică pozitivă a HR CI. Adaptarea organismului la ciclul zilnic de activitate este restabilită în AVC ușor, care se manifestă printr-o creștere a CI până la cea din GC, și începe să crească la pacienții cu AVC moderat și sever.
Având în vedere relația inversă dintre gradul de dinamică negativă a VRC și severitatea accidentului vascular cerebral, este posibil ca scăderea VRC, ca urmare a sindromului cerebrocardic, în accidentul vascular cerebral ușor și moderat, să fie întârziată și să se manifeste prin a 12-a zi de boală. neexclus şi Influență negativă asupra medicamentelor HRV.
Vă aducem la cunoștință revistele publicate de editura „Academia de Istorie Naturală”
31 martie la 14:06 19215 0
Studiul variabilității ritmului cardiac (HRV) a început în 1965, când cercetătorii Hon și Lee au remarcat că suferința fetală a fost precedată de intervale alternante între bătăile inimii înainte de a avea loc orice modificare vizibilă a ritmului cardiac. Doar 12 ani mai târziu, Wolf și colab. au descoperit o asociere cu un risc mai mare de deces la pacienții cu IM cu HRV redus. Rezultatele studiului Framingham pe o perioadă de urmărire de 4 ani (736 de persoane în vârstă) au demonstrat în mod convingător că HRV conține informații de prognostic independente și în afara factorilor de risc tradiționali. În 1981, Akselrod și colaboratorii au folosit analiza spectrală a fluctuațiilor ritmului cardiac pentru cuantificare indicatori ai sistemului cardiovascular de la sistolă la sistolă.
În 1996, un grup de lucru de experți de la Societatea Europeană de Cardiologie și de la Societatea Nord-Americană de Stimulare și Electrofiziologie a dezvoltat standarde pentru utilizarea măsurătorilor HRV în practica clinicași studii cardiace, în baza cărora sunt acum efectuate majoritatea studiilor. Pentru a determina HRV, se recomandă utilizarea unui număr de metode care oferă cel mai mult analiză completă cu costuri minime de metode și timp. Pe lângă recomandările privind alegerea metodei de evaluare a HRV, documentul conține cerințe pentru procedura de măsurare a tuturor parametrilor care afectează determinarea HRV.
Determinarea HRV, principalele domenii de aplicare a metodei, indicații de utilizare
duminicăsunt modificări naturale ale intervalelor dintre bătăile inimii (durata ciclurilor cardiace) din normal ritmul sinusal inimile. Se numesc intervale NN (de la norman la norman). O serie consecutivă de cardiointervale nu este un set de numere aleatoare, ci are o structură complexă, care reflectă influența reglatoare asupra nodului sinusal al inimii sistemului nervos autonom și diverși factori umorali. Prin urmare, o analiză a structurii HRV oferă informații importante despre starea reglării autonome a sistemului cardiovascular și a corpului în ansamblu.
Centrii cardiaci ai medulei oblongate și ai puțului controlează direct activitatea inimii, oferind efecte cronotrope, inotrope și dromotrope. emițătoare influențe nervoase mediatorii chimici servesc asupra inimii: acetilcolina în sistemul parasimpatic și norepinefrina în sistemul nervos simpatic.
Putem distinge condiționat 4 domenii de aplicare a metodelor de analiză HRV:
1. Evaluarea stării funcționale a organismului și a modificărilor acestuia pe baza determinării parametrilor echilibrului autonom și reglării neuroumorale.
2. Evaluarea severității răspunsului adaptativ al organismului sub influența diferitelor stresuri.
3. Evaluarea stării legăturilor individuale în reglarea autonomă a circulației sanguine.
4. Elaborarea concluziilor prognostice bazate pe evaluarea stării funcționale actuale a organismului, a severității răspunsurilor sale adaptative și a stării legăturilor individuale ale mecanismului de reglare.
Implementarea practică a acestor domenii deschide un domeniu larg de activitate atât pentru oameni de știință, cât și pentru practicieni. Următoarea este o listă orientativă și destul de incompletă a domeniilor de aplicare a metodelor de analiză a HRV și a indicațiilor pentru utilizarea lor, compilată pe baza unei analize a publicațiilor moderne interne și străine.
Lista domeniilor de aplicare a metodelor de analiză HRV:
1. Evaluarea reglării autonome a ritmului cardiac la persoanele practic sănătoase (nivel inițial de reglare autonomă, reactivitate autonomă, suport autonom al activității).
2. Evaluarea reglării autonome a ritmului cardiac la pacienții cu diverse patologii (modificări ale echilibrului autonom, gradul de predominanță a uneia dintre diviziunile sistemului nervos autonom). Chitanță Informații suplimentare pentru diagnosticul anumitor forme de boală, cum ar fi neuropatia autonomă în diabet.
3. Evaluarea stării funcționale a sistemelor de reglare ale organismului pe baza unei abordări integrale a sistemului circulator ca indicator al activității adaptative a întregului organism.
4. Determinarea tipului de reglare autonomă (vago-, normo- sau simpaticotonie).
5. Predicția riscului de moarte subită și aritmii fatale în IM și boala coronariană la pacienții cu aritmii ventriculare, cu ICC datorată hipertensiunii arteriale, cardiomiopatie.
6. Identificarea grupurilor de risc pentru dezvoltarea unei stabilități sporite a ritmului cardiac care pune viața în pericol.
7. Utilizați ca metodă de control la efectuarea diferitelor teste funcționale.
8. Evaluarea eficacității activităților terapeutice și profilactice și recreative.
9. Evaluarea nivelului de stres, a gradului de tensiune a sistemelor de reglare sub efecte extreme și subextreme asupra organismului.
10. Utilizați ca metodă de evaluare a stărilor funcționale în timpul masei examinări preventive diverse segmente ale populației.
11. Prognoza stării funcționale (stabilitatea corpului) în timpul selecției profesionale și determinarea aptitudinii profesionale.
12. Alegerea optimului terapie medicamentoasăținând cont de fondul reglării autonome a inimii. Monitorizarea eficacității terapiei în curs, ajustarea dozei de medicament.
13. Evaluarea și predicția reacțiilor psihice în funcție de gravitatea fondului vegetativ.
14. Controlul stării funcţionale în sport.
15. Evaluarea reglării autonome în procesul de dezvoltare la copii și adolescenți. Aplicare ca metodă de control în medicina școlară pentru cercetarea socio-pedagogică și medico-psihologică.
Lista furnizată nu este exhaustivă și poate fi completată.
Cauzele HRV
HRV are o origine externă și internă. La motive externe include o schimbare a poziției corpului în spațiu, activitate fizica, stres psiho-emoțional, temperatura mediului.
Inima denervată bate aproape constant. După cum sa menționat mai sus, labilitatea ritmului cardiac se datorează efectului autonom asupra nodului sinusal. Impulsurile simpatice accelerează ritmul cardiac, iar cele parasimpatice o încetinesc. Scopul principal al reglarii ritmului cardiac este stabilirea tensiunii arteriale. Este reglat de mecanismul baroreflex, care este cel mai rapid mecanism de reglare a tensiunii arteriale cu o perioadă de latentă de aproximativ 1-2 s. Pe lângă efectele vegetative asupra inimii, modificările ritmului cardiac sunt cauzate și de factori umorali. Fluctuațiile în concentrația de adrenalină și a altor agenți umorali din sânge explică originea undelor foarte lente ale ritmului cardiac (<0,04 Гц).
Mecanismul modificărilor ritmului cardiac în timpul respirației este asociat cu funcționarea sistemului baroreflex pentru stabilizarea tensiunii arteriale. Excursiile pieptului și ale diafragmei în timpul respirației duc la fluctuații de presiune în cavitatea toracică, ceea ce este un efect interesant asupra sistemului de stabilizare a tensiunii arteriale. După cum știți, debitul cardiac scade la inspirație și crește la expirație din cauza modificărilor fluxului sanguin către inimă cu modificări ale presiunii în cavitatea toracică. Acest lucru provoacă fluctuații ale tensiunii arteriale. O modificare a tonusului nervului vag are un efect direct asupra ritmului cardiac. La inspirație, are loc o scădere a tonusului nervului vag și intervalele cardio sunt reduse. În același timp, cu cât depresia vagală a nodului sinusal este mai puternică, cu atât sunt mai mari fluctuațiile ritmului cardiac în timpul respirației. Acest lucru este confirmat de faptul că blocarea cu atropină a nervului vag duce la o scădere bruscă a amplitudinii undelor respiratorii ale ritmului cardiac.
Se știe că odată cu creșterea volumului sanguin și creșterea presiunii în venele mari, apare o creștere a frecvenței cardiace în ciuda creșterii concomitente a tensiunii arteriale - așa-numitul reflex Bainbridge. Acest reflex prevalează asupra reflexului baroreceptor cu o creștere a BCC și, dimpotrivă, o scădere a volumului sanguin duce la o scădere a IOC și a tensiunii arteriale, în timp ce se remarcă o creștere a ritmului cardiac.
Ventilația pulmonară are un efect special asupra VRC: stimularea chemoreceptorilor determină hiperventilație moderată, în timp ce bradicardia este detectată din partea inimii și, dimpotrivă, cu hiperventilație semnificativă, ritmul cardiac crește de obicei.
Metode de cercetare HRV
Conform standardelor internaționale, HRV este examinat prin două metode:
1) înregistrarea intervalelor R–R în 5 min;
2) înregistrarea intervalelor R–R în timpul zilei. Înregistrarea pe termen scurt este mai des folosită pentru evaluarea expresă a HRV și diferite teste funcționale și de droguri. Pentru o evaluare mai precisă a HRV și studiul ritmurilor circadiene de reglare autonomă, se utilizează metoda de înregistrare zilnică a intervalelor R–R. Cu toate acestea, chiar și cu înregistrarea zilnică, calculul majorității indicatorilor HRV este efectuat pentru fiecare perioadă consecutivă de 5 minute. Acest lucru se datorează faptului că pentru analiza spectrală este necesar să se utilizeze numai segmente staționare ale ECG și, cu cât înregistrarea este mai lungă, cu atât mai des apar procese non-staționare.
Pentru a evalua componenta de înaltă frecvență (HF) a ritmului cardiac este necesară o înregistrare de aproximativ 1 min, în timp ce pentru analiza componentei de joasă frecvență (LF) sunt deja necesare 2 min de înregistrare. Pentru o evaluare obiectivă a componentei de frecvență foarte joasă a HRV (VLF), durata înregistrării ar trebui să fie de cel puțin 5 minute. Prin urmare, pentru a standardiza studiile HRV cu înregistrări scurte, a fost aleasă o durată preferată de înregistrare de 5 minute.
Cerințe pentru înregistrarea ECG pe termen scurt pentru analiza HRV
Studiul trebuie început nu mai devreme de 1,5-2 ore după masă. Studiile se desfășoară într-o cameră întunecată, în 12 ore este necesar să încetați să luați medicamente, să beți cafea, alcool, stres fizic și psihic. Înregistrarea este înregistrată în intervalul de la 9:00 la 12:00 în condiții confortabile la o temperatură a aerului de 20–22 °C. Înainte de începerea studiului, este necesară o perioadă de adaptare la condițiile de mediu timp de 5-10 minute. Studiul la femei trebuie efectuat ținând cont de fazele ciclului menstrual. Este necesar să eliminați toate influențele enervante: opriți telefonul, opriți vorbirea cu pacientul, excludeți apariția altor persoane în birou, inclusiv lucrătorii sanitari. Studiul inițial se efectuează în decubit dorsal sau stând cu sprijin pe spătarul unui scaun.
Protocoalele scurte de înregistrare includ de obicei teste de modulație a respirației: ținerea respirației cu o anumită frecvență și adâncime; raportul dintre durata fazelor de inspirație și expirație; teste ortostatice active și pasive; dinamometrie manuală; teste vegetative (Valsalva, cu ținerea respirației, masaj al sinusului carotidian, presiune asupra globilor oculari, teste la rece cu răcire a feței, mâinilor și picioarelor); teste farmacologice; teste mentale (exerciții de aritmetică, muzică); diverse combinații de protocoale.
Cu înregistrarea zilnică a ECG, fluctuațiile circadiene (zi-noapte) ale ritmului cardiac au un impact semnificativ asupra analizei HRV. În plus, HRV este afectată semnificativ de factori precum activitatea fizică a pacientului, diverse influențe stresante, aportul alimentar și somnul. Prin urmare, cu monitorizarea zilnică ECG, este necesar să se țină o evidență a acțiunilor pacientului și a diferiților factori care afectează ritmul cardiac. În patologie, este necesar să se determine timpul de expunere și severitatea diferitelor simptome, în special a durerii.
Contracțiile ectopice, episoadele de aritmie, interferența zgomotului și alte artefacte reduc semnificativ capacitatea analizei spectrale de a determina starea de reglare autonomă a funcției cardiace. Înainte de a calcula parametrii HRV, artefactele și extrasistolele trebuie eliminate din înregistrarea ECG. Acest lucru este posibil atunci când numărul lor relativ este mic - nu mai mult de 10% din toate intervalele R–R. Artefactele sunt considerate a fi intervale R–R, a căror durată depășește valoarea medie cu mai mult de 2 abateri standard.
Metode de analiză și indicatori determinați
Caracteristicile HRV pot fi determinate folosind multe metode diferite, fiecare dintre acestea reflectând unul dintre aspectele fenomenului studiat. De obicei, se disting următoarele grupuri de metode:
1) domeniul temporal (statistic și geometric);
2) domeniul frecvenței;
3) analiza autocorelației;
4) neliniar;
5) componente independente;
6) modelare matematică.
Metode din domeniul timpului
Studiul HRV prin metoda domeniului timp include analiza următorilor indicatori: SDNN - abaterea standard a N–N-intervale;
SDANN - SDNN înseamnă abaterea standard a segmentelor de 5 (10) minute pentru înregistrări de durată medie, de mai multe ore sau de 24 de ore;
RMSSD este rădăcina pătrată a sumei pătratelor diferenței valorilor perechilor consecutive de N–N intervale;
NN50 este numărul de perechi de intervale N–N consecutive pentru întreaga perioadă de înregistrare care diferă cu mai mult de 50 ms;
PNN50 - împărtășește NN50 din numărul total de perechi consecutive de N–N intervale care diferă cu mai mult de 50 ms, obținut pe întreaga perioadă de înregistrare.
După cum sa menționat mai sus, o metodă geometrică este, de asemenea, utilizată pentru a cuantifica HRV pe o perioadă lungă. Toate intervalele N–N pentru 24 de ore sunt prezentate sub forma unei histograme, iar apoi parametrii geometrici sunt calculați din aceasta.
Cel mai frecvent utilizat indice triunghiular HRV (indice HVR) și indice triunghiular de interpolare a histogramei N-N (TINN). Ambii indicatori sunt insensibili la diferite tipuri de erori care apar atunci când complexele QRS sunt împărțite în normale și anormale. Acest lucru reduce cerințele pentru calitatea înregistrării ECG și a analizei acesteia. Caracteristicile indicatorilor de timp sunt prezentate în tabel. 4.1.
Tabelul 4.1
Metode din domeniul frecvenței
În spectrul înregistrărilor scurte (de la 2 la 5 minute), se obișnuiește să se distingă 5 componente spectrale principale:
TH este puterea totală a spectrului;
VLF - frecvențe foarte joase în intervalul mai mic de 0,04 Hz;

LF - frecvențe joase în intervalul 0,04–0,15 Hz;
HF - frecvențe înalte în intervalul 0,15–0,4 Hz;
LF/HF - raportul LF la HF.
Caracterizarea și definirea tuturor indicatorilor spectrale sunt prezentate în tabel. 4.2.

Tabelul 4.3
În tabel. 4.3 arată corespondența dintre indicatorii temporali și spectrali ai HRV.
Analiza autocorelației
Se calculează funcția de autocorelare a unei serii de intervale R–R, care este un grafic al coeficienților de corelație obținuți prin deplasarea secvențială cu un interval R–R față de propria sa serie. După prima schimbare cu o valoare, coeficientul de corelație este cu atât mai mic decât unitatea, cu cât undele de înaltă frecvență sunt mai pronunțate. Dacă eșantionul este dominat de componente cu undă lentă, atunci coeficientul de corelație după prima schimbare este puțin mai mic decât unitatea. Deplasările ulterioare duc la o scădere treptată a coeficienților de corelație. Deoarece funcția de autocorelare și spectrul procesului sunt conectate printr-o pereche de transformate Fourier, utilizarea autocorelației sau a analizei spectrale este alegerea cercetătorului (Tabelul 4.4).
Metode de analiză neliniară
Diverse influențe asupra VRC, inclusiv mecanismele centrilor autonomi superiori, determină natura neliniară a modificărilor ritmului cardiac, ceea ce necesită utilizarea unor metode speciale pentru a descrie. Cu toate acestea, utilizarea analizei neliniare în practica clinică este limitată din cauza unui număr de factori:
1) complexitate atât în ceea ce privește analiza structurală, cât și în ceea ce privește algoritmii de calcul;
2) imposibilitatea utilizării protocoalelor scurte și necesitatea de a folosi doar înregistrări lungi pentru analiză;

Tabelul 4.4
3) absența unei baze fiziologice acumulate pentru interpretarea rezultatelor analizei neliniare.

Tabelul 4.5
Metodă independentă de analiză a componentelor
Deoarece determinarea benzilor de frecvență VLF, LF și HF în analiza spectrală a HRV este destul de arbitrară, este mai corect să se împartă HRV total în componente independente datorită diferitelor mecanisme ale sistemelor de reglementare. Această metodă aparține metodelor neliniare de analiză statistică și nu necesită înregistrarea pe termen lung a HRV.
Metoda modelării matematice
Metoda este strâns legată de metoda de analiză a componentelor independente, concentrându-se pe procesarea preliminară a semnalului HRV original cu aplicarea ulterioară a metodelor din domeniul frecvenței și a analizei neliniare. Metoda se bazează pe descrieri fiziologice ale funcționării sistemului nervos autonom.
Pentru a interpreta rezultatele analizei HRV, puteți utiliza datele privind corelațiile fiziologice ale indicatorilor HRV, prezentate în tabel. 4.6.

Tabelul 4.6
HRV la oameni sănătoși
HRV la persoanele sănătoase face posibilă evaluarea standardelor lor fiziologice, care sunt determinate de sex, vârstă, poziția corpului în spațiu, temperatura ambientală, confortul mental, ora din zi, sezonalitate și alți factori.
Indicatorii HRV sunt foarte individuali și se spune că dereglarea apare atunci când indicatorii depășesc limitele normei individuale. Nu există diferențe de gen în HRV, deși femeile au o frecvență cardiacă mai mare.
Vârsta este asociată cu o scădere a puterii totale a spectrului HRV datorită scăderii predominante a componentelor de joasă frecvență (LF) și de înaltă frecvență (HF). Deoarece scăderea LF și HF are loc sincron, raportul LF/HF se modifică puțin. Cea mai mare putere de spectru în copilărie și adolescență. Odată cu vârsta, răspunsul la modularea respirației scade, dar este asociat cu dezantrenarea fiziologică (Tabelul 4.7).
Greutatea corporală afectează și HRV: greutatea corporală mai mică se manifestă printr-un spectru de putere mai mare al HRV și HF, iar la persoanele obeze se remarcă o relație inversă. Fluctuațiile diurne (circadiene) ale HRV se manifestă printr-o putere mai mare a spectrului, VLF și LF în timpul zilei și mai puțin noaptea cu o creștere simultană a HF. Acest indicator crește la maxim în primele ore ale dimineții, în timp ce VLF fie nu se modifică, fie scade.
Exercițiile fizice și sportul duc la modificări pozitive ale HRV: ritmul cardiac scade, puterea spectrului HRV crește din cauza HF. Antrenamentul excesiv este plin de o creștere a ritmului cardiac și o scădere a HRV. Acest lucru explică parțial moartea subită, care este mai frecventă în sporturile profesioniste și asociată cu sarcini excesive.
Frecvența, adâncimea și ritmul respirator au un efect semnificativ asupra VRC; odată cu creșterea frecvenței respiratorii, contribuția relativă a HF la HRV scade și raportul LF/HF crește. Exercițiile Valsalva de respirație profundă măresc puterea spectrului HRV. Respirația ritmică crește puterea spectrului în detrimentul HF.
Valorile normale ale indicatorilor temporali și spectrale ai ritmului cardiac în funcție de vârstă sunt date în tabel. 4.7.
Diferențele în valorile indicatorilor HRV sunt, de asemenea, observate în perioadele de somn și veghe. În tabel. 4.8 prezintă indicatorii HRV la persoanele sănătoase în perioadele de somn și veghe.
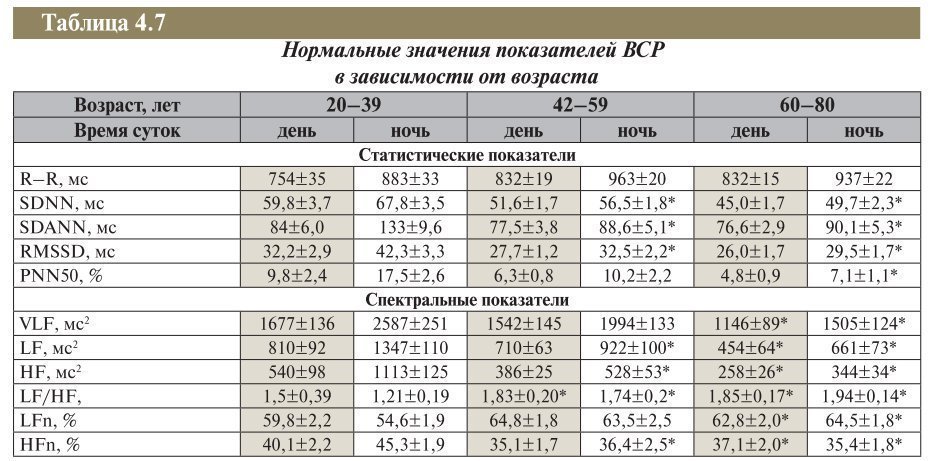
Tabelul 4.7
* Diferențele cu perioada corespunzătoare a zilei în grupul de vârstă 20–39 de ani sunt semnificative (p.<0,05).
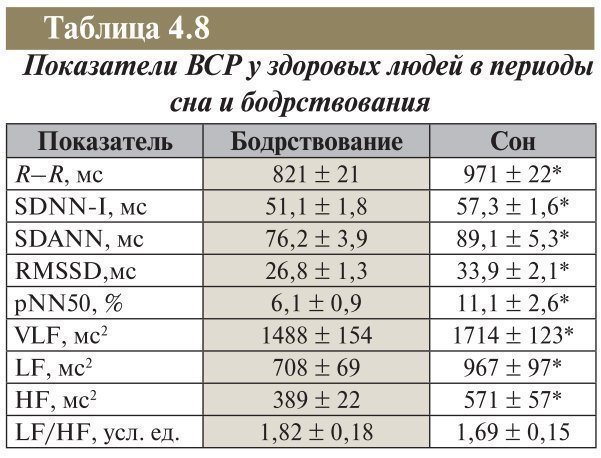
Tabelul 4.8
* Diferențele față de perioada de veghe sunt semnificative (p<0,05).
Evaluarea clinică a parametrilor HRV în diverse stări patologice
Reglarea organizată și echilibrată este cheia sănătății de calitate, crește șansele pacientului de recuperare sau remisie. Reacția sistemelor de reglare la stimuli este nespecifică, dar foarte sensibilă și, în consecință, metoda de analiză a HRV este nespecifică, dar foarte sensibilă într-o varietate de condiții fiziologice și patologice. Cu toate acestea, nu ar trebui să căutați indicatori și valori ale HRV inerente condițiilor sau formelor nosologice specifice. Având în vedere cele de mai sus, ni s-a părut interesant să luăm în considerare unele dintre trăsăturile care sunt relevate în analiza parametrilor HRV în diverse stări patologice.
Angina instabilă
Pacienții cu angină instabilă prezintă o scădere semnificativă a variabilității ritmului cardiac în timpul monitorizării zilnice ECG (SDNN, SDANN, SDNNi, RMSSD, PNN50). Scăderea indicatorilor HRV se corelează cu o scădere a segmentului ST pe ECG. Riscul de evenimente adverse (dezvoltarea IM, moarte subită) în timpul lunii este de 8 ori mai mare la valorile SDANN<70 мс.
LOR
LORcaracterizată printr-o scădere semnificativă a VRC în timpul monitorizării zilnice ECG comparativ cu CHF. Scăderea HRV în faza acută a IM se corelează cu disfuncția ventriculară, concentrația maximă a creatin fosfokinazei și severitatea AHF. Motivul pentru modificările observate în această patologie, cercetătorii văd o încălcare a relației dintre părțile simpatice și parasimpatice ale sistemului nervos. În perioada acută, se detectează o creștere a tonusului simpaticului (LF) și o scădere a tonusului sistemului nervos parasimpatic (HF). Influenţele simpatice asupra miocardului scad pragul de fibrilaţie, în timp ce influenţele parasimpatice au un caracter protector, ridicând pragul. O creștere a raportului LF/HF este determinată timp de 1 lună după MI. O scădere semnificativă a HRV în MI este un predictor independent și foarte informativ al tahicardiei ventriculare, al fibrilației ventriculare și al morții subite.
Analiza spectrală a HRV la pacienții după IM relevă o scădere a puterii totale a spectrului și a componentelor acestuia. Într-un studiu realizat de Grupul de Studiu HRV din America de Nord, au fost observați pacienți cu IM. S-a constatat că valorile scăzute ale HRV în timpul monitorizării ECG de 24 de ore se corelează cu riscul de moarte subită mai pronunțat decât valorile EF, numărul de extrasistole ventriculare și toleranța la efort. Au fost identificate valorile puterii spectrului în diferite game de frecvență asociate cu un prognostic nefavorabil al bolii: puterea totală a spectrului este mai mică de 2000 ms 2 , ULF<1600 мс 2 , VLF <180 мс 2 , LF <35 мс 2 , HF <20 мс 2 и отношение LF/HF <0,95. Низкая мощность в диапазоне VLF в большей степени, чем другие показатели, связана с возникновением внезапной аритмической смерти. Пограничными значениями выраженного снижения ВСР при оценке на протяжении 24 ч рекомендуется считать SDNN <50 мс и триангулярный индекс ВСР <15, а для умеренного снижения ВСР - SDNN <100 мс и триангулярный индекс ВСР <20.
În 1996, au fost prezentate rezultatele studiului GISSI-2, care a durat 1 mie de zile (567 de pacienți). Până la sfârșitul perioadei de observație, 52 de persoane au murit, ceea ce a însumat 9,1%. Cercetătorii au descoperit că, cu o scădere a PNN50, riscul de deces a crescut de 3,5 ori, cu o scădere a SDNN - de 3 ori, cu o creștere a RMSSD a crescut de 2,8 ori.
CH
La pacienții cu insuficiență cardiacă, este detectată o scădere semnificativă a HRV, care se datorează activării diviziunii simpatice a sistemului nervos și tahicardiei. Modificarea parametrilor de analiză a timpului HRV se corelează semnificativ cu severitatea bolii, dar modificarea parametrilor analizei spectrale nu este atât de clară. În studiul relației dintre activitatea influențelor parasimpatice asupra inimii la pacienții cu ICC și funcție VS, s-a constatat că gradul de scădere a VRC a fost asociat semnificativ cu FE. Astfel, scăderea reglării parasimpatice reflectă severitatea disfuncției sistolice.
GKMP
Cu HCM, se observă o scădere a HRV totală și a componentei sale parasimpatice. La pacienții cu această patologie, valorile LF și HF scad noaptea și se observă o valoare ridicată LF/HF comparativ cu cei sănătoși. În același timp, cele mai pronunțate valori ale componentei IC au fost găsite la pacienții cu paroxisme de tahicardie ventriculară.
Polineuropatia diabetică
Modificările HRV sunt un semn precoce (subclinic) al polineuropatiei, care face posibilă identificarea acestei afecțiuni chiar înainte de manifestarea semnelor clinice. În polineuropatia diabetică, se observă o scădere a puterii tuturor componentelor spectrale, nicio creștere a LF în timpul unui test ortostatic, un raport LF/HF „normal” și o deplasare la stânga frecvenței centrale a componentei LF.
Tulburări de ritm cardiac
Reflectând raportul dintre reglarea simpatică și parasimpatică, HRV face posibilă evaluarea riscului de aritmii care pun viața în pericol. Apariția aritmiilor ventriculare care pun viața în pericol, conform lui J.O. Valkama, este precedat de o creștere a puterii totale a spectrului, în primul rând datorită componentei sale de joasă frecvență.
În 1991, Farell și colab. au furnizat date dintr-un studiu al HRV la 416 pacienți cu aritmii. Obiectivul studiului a fost apariția tahicardiei ventriculare susținute sau a fibrilației ventriculare. S-a constatat că cu o combinație de SDNN<20 мс и желудочковой экстрасистолии более 10 в час чувствительность метода составляет 50%, а специфичность - 94%.
Medicamentele antiaritmice pot afecta HRV într-o varietate de moduri. Experimentul a arătat că o consecință hemodinamică a aritmiilor ventriculare este o modificare a activității eferente ventriculare. Prin urmare, suprimarea aritmiilor de la sine poate modifica valorile HRV. În tabel. 4.9 rezumă efectele medicamentelor antiaritmice asupra HRV.

Tabelul 4.9
Concluzie
Studiul HRV este o metodă neinvazivă, sensibilă și specifică de diagnosticare a disfuncției miocardice, o metodă de evaluare a efectului terapiei medicamentoase. Analiza indicatorilor HRV permite identificarea unui grup de pacienți cu risc crescut de moarte subită cardiacă, precum și prezicerea dezvoltării bolii.
O.S. Sychev, O.I. Zharinov „Variabilitatea frecvenței cardiace: mecanisme fiziologice, metode de cercetare, semnificație clinică și prognostică”
Toată lumea a avut zile în care bara așteaptă în mod amenințător următorul set, greutatea se apropie de un record personal, te ridici, respiri adânc... și faci exercițiul la fel de ușor ca și cum ar fi fost din plastic, nu din fier. .
Se întâmplă și altfel. Abia încălzit, încerci să faci genuflexiuni, dar greutatea nu merge. Mușchii refuză să se supună, vreau să renunț la tot și să adorm.
Diferența dintre antrenamentele reușite și cele nereușite se datorează în mare măsură stării sistemului nervos. Când îți antrenezi mușchii pentru a-i forța să se adapteze și să devină mai puternici, sistemul tău nervos este de asemenea stresat, îi face față și devine mai puternic.
Ciclul de tensiune și recuperare este foarte important pentru mușchi. De asemenea, este un factor decisiv pentru sănătatea sistemului tău nervos. Prin urmare, este atât de important să nu forțați, ci să calculați corect sarcinile și să dați corpului suficient timp pentru a se recupera.
Cum să înveți să reglezi corect acest ciclu? Ce trebuie făcut pentru ca cât mai multe zile petrecute în sală să aibă succes pentru tine?

Variabilitatea ritmului cardiac
Există multe modalități de a afla despre starea sistemului nervos, de la efectuarea unei analize detaliate a somnului până la introducerea de ace minuscule în fibrele nervoase pentru a măsura semnalul simpatic. Fiecare metodă are propriile sale merite. Cea mai simplă, mai accesibilă și mai precisă metodă este monitorizarea variației ritmului cardiac sau HRV..HRV îți permite să gestionezi obiectiv, fără a te baza pe sentimente subiective, zi după zi intensitatea antrenamentului și a recuperării. Metoda ajută la controlul individual al proceselor care asigură performanță mentală și fizică, rezistență la boli și răni.
Mai întâi, să vorbim pe scurt despre structura celor două părți principale ale sistemului nervos.
Sistem nervos anatomic controlează funcțiile vitale ale corpului, cum ar fi respirația, digestia, ritmul cardiac, tensiunea arterială și funcționarea tuturor organelor.
sistemul nervos somatic ne permite să facem sarcini zilnice, cum ar fi să ridicăm greutăți, să alergăm sau să luăm o ceașcă de cafea.
În cadrul sistemului nervos anatomic, există două subsisteme care sunt strâns legate. Unul din ei sistemul nervos simpatic. Ea este cea care, în funcție de situație, dă semnalul „fugi” sau „luptă”. Acest lucru îmbunătățește activitatea fiziologică a organismului în condiții de stres. Al doilea subsistem parasimpatic. Contracarează răspunsul organismului la semnalul sistemului nervos simpatic și contribuie la crearea condițiilor favorabile pentru odihnă și refacere. Doar nu le compara cu pedalele de gaz și de frână, pentru că nu există nicio contradicție între sisteme. Mai degrabă, ele pot fi comparate cu un spectru continuu. Acționând în mod concertat, ei schimbă doar gradul de participare.
Inima umană nu bate niciodată uniform, cu precizia unui metronom. Dimpotrivă, ritmul cardiac se modifică odată cu respirația. De fiecare dată când expirați, în câteva milisecunde, creierul trimite inimii un semnal inhibitor (supresiv) prin fibrele nervoase parasimpatice, ceea ce îi încetinește activitatea. Când inhalați, acest semnal dispare, iar semnalul simpatic crește, determinând inima să-și accelereze ușor ritmul.
Această fluctuație indică starea celor două componente ale sistemului tău nervos. Dacă sistemul parasimpatic, al cărui scop este să se „odihnească”, este foarte excitat, ritmul cardiac va fluctua foarte mult - va exista un grad ridicat de variabilitate. Dacă domină sistemul nervos simpatic, acțiunea sistemului parasimpatic slăbește și variabilitatea scade.
Acest mecanism vă permite să știți cum reacționează corpul dumneavoastră la sarcina alostatică ( reacție excesivă la stres), care obligă sistemul endocrin să mențină un echilibru homeostatic în condiții dinamice.
Reacție puternică la stres și recuperare rapidă
Nu va fi de prisos pentru orice atlet să înțeleagă ce procese fiziologice profunde se află în spatele schimbărilor vizibile din organism.Foarte des, diferența dintre un campion olimpic și cei care „au participat și ei” sau dintre un absolvent de succes care a fost selectat pentru forțele speciale și unul care a fost eliminat, se datorează tocmai proceselor nervoase.
În mod ideal, un stimul puternic ( precum concurența) provoacă un răspuns simpatic puternic la individ („fugi sau luptă”). Același răspuns parasimpatic puternic apare atunci când este timpul să vă odihniți și să vă recuperați. Acestea pot fi zile fără antrenament, perioade de descărcare sau pur și simplu pauze între runde sau meciuri.
În comparație cu concurenții de nivel inferior, sportivii de nivel olimpic și personalul forțelor speciale au atât un răspuns simpatic mai puternic în timpul competiției, cât și un impuls parasimpatic mai puternic în timpul repausului. Oscilațiile corpului lor au o amplitudine mare în ambele direcții. Au niveluri de bază mai scăzute ale hormonilor de stres și variații diurne mai mari ale nivelurilor de cortizol. Aceasta înseamnă că dimineața în corpul lor nivelul de cortizol este mult mai mare decât seara. Acest lucru permite corpului să oscileze între o excitare mai puternică în timpul zilei și o recuperare mai profundă pe timp de noapte.
Titlul de campionat vs. „diploma de participant”
În studiul Dr. Potterat, SEAL-urile au fost comparate cu soldații obișnuiți. La „foci” fluctuațiile ritmului cardiac sunt mai pronunțate. Aceasta înseamnă că în timpul somnului, când sistemul nervos parasimpatic se reface, ritmul cardiac încetinește în medie cu 29%, în timp ce la personalul militar obișnuit încetinește doar cu 21%.În „sigilii” în condiții normale ( nu într-o situație stresantă) în timpul zilei, nivelul de bază al hormonului stresului cortizol a fost mai scăzut, deși în condiții de stres în timpul parcurgerii cursului de supraviețuire, nivelul a crescut ca la toate subiecții.
Acesta este un punct foarte important. La soldații unităților de elită, în absența situațiilor stresante, impulsurile sistemului nervos parasimpatic sunt mai puternice. Capacitatea de relaxare este o calitate valoroasă!
Într-un alt studiu, a fost făcută o comparație între soldații forțelor speciale și soldații unităților convenționale în timpul antrenamentului intensiv de supraviețuire. Soldații Forțelor Speciale aflați în situații stresante, din cauza activității active a sistemului nervos simpatic, aveau un nivel mai ridicat de norepinefrină (norepinefrina a.k.a.). După finalizarea cursului de pregătire, nivelul de norepinefrină din comandouri a revenit la nivelul de bază care era înainte de antrenament. Și printre luptătorii unităților obișnuite, non-elite, nivelul a fost semnificativ mai scăzut decât cel de bază. Sistemul lor nervos simpatic era epuizat.
În cursul intensiv de pregătire a șoferilor militari, subiecții de testare cu mai mult succes au avut cele mai scăzute niveluri de variabilitate a ritmului cardiac chiar înainte și în timpul cursului. Acest lucru sugerează că atunci când vine vorba de testare, cei mai buni luptători au cel mai puternic răspuns simpatic.
Pe de altă parte, participanții cu cea mai mare variabilitate a frecvenței cardiace în acest moment au prezentat cea mai mare epuizare a puterii fizice și morale și cele mai scăzute rezultate la antrenament. După cum au emis ipoteza cercetătorilor, acești participanți au avut cel mai scăzut nivel de răspuns la „combaterea pericolului”.
Toate acestea arată cât de important este un răspuns puternic sănătos la stres și capacitatea de a vă recupera rapid după stres intens. Antrenamentul organizat corespunzător și recuperarea ulterioară ajută la dezvoltarea acestor abilități.
Sportivi și variabilitatea ritmului cardiac
Chiar dacă nu intenționați să înoți trei mile sub apă scăpând din captivitatea inamicului, aceste prevederi sunt esențiale pentru orice atlet.Reacții similare la stres în timpul competițiilor intense și responsabile au fost observate la examinarea sportivilor olimpici. În special, într-un studiu realizat de Dr. Eric Potterat ( Eric Potterat) și colegii săi de la Institutul Optibrain, care studiază fundamentele neurobiologice ale vieții în condiții extreme.
În plus, studiul variabilității ritmului cardiac a fost efectuat pe sportivi, printre care s-au numărat triatleți de putere, alergători, înotători.
Printre triatleți Oamenii de știință au descoperit o relație între HRV, putere și nivelurile hormonului dehidroepiandrosteron (DHEA) ( un hormon necesar restabilirii sistemului nervos). După o sesiune de antrenament de forță de 2 ore care a inclus ridicarea a 95% din maxim 1 repetare, sportivii au fost urmăriți pentru o perioadă de recuperare de 72 de ore.
Nivelurile de forță, HRV și DHEA au scăzut după antrenament. Până la sfârșitul perioadei de 72 de ore, aceste niveluri și-au revenit la linia de bază inițială și au crescut ocazional și au crescut la un nou nivel. (Vezi graficele de mai jos).
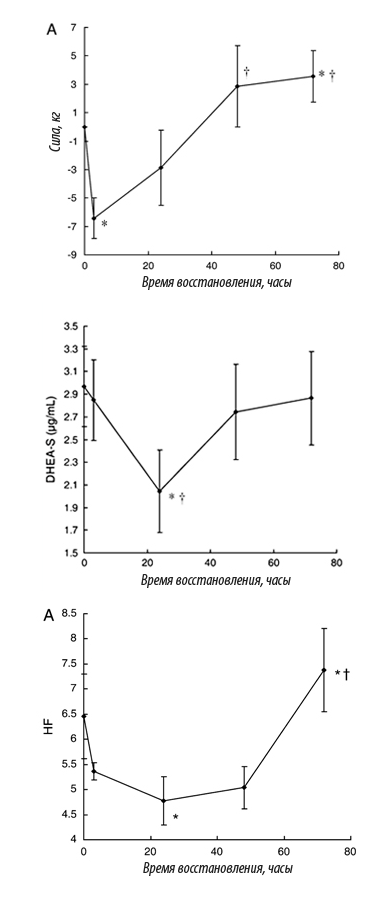
* „HF” în ultimul grafic este puterea semnalului parasimpatic.
Aceasta ilustrează procesul de recuperare neuronală care are loc după un antrenament intens. Stresul inițial al antrenamentului a contribuit la creșterea puterii semnalului simpatic și la scăderea nivelului de DHEA de protecție. Când a început procesul de recuperare și a existat o reducere a iritației, și nivelurile HRV și DHEA s-au recuperat.
Pe parcursul experimente cu alergători la distante medii, sportivii s-au antrenat mai intai intens timp de trei saptamani, apoi a avut loc o descarcare saptamanala. Odată cu acumularea sarcinii alostatice ca urmare a antrenamentului, sportivii au avut o scădere cu 40% a variabilității ritmului cardiac.
În perioada de recuperare, schimbarea s-a produs în sens invers și, ca urmare, sportivii au experimentat o creștere absolută a HRV. Aceasta a confirmat ipoteza că repetele „ perioade consecutive de antrenament de intensitate mare și scăzută pot duce la o creștere progresivă a activității în principal parasimpatice, care s-a dovedit deja a fi direct legată de valori mai mari ale VO2 MAX (consumul maxim de oxigen)».
Interesant este că în timpul experimentului a fost măsurată și ritmul cardiac al sportivilor în repaus. În timpul experimentului, schimbarea a fost de numai aproximativ 10% (aproximativ patru bătăi pe minut). Dar ritmul cardiac în repaus este afectat de un număr mare de factori variabili. În plus, amploarea schimbărilor a fost relativ mică. De aceea ritmul cardiac de repaus este foarte greu de evaluat starea de sănătate a sistemului nervos.
HRV și inflamație cronică, cortizol, glucoză, imunitate și patologia țesuturilor moi
Variabilitatea ritmului cardiac este o măsură fiabilă a inflamației sistemice, a creșterii cronice a nivelurilor hormonului de stres, a modificărilor absorbției de glucoză, a stării imunitare și a leziunilor țesuturilor moi.„Scăderea funcției vagale și variabilitatea ritmului cardiac (HRV) s-a dovedit a fi asociate cu creșterea glicemiei și hemoglobinei A1c, creșterea cortizolului urinar nocturn și creșterea activității citokinelor proinflamatorii și a proteinelor de fază acută. Și toți acești factori indică o creștere a încărcăturii alostatice și o sănătate precară.” Thayer și Sternberg, Neuroendocrine și Immune Crosstalk, volumul 1088, 2006.
Numeroase studii care implică înotători au arătat relația dintre HRV și boală, precum și între HRV și leziunile țesuturilor moi.
Practic, cu câteva zile înainte de îmbolnăvire sau rănire, s-a observat o creștere a HRV, iar direct în timpul bolii sau leziunii, variabilitatea ritmului cardiac a scăzut, iar tonusul sistemului nervos simpatic a crescut.
Potrivit cercetătorilor, cea mai probabilă explicație pentru creșterea pe termen scurt a variabilității ritmului cardiac înainte de îmbolnăvire este că sistemul parasimpatic își crește activitatea ca răspuns la agentul patogen imediat, în încercarea de a preveni răspândirea infecției și a inflamației.
După o perioadă de incubație de aproximativ cinci zile, când acțiunile antiinflamatorii ale sistemului parasimpatic nu pot împiedica procesul patogen, agentul patogen preia controlul. Acest lucru duce la o creștere bruscă a inflamației activate de sistemul simpatic și la o scădere a tonusului sistemului nervos parasimpatic.
Cum se măsoară HRV?
 Pentru a determina diferența dintre activitatea sistemului parasimpatic și cel simpatic, segmentele dintre undele R sunt măsurate pe electrocardiogramă ( sau diferența de timp între bătăile inimii). Deoarece ambele subsisteme controlează activitatea inimii și folosesc aceleași căi pentru a face acest lucru, această măsurătoare oferă o indicație precisă a echilibrului sistemului dumneavoastră nervos autonom.
Pentru a determina diferența dintre activitatea sistemului parasimpatic și cel simpatic, segmentele dintre undele R sunt măsurate pe electrocardiogramă ( sau diferența de timp între bătăile inimii). Deoarece ambele subsisteme controlează activitatea inimii și folosesc aceleași căi pentru a face acest lucru, această măsurătoare oferă o indicație precisă a echilibrului sistemului dumneavoastră nervos autonom. Utilizarea HRV în controlul și recuperarea sarcinii
Pentru a profita de această metodă, este necesar să înțelegem cum reacționează organismul la stres, adică. pentru activitate fizică. Aceasta înseamnă, desigur, că sarcina la care trebuie să răspundă organismul va fi adecvată.Conform Sindromului General de Adaptare (GAS) al lui Hans Selye, organismul trece prin trei etape de răspuns la stres:
„Șoc” sau „Stadiul anxietății”
aceasta este prima reacție a unui organism sănătos la un nou stimul. În această etapă:
HRV scăzut
aferent ( centripet, spre creier) semnalele provoacă un eferent ( îndreptată spre periferie) efecte asupra sistemelor nervos și hormonal și asupra neuronilor motori.
Organismul reacționează prin creșterea tonusului sistemului nervos simpatic.
Niveluri crescute de hormoni de stres CRH și ACTH)
Eliberare crescută de adrenalină, norepinefrină și cortizol
Următoarea etapă este „Supratensiune” sau „Etapa de rezistență”
, care este răspunsul organismului la un dezechilibru între sarcina de antrenament și recuperare.
O scădere a densității receptorilor beta-2 adrenergici reduce răspunsul glandelor suprarenale la hormonul de stres ACTH (corticotropină).
SNC răspunde la scăderea răspunsului suprarenal prin creșterea producției de hormoni de stres.
Ton simpatic în timpul stresului ( a face exerciţii fizice) crește.
Tonul parasimpatic crește în timpul recuperării.
Prin creșterea răspunsului antiinflamator al sistemului parasimpatic, variabilitatea ritmului cardiac crește.
Scăderea turnover-ului proteinelor contractile adică, recuperarea încetinește).
Cortizolul și alți hormoni de stres rămân crescuti.
A treia etapă se numește „stresul cronic” „Etapa de supraantrenament”
sau „Epuizare”. Această etapă apare dacă organismul nu se adaptează mult timp la stresul cronic.
SNC oprește producția de hormoni de stres.
Glandele suprarenale încă nu răspund la hormonul de stres ACTH.
Reacția sistemului simpatic este slăbită.
HRV rămâne ridicată datorită unui răspuns cronic crescut al sistemului nervos parasimpatic.
Concentrație crescută de cortizol.
Scăderea fluctuației diurne a nivelului de cortizol.
Încetinirea mai puțin pronunțată a ritmului cardiac pe timp de noapte.
Niveluri scăzute de testosteron și alți markeri anabolizanți.
Simptome psihologice de „burnout” ( epuizare emoțională).
Scăderea sintezei proteinelor (recuperarea întârziată după lezarea țesutului muscular).
Scăderea imunității.
Activitate crescută a inflamației sistemice.
„Supercompensare” sau "Recuperare" este etapa de descărcare. Dacă nu ați ajuns la etapa #3 „Supraantrenament”, veți avea nevoie doar de aproximativ o săptămână pentru a vă recupera. În epuizare severă, recuperarea completă poate dura câteva luni.
HRV scade la valoarea inițială ( nivelul de bază poate crește dacă sistemul de antrenament vizează exercițiul aerobic).
Nivelurile de cortizol scade la valoarea de bază în repaus.
Fluctuațiile zilnice ale nivelului de cortizol cresc.
Sistemul nervos central raspunde la stimuli puternici prin cresterea concentratiei hormonului de stres.
Glandele suprarenale restabilesc concentrația de adrenoreceptori Beta 2 și sensibilitatea la hormonii centrali.
Inflamația este redusă.
Nu-ți distruge corpul!
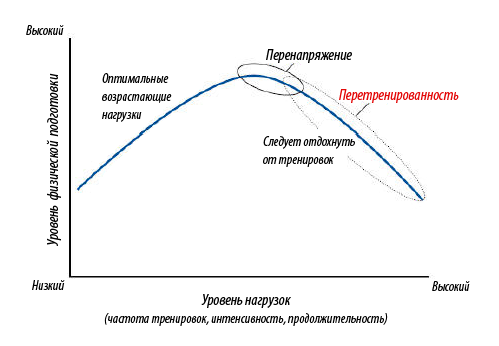
Nu trebuie să treci prin toate cele trei etape ale Sindromului General de Ajustare pentru a profita de etapa de supracompensare. Modul ideal este să ajungeți la a doua etapă și apoi să descărcați. Graficul arată procesul de acumulare a stresului și efectul acestuia asupra rezistenței.
Cum să monitorizezi singur HRV?
Există mai multe moduri, de la utilizarea sistemului Omegawave de mii de dolari până la software pentru smartphone și un simplu monitor de ritm cardiac. Vom lua în considerare a doua metodă.Cea mai cunoscută aplicație este Ithlet (plătit) A fost prima aplicație accesibilă și simplă de acest gen pentru smartphone-uri. De asemenea, va trebui să cumpărați un receptor care acceptă semnale de la un monitor analog al ritmului cardiac și o aplicație. Doar conectați totul și inspirați și expirați timp de 60 de secunde în fiecare dimineață. Aplicația vă va monitoriza HRV și va afișa datele într-un grafic.
Programul va reflecta nivelul relativ al VRC pentru ziua, pentru saptamana sau pentru luna. Modificările sunt evidențiate în culoare. Albastru sau verde indică nicio modificare sau pozitivă a HRV, galbenul indică o scădere ușoară, iar roșu indică o scădere semnificativă.
Ideea este să, concentrându-vă pe culoare, să determinați intensitatea antrenamentului. Dacă vezi galben, atunci totul este în regulă. Dacă modificările sunt „înroșite”, ar trebui să vă odihniți o zi. Culoarea verde sau albastră indică faptul că nu te străduiești suficient.
Această metodă are anumite limitări. Nu determină în mod fiabil creșterea VRC cauzată de supraîncărcare în etapa 2. Cu alte cuvinte, programul nu recunoaște în mod fiabil dacă creșterea VRC este cauzată de acumularea de stres și trecerea la etapa #2 „Suprasolicitare” sau insuficientă. antrenament și recuperare după etapa #1.
Există o altă aplicație numită Bioforce. Se ține cont de deficiențele descrise mai sus. Cu Bioforce, puteți vedea motivul creșterii HRV și puteți înțelege ce este: stres sau recuperare. Costă mult mai mult decât Ithlete.
Ce să faci cu rezultatele?
Iată cum să folosiți datele în mod adecvat. Mai întâi, stabiliți-vă linia de bază.Faceți o descărcare, întrerupeți programul de antrenament curent timp de 7 până la 10 zile. Apoi creați un nou program și măsurați timp de 4 până la 6 săptămâni.
Păstrați un jurnal detaliat de antrenament, care să descrie fiecare antrenament (exercițiu, greutate, număr de seturi, repetări, odihnă), nutriție, durata și calitatea somnului, metodele de recuperare și calitatea antrenamentului (motivație, starea de spirit).
La sfârșitul programului de antrenament, descărcați timp de 7 până la 10 zile.
Când este gata un jurnal detaliat de 4-6 săptămâni de antrenament, puteți să vă așezați, să priviți cu atenție totul și să determinați linia de bază. Acest lucru va ajuta la înțelegerea sensului măsurătorilor zilnice. Ar trebui să vedeți cum se corelează intensitatea antrenamentului, calitatea recuperării (în special somnul) și tendința generală a HRV se modifică pe parcursul întregului ciclu de antrenament pe măsură ce treceți prin etapele de adaptare generală la stres.
În timp, acest lucru vă va ajuta să înțelegeți mai bine modul în care organismul dumneavoastră răspunde la stres și cum să gestionați procesul de recuperare pentru a obține un progres optim.
In cele din urma
Chiar dacă scopul antrenamentului nu este realizări înalte și participarea la competiții, ar trebui să te străduiești să reușești în antrenament. Măsurarea variabilității ritmului cardiac este o modalitate simplă și relativ ieftină de a monitoriza starea sistemului neuroendocrin pentru persoanele care duc un stil de viață activ.Înțelegând cum funcționează sistemul dumneavoastră nervos, veți deveni mai puternic, veți intra în formă excelentă și veți evita rănile și bolile.
Acest articol nu este o reclamă pentru anumite programe și produse. Scopul nostru este să vă familiarizăm cu metodele moderne de autodiagnosticare a stării corpului. A te baza pe propriile sentimente și a-ți asculta corpul nu strica niciodată, dar dacă poți vedea informațiile sub formă de numere și grafice, cu siguranță nu vor fi de prisos!
Această secțiune a fost scrisă de Prof. Dr. med. R.M. Baevski
Introducere
Analiza variabilității ritmului cardiac este o metodologie și o tehnologie modernă pentru studierea și evaluarea stării sistemelor de reglare ale corpului, în special a stării funcționale a diferitelor părți ale sistemului nervos autonom. Studiile privind variabilitatea ritmului cardiac (HRV) au fost începute în URSS la începutul anilor ’60 simultan în medicina spațială (R.M. Baevsky, O.G. Gazenko, 1963) și în practica clinică (D. Zemaityte, 1965). În 1966, la Moscova a avut loc cel de-al 1-lea Simpozion al întregii uniuni privind analiza matematică a ritmului cardiac, la care au fost prezentate peste 50 de rapoarte (V.V. Parin, R.M. Baevsky, 1968). Cel de-al doilea simpozion al întregii uniuni a avut loc în 1977 și la acesta au fost deja prezentate peste 300 de rapoarte. În țara noastră, în anii 60 - 70, au fost efectuate studii ample folosind analiza matematică a ritmului cardiac în cardiologie, chirurgie, fiziologia muncii și sportului, fiziologia experimentală, datorită cărora s-au dezvoltat idei despre semnificația indicatorilor de echilibru autonom. pentru evaluarea reacțiilor adaptative nespecifice. Aceste idei au fost rezumate în monografia „Analiza matematică a modificărilor ritmului cardiac sub stres” (R.M. Baevsky, O.I. Kirillov, S.Z. Kletskin, 1984) și apoi au fost dezvoltate în continuare în dezvoltarea problemelor de diagnostic prenosologic (A.P. Berseneva, 1991, R.M. , A.P. Berseneva, 1993-1997). În 1985 și 1989 în URSS au fost publicate recomandări metodologice pentru analiza matematică a ritmului cardiac.
În Europa de Vest și SUA, studiul HRV a fost dezvoltat abia la sfârșitul anilor 1970 și începutul anilor 1980. Această direcție se dezvoltă în mod deosebit activ în prezent. Zeci de lucrări despre variabilitatea ritmului cardiac sunt publicate lunar. Nici un singur congres sau simpozion cardiologic nu este complet fără o discuție despre această problemă. În 1996, un grup de experți de la Societatea Europeană de Cardiologie și de la Societatea Nord-Americană de Electrofiziologie (Task Forse) au dezvoltat linii directoare (standarde) pentru măsurarea, interpretarea fiziologică și utilizarea clinică a variabilității ritmului cardiac (Circulation, 93:1043-1065). ,1996). Aceste recomandări iau în considerare separat studiile pe termen scurt ale variabilității ritmului cardiac (înregistrări pe termen scurt) și datele din înregistrările zilnice de 24 de ore (înregistrări pe termen lung).
În ultimul deceniu s-au format în țara noastră și în străinătate diferite abordări ale analizei HRV, care, însă, nu se contrazic. În general, HRV este considerată ca rezultat al activării diferitelor mecanisme de reglare care asigură menținerea homeostaziei cardiovasculare. În prezent, semnificația științifică și aplicată a metodelor de analiză HRV este în general recunoscută, iar în fiecare an acestea devin din ce în ce mai răspândite. Îmbunătățirea continuă a metodologiei de studiu HRV este asociată cu dezvoltarea rapidă a tehnologiei informatice. În fiecare an apar noi concepte pentru evaluarea HRV. Cu toate acestea, există deja metode și abordări bine testate și dovedite.
Aceste ghiduri sunt pregătite ca unul dintre documentele pentru complexul hardware-software „Varicard”, dar pot fi utilizate și independent, de către toți cei care utilizează metode de cercetare HRV în munca lor. Recomandările se aplică numai analizei înregistrărilor pe termen scurt cu o durată de bază de 5 minute. Analiza înregistrărilor zilnice ale cardiointervalelor (înregistrări pe termen lung) are propriile sale specificități și necesită o abordare conceptuală diferită. Cu toate acestea, fragmente individuale din înregistrarea zilnică pot fi analizate și folosind tehnicile descrise aici.
La pregătirea recomandărilor metodologice, am considerat că primul complex hardware și software disponibil comercial pentru analiza și evaluarea HRV ar trebui să ofere, în primul rând, implementarea unor metode bine cunoscute și bine dovedite, precum și posibilitatea dezvoltării ulterioare. de instrumente software pe măsură ce apar din ce în ce mai multe metode noi de analiză HRV. În același timp, setul de bază de programe ar trebui să se bazeze, în primul rând, pe experiența acumulată în țara noastră, ținând cont de ultimele realizări ale oamenilor de știință străini.
Fundamente teoretice pentru analiza variabilității ritmului cardiac
Medicina spațială a fost unul dintre primele domenii ale științei și practicii, în care analiza HRV (analiza matematică a ritmului cardiac) a fost folosită pentru a obține noi informații științifice și a rezolva problemele de control medical asupra astronauților (Baevsky R.M., 1970). În același timp, reacțiile sistemului circulator și, în special, mecanismele sale de reglare au fost considerate ca rezultat al adaptării organismului la un număr mare de diverși factori de mediu. În acest sens, în urmă cu mai bine de un sfert de secol, s-a format conceptul de sistem cardiovascular ca indicator al reacțiilor adaptative ale întregului organism (VV Parin și colab., 1967). Implementarea practică a acestui concept sub forma unei metodologii și tehnologie specifice pentru măsurătorile de diagnosticare este caracterizată de o serie de avantaje importante. În primul rând, metode bine-cunoscute și disponibile public pentru măsurarea nivelului de funcționare a sistemului circulator (volumul minute și stroke, frecvența pulsului, tensiunea arterială). În al doilea rând, pentru a evalua sistemul de reglare autonomă a inimii și a vaselor de sânge, pot fi folosite date privind variabilitatea parametrilor hemodinamici, dintre care ritmul cardiac este cel mai simplu și mai accesibil pentru analiză. Dispozitive cu receptori sensibili - baro- și chemo-receptorii controlează diferiți parametri ai circulației sângelui în diferite puncte ale patului vascular și în inima însăși și informează constant sistemul nervos central despre modificările care au loc. Aceasta oferă flexibilitate pentru adaptarea inimii și a vaselor de sânge la condițiile de mediu în continuă schimbare ca urmare a activității mecanismelor de reglare perfecte. Astfel, prin controlul activității mecanismelor de reglare a circulației sanguine, obținem efectiv informații despre adecvarea răspunsului mecanismelor adaptative la diferite efecte ale schimbării condițiilor de mediu. În al treilea rând, sunt bine cunoscute mecanismele compensatorii care asigură adaptarea sistemului cardiorespirator la schimbările din mediu. Acestea includ o varietate de mecanisme reflexe, o creștere a ventilației pulmonare, viteza fluxului sanguin, consumul de oxigen, hiperfuncția inimii, optimizarea proceselor metabolice în țesuturi etc. Toate aceste mecanisme, ca verigi ale unui singur sistem funcțional, acționează în cele din urmă spre obtinerea rezultatului final – mentinerea homeostaziei cardiovasculare. În consecință, este posibil, folosind metode adecvate de analiză, să se evalueze nu numai rezultatul reacției adaptative a organismului, ci și să se identifice gradul de participare la această reacție a diferitelor niveluri și legături ale mecanismului de reglementare.
Sistemele de reglare ale corpului sunt un aparat care funcționează constant pentru monitorizarea stării tuturor sistemelor și organelor, a interacțiunii lor și a menținerii unui echilibru între organism și mediu. Activitatea sistemelor de reglare depinde de starea funcțională a organismului. Este posibil să se distingă condiționat trei niveluri de activitate ale sistemelor de reglementare: 1) nivelul de control, 2) nivelul de reglementare, 3) nivelul de control (Parin V.V., Baevsky R.M., 1966). În condiții normale, când sistemul reglat (controlat) funcționează în modul normal, fără a experimenta sarcini suplimentare, mecanismul de reglare îndeplinește numai funcții de control, adică. primește informații despre starea sistemului reglementat și nu interferează cu funcționarea acestuia. Dacă apar sarcini suplimentare, dacă sistemul reglementat trebuie să mărească consumul de energie pentru a-și îndeplini funcțiile, atunci mecanismul de reglare trece la un alt mod de funcționare - „intervine” în procesul de control și îl corectează: ajutând sistemul reglementat să funcționeze funcțiile sale. Totodată, putem vorbi despre trecerea mecanismului de reglementare la nivelul de reglementare. În acest caz, prin canalele nervoase și umorale corespunzătoare, semnalele de control sunt transmise către sistemul reglementat, asigurând mobilizarea rezervelor funcționale suplimentare necesare. Dacă rezervele proprii ale sistemului reglementat sunt insuficiente pentru a obține efectul dorit, atunci mecanismele de reglare intră în modul de control. Aici, activitatea acestora crește semnificativ, întrucât alte niveluri superioare de reglementare trebuie conectate la procesul de management, care asigură mobilizarea rezervelor funcționale ale altor sisteme. În funcție de cele trei niveluri de activitate, tensiunea mecanismelor de reglare (activitatea acestora) crește. Astfel, în funcție de gradul de tensiune al mecanismelor de reglare, se pot judeca rezervele funcționale ale sistemului circulator și capacitățile adaptative ale întregului organism.
Gradul de tensiune al sistemelor de reglare este un răspuns integral al organismului la întregul complex de factori care îl afectează, indiferent cu ce sunt asociate. Sub influența unui complex de factori de natură extremă, apare un sindrom general de adaptare (G. Selye, 1960), care este un răspuns universal al organismului la efectele stresante de orice natură și acest sindrom se manifestă în același mod ca și mobilizarea rezervelor funcţionale ale organismului. Un organism sănătos, având o rezervă suficientă de capacități funcționale, răspunde la efectele stresante cu obișnuit, normal, așa-numitul stres de lucru al sistemelor de reglementare. Deci, de exemplu, dacă trebuie să urcăm scările, atunci, în mod natural, costurile cu energia cresc și trebuie mobilizate resurse suplimentare. Cu toate acestea, pentru unii oameni, o astfel de mobilizare nu este însoțită de o tensiune semnificativă în sistemele de reglementare, iar pulsul la urcarea, de exemplu, la etajul 5, crește cu doar 3-5 bătăi, adică. homeostazia cardiovasculară rămâne practic neschimbată. Pentru alte persoane, această sarcină este prea mare și există o tensiune pronunțată în sistemele de reglare cu o creștere a ritmului cardiac cu 15-20 sau mai multe bătăi: ceea ce indică deja prezența tulburărilor de homeostazie.
Chiar și în repaus, tensiunea sistemelor de reglementare poate fi mare dacă o persoană nu are suficiente rezerve funcționale. Acest lucru se exprimă, în special, în stabilitatea ridicată a ritmului cardiac, caracteristică tonului crescut al diviziunii simpatice a sistemului nervos autonom. Acest departament al mecanismului de reglare, care este responsabil pentru mobilizarea de urgență a resurselor energetice și metabolice în orice fel de stres, este activat prin canalele nervoase și umorale. Este un element integral al sistemului hipotalamo-hipofizo-adrenocorticotrop care implementează răspunsul organismului la stres. Un rol important în acest sens revine sistemului nervos central, care coordonează și dirijează toate procesele din organism.
Inima este un indicator foarte sensibil al tuturor evenimentelor care au loc în organism. Ritmul contracțiilor sale, reglat prin diviziunile simpatic și parasimpatic ale sistemului nervos autonom, este foarte sensibil la orice stres. Nu este o coincidență că diagnosticul pulsului ocupă un loc atât de important în medicina chineză. Medicii antici din China și Tibet au putut să pună un diagnostic, să prescrie tratament și să prezică cursul bolilor pe baza simțirii pulsului. Forța și ritmul contracțiilor inimii poartă informații despre starea sistemelor care le reglează. Astăzi, într-o oarecare măsură, am învățat deja, folosind dispozitive electronice și instrumente de calcul, să obținem, pe baza analizei ritmului cardiac, date obiective privind starea sistemelor simpatic și parasimpatic, interacțiunea acestora și la niveluri superioare de reglare în centrii subcorticali și cortexul cerebral.
Este posibil să se judece gradul de tensiune al sistemelor de reglare folosind mai multe metode: prin studierea conținutului de hormoni adrenalină și norepinefrină din sânge, prin modificarea diametrului pupilei, după cantitatea de transpirație etc. etc. Dar cea mai simplă și mai accesibilă metodă și, cel mai important, care permite controlul dinamic continuu, este o analiză matematică a ritmului cardiac. Modificările ritmului cardiac sunt o reacție operațională universală a întregului organism ca răspuns la orice influență a factorilor de mediu. Cu toate acestea, frecvența cardiacă medie măsurată în mod tradițional reflectă doar efectul final al numeroaselor influențe reglatoare asupra aparatului circulator, caracterizează trăsăturile mecanismului homeostatic deja stabilit. Una dintre sarcinile importante ale acestui mecanism este de a asigura un echilibru între diviziunile simpatice și parasimpatice ale sistemului nervos autonom (homeostazia vegetativă). Aceeași frecvență a pulsului poate corespunde diferitelor combinații de activități ale legăturilor sistemului care controlează homeostazia autonomă. În plus, nivelurile mai ridicate de reglare afectează și ritmul cardiac. Acest lucru dă motive să se considere nodul sinusal ca un indicator sensibil al reacțiilor adaptative ale corpului în procesul de adaptare la condițiile de mediu.
În fiecare moment al vieții sale, organismul experimentează o influență continuă a factorilor care deviază echilibrul într-o direcție sau alta. În același timp, intră în joc mecanisme de reglementare care previn sau compensează schimbările deja apărute sau emergente. În acest sens, este firesc ca problema homeostaziei să fie cel mai strâns legată de problema adaptării organismului la condițiile de mediu în schimbare, la cerințele impuse unui sistem viu în condiții de stres. Compararea rezultatelor unui număr mare de observații și studii clinice și clinico-fiziologice arată că unele tulburări în funcționarea normală a organismului pot fi privite ca un tip special de patologie - „boala homeostaziei” (Kassil, 1966). Acestea includ afecțiuni cauzate de insuficiența, excesul sau inadecvarea sistemelor adaptative ale corpului. Cu o anumită convenționalitate, acestea ar trebui să includă disfuncția asociată procesului de îmbătrânire, unele tulburări funcționale, epuizarea sistemului nervos, aparatul endocrin, boli precum disfuncția autonomă etc. (Grașcenkov, 1964; Kassil, 1966; Horizontov, 1976).
Mecanisme de reglare a ritmului cardiac
Principalele informații despre starea sistemelor care reglează ritmul cardiac este conținută în „funcția de împrăștiere” a duratelor intervalelor cardio. Aritmia sinusală reflectă procesele complexe de interacțiune dintre diferitele circuite de reglare a frecvenței cardiace. Cel mai simplu model este un model cu două bucle de reglare a frecvenței cardiace (Baevsky R.M., 1968). S-a bazat pe o abordare cibernetică, în care sistemul de control al nodului sinusal a fost prezentat sub forma a două circuite interconectate: central și autonom, controlat și controlat cu canale directe și de feedback. Dacă reprezentăm sistemul de control al ritmului cardiac sub forma a două circuite, așa cum se arată în Figura 1, atunci pe baza datelor cunoscute privind componentele respiratorii și non-respiratorii ale ritmului cardiac, pot fi luate în considerare următoarele prevederi.
Figura 1. Model cu două bucle de reglare a ritmului cardiac
Nodul sinusal, nervii vagi și nucleii lor din medula oblongata sunt organele de lucru ale circuitului de reglare controlat (inferior, autonom). Un indicator al activității acestui circuit este o aritmie sinusală respiratorie. În acest caz, sistemul respirator poate fi considerat ca un element de feedback într-un circuit autonom de reglare a frecvenței cardiace. Circuitul de reglare (superior, central) este caracterizat de diferite componente cu unde lente ale ritmului cardiac. Indicatorul său este aritmia sinusală non-respiratorie. O conexiune directă între circuitele de control și controlat se realizează prin canalele nervoase (în principal simpatice) și umorale. Feedback-ul este asigurat și de căile nervoase și umorale, dar un rol important îl au impulsurile aferente de la baroreceptorii inimii și ai vaselor de sânge, de la chemoreceptori și din zonele extinse de receptori ale altor organe și țesuturi.
Circuitul controlat în repaus funcționează într-un mod autonom, care se caracterizează prin prezența unei aritmii respiratorii pronunțate. Undele respiratorii cresc în timpul somnului sau în timpul anesteziei, când influențele centrale asupra circuitului de reglare autonomă scad. Diverse sarcini asupra corpului, care necesită includerea unui circuit central de reglare în procesul de control al ritmului cardiac, duc la o slăbire a componentei respiratorii a aritmiei sinusale și la o creștere a componentei sale non-respiratorii. Tiparul general este că nivelurile mai mari de control inhibă activitatea nivelurilor inferioare. În același timp, amplitudinea undelor respiratorii ale ritmului cardiac scade mai mult, cu atât mai activ este inclus circuitul central (de control) în procesul de control. Întrucât circuitul autonom este în esență circuitul reglării parasimpatice, centralizarea controlului înseamnă o schimbare a homeostaziei autonome către predominanța reglării nervoase simpatice. Prin urmare, slăbirea aritmiei respiratorii este de obicei asociată cu o creștere a tonusului diviziunii simpatice a sistemului nervos autonom.
Circuitul de control sau central pentru controlul frecvenței cardiace reprezintă toate „etajele” controlului neuroumoral al funcțiilor fiziologice de la centrii subcorticali ai medulei oblongate până la nivelul hipotalamo-hipofizar de reglare autonomă și nivelul influențelor corticale asupra funcțiilor autonome. Circuitul central poate fi reprezentat schematic ca fiind format din trei niveluri. Aceste niveluri corespund nu atât structurilor anatomice și morfologice ale creierului, cât anumitor sisteme funcționale sau niveluri de control care se formează în procesul de control al funcțiilor fiziologice ale corpului:
Nivelul de menținere a homeostaziei intrasistemice, în special în sistemul cardiorespirator. Aici rolul principal îl au centrii nervoși subcorticali, în special centrul vasomotor ca parte a centrului cardiovascular subcortical, care are un efect stimulator și inhibitor asupra inimii prin fibrele nervilor simpatici (nivel B);
Nivelul care echilibrează diferitele sisteme ale corpului între ele și asigură homeostazia intersistemului. Partea principală în activitatea acestui nivel de control este ocupată de centrii vegetativi superiori (inclusiv sistemul hipotalamo-hipofizar), care asigură homeostazia hormonal-vegetativă (nivel B);
Nivelul de organizare al interacțiunii organismului cu mediul extern (activitatea adaptativă a organismului). Acest nivel include sistemul nervos central, inclusiv mecanismele corticale de reglare, care coordonează activitatea funcțională a tuturor sistemelor corpului în conformitate cu influența factorilor de mediu (nivelul A).
Cu o reglementare optimă, managementul are loc cu participarea minimă a nivelurilor superioare de management, cu o centralizare minimă a managementului. Cu un control suboptim, este necesară activarea unor niveluri tot mai înalte de control. Aceasta se manifestă sub forma unei slăbiri a aritmiei respiratorii și a unei creșteri a componentei non-respiratorii a aritmiei sinusale, apariția undelor lente de ordin tot mai înalt. Cu cât sunt activate niveluri mai ridicate de control, cu atât perioada undelor lente corespunzătoare ale ritmului cardiac este mai lungă (RM Baevsky, 1978).
Aritmia respiratorie sinusală a fost descoperită în ultimul secol (Ludwig, 1847). Nu există un consens cu privire la originea aritmiei respiratorii, deși majoritatea cercetătorilor consideră că este un fapt incontestabil că respirația influențează ritmul inimii și participarea activă la acest proces a nucleilor nervilor vagi, a căror inhibare și excitare este transmisă nodul sinusal prin terminațiile nervoase corespunzătoare, determinând o scurtare a duratei intervalelor cardiace în timpul inspirației și prelungirea la expirație (Ludwig, 1847; Fogelson, 1951; Kingisepp și Epler, 1968). Conform lui Sayers (1973), respirația afectează durata cardiociclurilor prin presiunea interpleurală și activitatea baroreceptorilor. M. Klimes (1963) a dezvoltat un model de reglare respiratorie a ritmului cardiac. Acest model se bazează pe poziția teoriei controlului automat și interpretează relația dintre respirație și magnitudinea inhibării „vagale” a inimii cu ajutorul funcțiilor de transfer construite pe curbe reale ale proceselor tranzitorii ale ritmului cardiac în timpul inhalării și expiraţie.
Aritmiile sinusale non-respiratorii sunt fluctuații ale ritmului cardiac cu perioade mai mari de 6-7 secunde (sub 0,15 Hz). Fluctuațiile lente (non-respiratorii) ale frecvenței cardiace se corelează cu tensiune arterială similară și unde pletismografice. Există valuri lente de ordinul 1, 2 și superior.
Nivelul de cunoștințe existent nu ne permite să indicăm cu exactitate sursa de origine a fiecăruia dintre tipurile de unde lente. Syers (1973) consideră că undele lente ale ritmului cardiac de ordinul întâi (cu o perioadă de 7 până la 20 de secunde) sunt asociate cu activitatea sistemului de reglare a tensiunii arteriale, iar undele de ordinul doi (cu o perioadă de 20 până la 70 de secunde) sunt asociate cu sistemul de termoreglare. Se presupune că oscilațiile cu o perioadă mai mare de 20 de secunde sunt determinate de caracteristicile mecanice ale mușchilor netezi vasculari. Neliniaritatea acestui sistem mecanic și posibilitatea de interferență a oscilațiilor lente cu cele respiratorii sunt subliniate, mai ales la adâncimea mare a respirației, în special, în timpul stresului mental și fizic.
S-a demonstrat că la sportivii cu un nivel scăzut de capacitate de muncă, precum și la indivizii neantrenați, în repaus, apariția periodicelor cu unde lente este mult mai des observată (V.I. Vorobyov, 1978). Kepezhenas și Zemaitite (1983) au observat o schimbare a tipului de ritmografie cu o tranziție de la un ritm cu o amplitudine mare a undelor respiratorii la o predominanță a undelor lente în timpul efortului fizic prelungit și cu o scădere a aptitudinii sportivilor.
Înregistrările scurte cu o durată de până la 5 minute fac posibilă detectarea doar a ritmurilor cu perioade nu mai mari de 1,5-2 minute. Cu toate acestea, cu o înregistrare mai lungă a ritmului cardiac, se observă fluctuații cu perioade de minute și zeci de minute, ceea ce indică prezența unei relații între ritmul cardiac și structurile sistemului de control care sunt responsabile de generarea fluctuațiilor corespunzătoare. Deci, de exemplu, Navakatikyan et al (1979) au dezvăluit relația dintre undele lente ale ritmului cardiac și fluctuațiile conținutului de catecolamine și corticosteroizi din sânge. S-a observat o relație între undele lente ale ritmului cardiac și activitatea sistemului hipofizo-suprarenal (Karpenko, 1977; Navakatikyan, Krzhanovskaya, 1979).
Structura ritmului cardiac include nu numai componente oscilatorii sub formă de unde respiratorii și non-respiratorii, ci și procese non-periodice (așa-numitele componente fractale). Originea acestor componente ale ritmului cardiac este asociată cu caracterul multinivel și neliniar al proceselor de reglare a ritmului cardiac și cu prezența proceselor tranzitorii. Ritmul inimii, strict vorbind, nu este un proces aleator staționar cu proprietăți ergodice, ceea ce implică repetabilitatea caracteristicilor sale statistice pe orice intervale arbitrare. Variabilitatea ritmului cardiac reflectă o imagine complexă a diferitelor influențe de control asupra sistemului circulator cu interferența componentelor periodice de diferite frecvențe și amplitudini, cu o natură neliniară a interacțiunii diferitelor niveluri de control. Când folosim înregistrări scurte (până la 5 minute), limităm artificial numărul de mecanisme de reglare studiate, restrângem gama de acțiuni de control studiate asupra ritmului cardiac. Acest lucru simplifică analiza datelor, dar nu simplifică interpretarea rezultatelor, deoarece modificările ritmului cardiac reflectă anumite etape ale adaptării organismului la condițiile de mediu.
Metode de bază pentru analiza variabilității ritmului cardiac
Metodele pentru studierea variabilității ritmului cardiac pot fi împărțite în trei grupe: 1) metode pentru evaluarea statistică a unui tablou numeric de cardiointervale; 2) metode de evaluare a relației dintre intervalele cardio; 3) metode de dezvăluire a periodicității latente a seriei dinamice de cardiointervale (Baevsky, Kirillov, Kletskin, 1984). Conform standardelor publicate recent ale Societății Europene de Cardiologie și ale Societății Nord-Americane de Electrofiziologie (Variabilitatea frecvenței cardiace, 1996), se disting două grupe de metode - timp (Metode în domeniul timpului) și frecvență (Metode în domeniul frecvenței). Metodele de timp includ analiza statistică și metodele geometrice, metodele de frecvență includ analiza spectrală. Următoarele cinci metode de analiză a ritmului cardiac au primit cea mai mare utilizare în Rusia (URSS) în ultimii 30 de ani: 1) Analiza statistică, 2) Pulsometria variațională - corespunde metodelor geometrice conform standardelor europene-americane, 3) Analiza autocorelației, 4) Ritmografie de corelație și 5) Analiză spectrală. Aceste metode sunt cele mai comune și s-a acumulat multă experiență în aplicarea lor în diverse domenii ale medicinei clinice și fiziologiei aplicate.
Complexul hardware-software „Varicard” implementează toate metodele de analiză de mai sus. În plus, software-ul Varicarda oferă o analiză cuprinzătoare a variabilității ritmului cardiac, care nu are analogi în practica mondială. În același timp, conform unui anumit set de indicatori, se formează o concluzie asupra gradului de tensiune a sistemelor de reglementare (un indicator al activității sistemelor de reglementare - PARS). Tabelul de mai jos prezintă o listă de indicatori de variabilitate a frecvenței cardiace calculate folosind programul complexului Varicard. Acești indicatori sunt discutați mai detaliat mai jos.
Caracteristici statistice serii dinamice de cardiointervale includ: frecvența cardiacă (Heart Rate-HR), abaterea standard (Standard Deviation-SD), coeficientul de variație (CV). Pe lângă acești indicatori statistici „clasici”, se calculează patru indicatori de diferență. Pentru a face acest lucru, se formează o nouă serie dinamică de valori numerice-valori ale diferențelor dintre fiecare cardiointerval anterior și ulterior. Prin obținerea unei serii de valori ale diferențelor se poate elimina (elimina) componenta constantă a seriei dinamice și toate oscilațiile lente. Aici, în forma sa pură, există doar o componentă rapidă a variabilității - fluctuațiile respiratorii în durata intervalelor cardio. Prin urmare, toți indicatorii de diferență reflectă într-o oarecare măsură activitatea diviziunii parasimpatice a sistemului nervos autonom, adică. aparțin buclei de control autonome. SDSD este rădăcina medie a abaterii pătrate a seriei dinamice de valori ale diferenței, RMSSD este rădăcina pătrată a sumei pătratelor valorilor diferenței (Root Mean of Sum Saccessive Deviations), NN50 count este numărul de diferențe ale căror valori sunt mai mari de 50 de milisecunde, pNN50 este același, dar ca procent din numărul total de intervale.
Pulsometria variației. Esența pulsometriei variaționale este obținerea legii de distribuție a intervalelor cardio ca variabile aleatoare. Pentru a face acest lucru, se construiește o curbă de distribuție - o histogramă. Metoda pulsometriei variaționale corespunde metodelor geometrice conform standardelor euro-americane. Figura 2 prezintă o curbă tipică de distribuție cu principalii indicatori matematici indicați pe ea: Mo (mod), AMo (amplitudinea modului), MxDMn (interval de variație - Diferența dintre valoarea maximă și minimă). Mai jos este o scurtă interpretare medicală și fiziologică a acestor indicatori.
Modul este cea mai frecventă valoare a intervalului cardio din această serie dinamică. În sens fiziologic, acesta este cel mai probabil nivelul de funcționare a sistemului cardiovascular. Cu o distribuție normală și o staționaritate ridicată a procesului studiat, Mo diferă puțin de așteptările matematice.

Figura 2. Pulsograma variației (histogramă)
Amplitudinea modului (AMo) este numărul de cardiointervale corespunzător valorii modului, ca procent din dimensiunea eșantionului. Acest indicator reflectă efectul stabilizator al centralizării controlului ritmului cardiac, care se datorează în principal gradului de activare a diviziunii simpatice a sistemului nervos autonom.
Intervalul de variație (MxDMn) reflectă gradul de variabilitate al valorilor cardiointervalelor din seria dinamică studiată. Se calculează prin diferența dintre valorile maxime și minime ale intervalelor cardio și, prin urmare, cu aritmii sau artefacte, pot fi făcute erori dacă seria dinamică a intervalelor cardio nu a fost pre-editată. Când se calculează MxDMn, valorile extreme ale intervalelor cardio ar trebui să fie eliminate dacă sunt mai mici de 3 la sută din volumul total al probei analizate. Semnificația fiziologică a MxDMn este de obicei asociată cu activitatea diviziunii parasimpatice a sistemului nervos autonom. Cu o dimensiune a eșantionului de 128 de cardiointervale sau mai puțin și în absența tranzitorilor, amplitudinea undelor respiratorii prevalează de obicei asupra amplitudinii fluctuațiilor non-respiratorii ale ritmului cardiac. Cu toate acestea, în unele cazuri, cu o amplitudine semnificativă a componentelor undei lente, valorile MxDMn pot reflecta într-o mai mare măsură starea centrilor nervoși subcorticali.
Pe baza datelor pulsometriei variaționale, se calculează o serie de indicatori derivați, dintre care cel mai frecvent este indicele de tensiune a sistemului de reglare (In), care reflectă gradul de centralizare a controlului ritmului cardiac și caracterizează în principal activitatea diviziunii simpatice. a sistemului nervos autonom.
Acest indicator este utilizat pe scară largă în medicina sportivă, fiziologia muncii, cercetarea spațială, precum și în clinică. Valoarea lui In variază în mod normal între 50 și 150 de unități convenționale. Cu stres emoțional și muncă fizică la oamenii sănătoși, valorile Yin-ului cresc la 300-500 de unități, iar la persoanele în vârstă cu rezerve reduse, astfel de valori sunt observate chiar și în repaus. În prezența anginei, In ajunge la 600-700 de unități, iar în starea pre-infarct, chiar 900-1100 de unități.
Ritmografie de corelație (CRG) este o metodă de reprezentare grafică a unei serii dinamice de cardiointervale sub forma unui „nor” (scattergram) prin construirea unei serii de puncte într-un sistem de coordonate dreptunghiular. În acest caz, de-a lungul axei ordonatelor, fiecare interval R-R curent este reprezentat grafic, iar de-a lungul axei absciselor, fiecare interval R-R ulterior. Figura 3 prezintă un eșantion CRG tipic. Un avantaj important al acestei metode este că vă permite să recunoașteți și să analizați eficient aritmiile cardiace. Indicatorii numerici ai CRG sunt axele elipsei (a și b) formate din norul de puncte și raportul lor a/b. Semnificația fiziologică a raportului a / b este apropiată de Ying, caracterizează gradul de centralizare a controlului ritmului cardiac, activitatea diviziunii simpatice a sistemului nervos autonom.
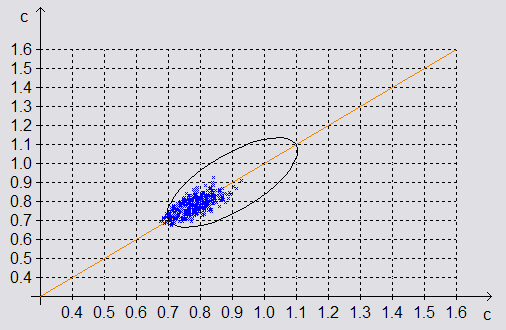
Figura 3. Ritmogramă de corelație (scattergram)
Analiza autocorelației. Calculul și construcția funcției de autocorelare a seriei dinamice de intervale cardio (vezi Figura 4) are ca scop studierea structurii interne a acestei serii ca proces aleatoriu. Funcția de autocorelare este un grafic al dinamicii coeficienților de corelație obținuți prin deplasarea succesivă a seriei dinamice analizate cu un număr față de propria serie. După prima deplasare cu o valoare, coeficientul de corelație este mai mic decât unitatea, cu atât undele respiratorii sunt mai pronunțate. Dacă componentele cu undă lentă domină în eșantionul studiat, atunci coeficientul de corelație după prima schimbare va fi doar puțin mai mic decât unitatea. Deplasările ulterioare duc la o scădere treptată a coeficientului de corelație până la apariția coeficienților de corelație negativi. Semnificația fiziologică a utilizării analizei de autocorelare este de a evalua gradul de influență al buclei centrale de control asupra celei autonome. Cu cât această influență este mai puternică, cu atât mai aproape de unitate este valoarea coeficientului de corelație la prima schimbare. Autocorrelograma vă permite să judecați periodicitatea latentă a ritmului cardiac. Cu toate acestea, această analiză este doar calitativă.

Figura 4. Funcția de autocorelare
Analiza spectrală. Pentru o evaluare cantitativă precisă a proceselor periodice din ritmul cardiac, se utilizează analiza spectrală. Semnificația fiziologică a analizei spectrale este că este folosită pentru a evalua activitatea nivelurilor individuale de control al ritmului cardiac. Figura 5 prezintă o mostră dintr-un spectru tipic de ritm cardiac pentru o probă de 5 minute.
Figura 5. Spectrul ritmului cardiac
Aici, valorile perioadelor de oscilație în secunde sunt reprezentate de-a lungul axei absciselor, iar puterile componentelor spectrale corespunzătoare în milisecunde pătrat/Hz (/Hz) sunt reprezentate de-a lungul axei ordonatelor. În analiza spectrală a așa-numitei serii dinamice scurte de cardiointervale de până la 5 minute, este posibil să se măsoare doar puterea undelor respiratorii și a undelor lente de ordinul 1 și 2. În ceea ce privește undele lente de ordinul 2, conform standardelor european-americane, intervalul lor este determinat în intervalul de la 0,04 la 0,003 Hz sau de la 25 la 300 s. Totuși, numeroase date din literatură indică faptul că în acest interval se observă fluctuații de natură variată: cele asociate cu procese de termoreglare (Sayers, 1973, 1981), cu procese redox, cu procese metabolice, în special cu glicoliză (Boiteux et. al, 1977) . Astfel, în intervalul de până la 5 minute, pot fi distinse valuri nu doar de ordinul 2, ci și de al 3-lea-4. Prin urmare, în complexul „Varicard”, undele lente de ordinul 2 sunt calculate în intervalul de la 25 la 70 de secunde (0,04-0,015 Hz). De regulă, aceste unde sunt asociate cu activitatea părților suprasegmentare ale creierului (Khaspekova, 1994), cu activitatea centrilor subcorticali simpatici. În ceea ce privește undele lente de ordinul 3-4, puterea lor principală este reflectată, de regulă, de armonica 1 a spectrului. Se adoptă denumirile componentelor spectrale, conform standardelor euro-americane. Numele lor reflectă compoziția de frecvență: oscilații de înaltă frecvență (High Frequency -HF), oscilații de joasă frecvență (Low Freqyency -LF), oscilații de frecvență foarte joasă - (Very Low Freqyency -VLF) și oscilații de frecvență ultra joasă (Ultra Low Freqency - ULF). Gamele de frecvență ale acestor componente arată astfel:
HF: 0,4 - 0,15 Hz (2,5 - 7 sec.)
LF: 0,15 - 0,04 Hz (7 - 25 sec.)
VLF: 0,04 - 0,015 Hz (25 - 70 sec.)
ULF: mai puțin de 0,015 Hz (mai mult de 70 sec.)
Analiza spectrală calculează de obicei pentru fiecare dintre componente puterea totală absolută în interval, puterea medie în interval, valoarea armonicii maxime și valoarea relativă ca procent din puterea totală în toate intervalele (Puterea totală-TP) . Conform analizei spectrale a frecvenței cardiace, se calculează următorii indicatori: indicele de centralizare - IC (Indice de centralizare, IC = (HF + LF) / VLF) și indicele de activare a centrilor nervoși subcorticali IAP (Indice de Activitatea Centrilor Subcorticali, ISCA = LF / VLF). IC reflectă gradul de predominanță a componentelor non-respiratorii ale aritmiei sinusale față de cele respiratorii. De fapt, aceasta este o caracteristică cantitativă a relației dintre circuitele central și autonom de reglare a frecvenței cardiace. Al doilea indice IAP caracterizează activitatea centrului nervos subcortical cardiovascular în raport cu nivelurile superioare de control. Activitatea crescută a centrilor nervoși subcorticali se manifestă prin creșterea IAP. Acest indice poate fi utilizat pentru a controla procesele de inhibiție corticale. În plus, conform standardelor europene-americane, se calculează raportul HF/LF.
Evaluare cuprinzătoare variabilitatea ritmului cardiac poate fi realizată în ceea ce privește activitatea sistemelor de reglementare (PARS). Se calculează în puncte conform unui algoritm special care ia în considerare indicatorii statistici, indicatori de histogramă și datele din analiza spectrală a intervalelor cardio. PARS face posibilă diferențierea diferitelor grade de tensiune în sistemele de reglementare. PARS a fost propus la începutul anilor 80 (Baevsky R.M. et al., 1964) și s-a dovedit a fi destul de eficient în evaluarea capacităților de adaptare ale corpului. Algoritmul pentru calculul său a fost îmbunătățit treptat și până acum a fost dezvoltat un nou algoritm care ia în considerare valorile tuturor indicatorilor principali ai variației ritmului cardiac.
Valorile PARS sunt exprimate în punctele de la 1 la 10. Pe baza analizei valorilor PARS, pot fi diagnosticate următoarele stări funcționale:
1. Starea de tensiune optima a sistemelor de reglare, necesara mentinerii echilibrului activ al organismului cu mediul (norma, PARS = 1-2).
2. Starea de tensiune moderată a sistemelor de reglare, când organismul are nevoie de rezerve funcționale suplimentare pentru a se adapta la condițiile de mediu. Astfel de condiții apar în procesul de adaptare la muncă, cu stres emoțional sau sub influența factorilor negativi de mediu (PARS = 3-4).
3. Starea de tensiune pronunțată a sistemelor de reglare, care este asociată cu mobilizarea activă a mecanismelor de protecție, inclusiv o creștere a activității sistemului simpatico-suprarenal și a sistemului hipofizo-suprarenal (PARS = 4-6).
4. Starea de suprasolicitare a sistemelor de reglementare, care se caracterizează prin insuficiența mecanismelor de protecție și adaptare, incapacitatea acestora de a oferi un răspuns adecvat al organismului la impactul factorilor de mediu. Aici, activarea excesivă a sistemelor de reglementare nu mai este susținută de rezervele funcționale corespunzătoare (PARS = 6-8).
5. Starea de epuizare (astenizare) a sistemelor de reglare, în care activitatea mecanismelor de control scade (insuficiența mecanismelor de reglare) și apar semne caracteristice de patologie. Aici, schimbările specifice predomină clar asupra celor nespecifice (PARS = 8-10).
Programul prevede emiterea pe ecran și tipărirea unei concluzii speciale privind rezultatele calculului PARS. Această concluzie este însoțită de un grafic sub forma unei „scări a statelor”, dezvoltat în domeniul diagnosticului prenosologic (Baevsky, 1979, Berseneva, 1991, Baevsky, Berseneva, 1997). În același timp, pentru claritate se disting trei zone de stări funcționale, prezentate sub forma unui „semafor”.
Scara „Semafor” este bine înțeleasă de fiecare persoană, fie că este vorba de șofer sau pieton. VERDE înseamnă că totul este în ordine, poți merge mai departe fără teamă. Nu sunt necesare măsuri speciale de prevenire și tratament. GALBEN – indică necesitatea unei atenții sporite pentru sănătatea ta.
Starea funcțională a corpului este de așa natură încât „trebuie să te oprești și să privești în jur înainte de a merge mai departe”. Cu alte cuvinte, aici deja vorbim despre necesitatea unor măsuri de îmbunătățire a sănătății și de prevenire, despre o atitudine mai atentă la starea cuiva. În cele din urmă, RED arată că nu poți merge mai departe, trebuie să iei măsuri serioase în ceea ce privește sănătatea ta. Necesită mai întâi diagnosticul și apoi tratamentul posibilelor boli.
Alocarea zonelor de sănătate verzi, galbene și roșii ne permite să caracterizăm starea funcțională a unei persoane în ceea ce privește riscul de a dezvolta o boală. Pentru fiecare treaptă a „scării stărilor”, se asigură o „diagnostic” a stării funcționale în funcție de gradul de severitate al tensiunii sistemelor de reglementare. În plus, este posibilă atribuirea subiectului uneia dintre cele 4 stări funcționale conform clasificării adoptate în diagnosticul prenosologic:
Starea normei sau starea de adaptare satisfăcătoare,
stare de tensiune funcțională,
O stare de supratensiune sau o stare de adaptare nesatisfăcătoare,
Starea de epuizare a sistemelor de reglementare sau eșecul adaptării.
Trebuie remarcat faptul că PARS nu are analogi în studiile străine, deoarece în prezent, judecând după Standardele propuse de Societatea Europeană de Cardiologie și Societatea Nord-Americană de Electrofiziologie, atenția lor principală se atrage asupra posibilității de a utiliza analiza inimii. variabilitatea ratei pentru a evalua homeostazia autonomă, raportul dintre activitățile diviziunilor simpatice și parasimpatice ale sistemului nervos autonom și starea funcției baroreflexe.
Lista de mai jos conține o listă de indicatori de variabilitate a frecvenței cardiace calculați folosind programul de bază al complexului hardware-software Varicard. Cele mai multe se referă la rezultatele analizei spectrale. Acest lucru, cu toate acestea, nu înseamnă că datele spectrale ar trebui să fie preferate în studiile clinice și fiziologice. Numărul indicatorilor spectrale a crescut semnificativ datorită faptului că în fiecare dintre cele 4 game de frecvență se calculează 5 indicatori: puterea în valori absolute și relative, puterea medie, puterea maximă și valoarea perioadei dominante. Cercetătorul are posibilitatea de a alege în fiecare caz indicatorul care s-a dovedit a fi cel mai informativ.
Principalii indicatori ai variabilității ritmului cardiac și interpretarea lor fiziologică scurtă pentru înregistrările cu o dimensiune a eșantionului de 5 minute (înregistrări pe termen scurt)
1. HR (Pulse Rate) - Nivelul mediu de funcționare al sistemului circulator
2. SDNN (Standard deviation of the full array of cardiointervals) - Efectul total al reglării autonome a circulației sanguine
3. RMSSD (Rădăcina pătrată a sumei diferenţelor unui număr consecutiv de cardiointervale) - Activitatea verigii parasimpatice de reglare autonomă
4. pNN50 (Numărul de perechi de cardiointervale cu o diferență mai mare de 50 ms în % din numărul total de cardiointervale din matrice) - Un indicator al gradului de predominanță a legăturii parasimpatice de reglare față de cea simpatică (valoare relativă) )
5. CV (Coeficientul de variație al întregii game de cardiointervale) - Indicator normalizat al efectului total al reglarii
6. MxDMn (TINN*) (Diferența dintre valorile maxime și minime ale cardiointervalelor) - Amplitudinea maximă a influențelor reglatoare
7. МxRMn (Raportul dintre intervalul cardio maxim și minim) - Gama relativă de influențe reglatoare
8. Mo (Mod) - Nivelul cel mai probabil de funcționare a sistemului cardiovascular
9. AMoSD (Amplitudinea modului la lățimea clasei SD) - Un indicator condiționat al activității legăturii simpatice de reglare
10. AMo50 (Amplitudinea modului cu o lățime a clasei de 50 ms) - Un indicator condiționat al activității legăturii simpatice de reglare
11. AMo7,8 (Amplitudinea modului la o lățime de clasă de 1/128 s) - Un indicator condiționat al activității legăturii simpatice de reglare
12. SI (Indice de stres) - Gradul de tensiune al sistemelor de reglementare (gradul de predominanță a activității mecanismelor centrale de reglare asupra celor autonome)
13. HF, [%] (Puterea spectrului componentei de înaltă frecvență a variabilității în% din puterea totală a oscilațiilor) - Nivelul relativ de activitate al verigii parasimpatice de reglare
14. LF, [%] (Puterea spectrului componentei de joasă frecvență a variabilității în% din puterea totală a oscilațiilor) - Nivelul relativ de activitate al centrului vasomotor
15. VLF, [%] (Puterea spectrului componentei de frecvență ultra joasă a variabilității în% din puterea totală a oscilațiilor) - Nivelul relativ de activitate al verigii simpatice de reglare
16. CC1 (Valoarea primului coeficient al funcției de autocorelare) - Gradul de activitate al circuitului de reglare autonomă
17. CC0 (Numărul de deplasări în funcția de autocorelare până când valoarea coeficientului de corelare este mai mică decât zero) - Gradul de activitate al circuitului central de reglare
18. NArr (Numărul de contracții aritmice) - Numărul absolut de contracții aritmice în 5 minute
19. TP (Puterea totală a spectrului variabilității ritmului cardiac) - Nivelul total de activitate al sistemelor de reglementare
20. HFmx (Puterea maximă a spectrului componentei de variabilitate de înaltă frecvență în ms2) - Nivelul maxim de activitate al legăturii parasimpatice de reglare
21. LFmx (spectrul de putere maximă al componentei de joasă frecvență a variabilității în ms2) - Nivelul maxim de activitate al centrului vasomotor
22. VLFmx (Puterea maximă a spectrului componentei de variabilitate de frecvență ultra joasă în ms2) - Nivelul maxim de activitate al legăturii simpatice de reglare
23. ULFmx (Maximum power spectrum of the ultra-low-frequency component of variability in ms2) - Nivelul maxim de activitate al nivelurilor subcorticale de reglare (centri vegetativi superiori).
24. HFt (Perioada dominantă a componentei de înaltă frecvență a spectrului variabilității ritmului cardiac) - Perioada medie a ciclului respirator
25. LFt (Perioada dominantă a componentei de joasă frecvență a spectrului variabilității ritmului cardiac) - Timpul mediu al reacției baroreflexe
26. VLFt (Perioada dominantă a componentei de frecvență ultra joasă a spectrului de variabilitate a frecvenței cardiace) - Perioada medie a răspunsului reflex al centrului subcortical cardiovascular
27. ULFt (Perioada dominantă a componentei de frecvență ultra joasă a spectrului de variabilitate a frecvenței cardiace) - Perioada medie de timp a răspunsului neuroreflex al nivelurilor subcorticale de reglare (centri autonomi superioare).
28. (LF/HF) (Raportul dintre valorile componentei de joasă frecvență și de înaltă frecvență a variabilității ritmului cardiac) - Raportul nivelurilor de activitate ale circuitelor centrale și autonome de reglare
29. (VLF/HF) (Raportul dintre valorile componentei de frecvență ultra joasă și de înaltă frecvență a variabilității ritmului cardiac) - Raportul nivelurilor de activitate ale circuitelor de reglare centrală și autonomă
30. IC (Index of Centralization) - Gradul de centralizare a controlului ritmului cardiac
31. IARS (Indicator (indice) de activitate a sistemelor de reglementare - PARS) - Indicator de activitate a sistemelor de reglementare
* Folosit numai în sistemul de punctare recomandat de standardele Societății Europene de Cardiologie și Societății Nord-Americane de Electrofiziologie (Variabilitatea ritmului cardiac. Standarde de măsurare, interpretare fiziologică și utilizare clinică. Circulație, 93:1043-1065,1996).
În concluzie, este oferită o scurtă descriere a celor 7 indicatori principali ai variației ritmului cardiac, care sunt cel mai des utilizați în studiile clinice și fiziologice.
1. RMS, SD. Cea mai simplă evaluare a variabilității ritmului cardiac este de a calcula abaterea standard a duratei intervalelor cardio. Aceasta este o procedură statistică standard bine-cunoscută. Valorile RMS sunt exprimate în milisecunde (ms). Valorile RMS normale sunt în intervalul 40-80 ms. Cu toate acestea, aceste valori au caracteristici de vârstă și gen care ar trebui luate în considerare atunci când se evaluează rezultatele studiului. RMS este cel mai simplu și mai popular indicator al activității mecanismelor de reglementare. Acesta este un indicator extrem de sensibil al stării mecanismelor de reglementare. Cu toate acestea, o creștere sau scădere a RMS poate fi asociată atât cu circuitul de reglare autonomă, cât și cu cel central. De regulă, o creștere a COEX indică o creștere a reglementării autonome, i.e. influența respirației asupra ritmului cardiac, care se observă cel mai adesea în timpul somnului. O scădere a sistemului COEX este de obicei asociată cu o creștere a reglării simpatice, care suprimă activitatea circuitului autonom. O scădere bruscă a RMS este asociată cu o tensiune semnificativă a sistemelor de reglementare, atunci când în procesul de reglare sunt incluse niveluri mai ridicate de control și aceasta duce la o suprimare aproape completă a activității circuitului autonom. Informații similare în sens fiziologic cu RMS pot fi obținute din indicatorul puterii totale a spectrului - TP. Acest indicator diferă prin aceea că caracterizează numai procesele periodice ale ritmului cardiac și nu conține așa-numita parte fractală a procesului, adică. componente neliniare și neperiodice.
2. RMSSD- un indicator al activității verigii parasimpatice de reglare autonomă. Acest indicator este calculat din seria dinamică a diferențelor în valorile perechilor succesive de intervale cardio și nu conține componente cu unde lente ale ritmului cardiac. În forma sa cea mai pură, reflectă activitatea circuitului autonom de reglare. Cu cât valoarea RMSSD este mai mare, cu atât este mai activă legătura de reglare parasimpatică. În mod normal, valorile acestui indicator sunt în intervalul 20-50 ms. Informații similare pot fi obținute din indicatorul pNN50, care exprimă în % numărul de valori ale diferențelor mai mari de 50 ms.
3. INDICE DE TENSIUNE AL SISTEMELOR DE REGLARE (IN) caracterizează activitatea mecanismelor de reglare simpatică, starea circuitului central de reglare. Acest indicator este calculat pe baza unei analize a graficului de distribuție a intervalelor cardio - o histogramă. Activarea circuitului central, întărirea reglării simpatice în timpul efortului se manifestă prin stabilizarea ritmului, o scădere a răspândirii duratelor intervalelor cardio, o creștere a numărului de intervale de același tip în durată (o creștere a amplitudinea modului a numărului de intervale corespunzătoare valorii modului - valoarea cel mai frecvent întâlnită). Analiza formei histogramei sau metoda pulsometriei variaționale demonstrează clar acest proces sub forma unei îngustări a histogramei cu o creștere a amplitudinii modului. Cantitativ, aceasta poate fi exprimată prin raportul dintre înălțimea histogramei și lățimea acesteia. Acest indicator se numește indicele de tensiune al sistemelor de reglementare (In). În mod normal, Ying variază între 80-150 de unități convenționale. Acest indicator este foarte sensibil la creșterea tonusului sistemului nervos simpatic. O sarcină mică (fizică sau emoțională) crește Ying-ul de 1,5-2 ori. Cu sarcini semnificative, crește de 5-10 ori. La pacienții cu o tensiune constantă a sistemelor de reglare, In în repaus poate fi egală cu 400-600 de unități convenționale. La pacienții cu crize de angină și infarct miocardic, în repaus ajunge la 1000-1500 de unități.
4. PUTEREA COMPONENTEI DE ÎNALTĂ FRECVENȚĂ A SPECTRULUI (UNDE RESPIRATORII). Activitatea diviziunii simpatice a sistemului nervos autonom ca una dintre componentele echilibrului autonom poate fi apreciată prin gradul de inhibare (suprimare) a activității circuitului de reglare autonomă, de care este responsabilă diviziunea parasimpatică. Acest bine reflectă indicatorul puterii undelor respiratorii ale ritmului cardiac în formă absolută și procentuală. De obicei, componenta respiratorie (HF-frecvență înaltă) este de 15-25% din puterea totală a spectrului. O scădere a acestei proporții la 8-10% indică o deplasare a echilibrului autonom către predominanța diviziunii simpatice. Dacă valoarea HF scade sub 2-3%, atunci putem vorbi despre o predominanță accentuată a activității simpatice. În acest caz, valorile RMSSD și pNN50 scad, de asemenea, semnificativ.
5. PUTEREA COMPONENTEI DE JĂ FRECVENȚĂ A SPECTRULUI (UNDELE LENTE DE ORDINUL I SAU UNDELE VASOMOTORII). Acest indicator (LF) caracterizează starea sistemului de reglare a tonusului vascular. În mod normal, receptorii sensibili din zona sinusului carotidian percep modificări ale tensiunii arteriale, iar impulsurile nervoase aferente intră în centrul vasomotor (vasomotor) al medulei oblongate. Aici se realizează sinteza aferentă (prelucrarea și analiza informațiilor primite) și semnalele de control (impulsurile nervoase eferente) intră în sistemul vascular. Acest proces de control al tonusului vascular cu feedback asupra fibrelor musculare netede ale vaselor este efectuat în mod constant de centrul vasomotor. Timpul necesar centrului vasomotor pentru operațiunea de primire, procesare și transmitere a informațiilor variază de la 7 la 20 de secunde; în medie este de 10 secunde. Prin urmare, în ritmul inimii pot fi detectate unde cu o frecvență apropiată de 0,1 Hz (10 s), care se numesc vasomotorii. Pentru prima dată aceste unde au fost observate de Mayer și colab.(1931) și de aceea sunt numite uneori unde Mayer. Puterea undelor lente de ordinul I determină activitatea centrului vasomotor. Trecerea de la poziția „culcat” la poziția „în picioare” duce la o creștere semnificativă a puterii în acest interval de fluctuații ale ritmului cardiac. Activitatea centrului vasomotor scade odată cu vârsta, iar la vârstnici acest efect este practic absent. În locul undelor lente de ordinul 1, puterea undelor lente de ordinul 2 crește. Aceasta înseamnă că procesul de reglare a tensiunii arteriale se realizează cu participarea unor mecanisme nespecifice prin activarea diviziunii simpatice a sistemului nervos autonom. De obicei, procentul undelor vasomotorii în poziția „culcat” este de la 15 la 35-40%. Trebuie menționat și indicatorul frecvenței dominante în gama undelor vasomotorii. De obicei, este în 10-12 secunde. O creștere la 13-14 secunde poate indica o încetinire a procesării informațiilor în centrul vasomotor sau o încetinire a transmiterii informațiilor în sistemul de reglare baroreflex.
6. PUTEREA COMPONENTEI „SUPER”-CU JĂ FRECVENȚĂ A SPECTRULUI (UNDE LENTE DE ORDINUL II). Componenta spectrală a ritmului cardiac în intervalul 0,04-0,015 Hz (25-70 s), conform multor autori străini (Pagani M., 1989, 1994, Maliani, 1991), caracterizează activitatea diviziunii simpatice a sistem nervos autonom. Totuși, în acest caz vorbim despre influențe mai complexe de la nivelul supra-segmental de control, deoarece amplitudinea VLF este strâns legată de stresul psiho-emoțional (Kudryavtseva V.I., 1974, Menitsky D.N., 1978). Datele lui N.B. Khaspekova (1996) au arătat în mod fiabil că VLF reflectă influențe ergotrope cerebrale asupra nivelurilor subiacente de control și fac posibilă aprecierea stării funcționale a creierului în patologiile psihogene și organice ale creierului. Potrivit lui A.N. VLF lui Fleishman este un bun indicator al controlului metabolic (1996). Astfel, VLF caracterizează influența centrilor autonomi superiori asupra centrului subcortical cardiovascular și poate fi folosit ca un marker de încredere al gradului de conexiune între nivelurile autonome (segmentare) de reglare a circulației sanguine și nivelurile suprasegmentare, inclusiv nivelurile hipofizo-hipotalamic și cortical. . În mod normal, puterea VLF este de 15-30% din puterea totală a spectrului.
7. ARITMIE- un indicator al prezenței și severității contracțiilor cardiace aritmice. Aritmiile includ contracții extraordinare sau o întârziere a următoarei contracții. În primul caz, acest lucru se datorează excitabilității crescute a miocardului sau a centrilor nervoși. În același timp, se disting contracțiile extraordinare intraventriculare și extraventriculare (supraventriculare) (extrasistole). În al doilea caz, vorbim despre blocarea răspândirii excitației prin mușchiul inimii ca urmare a unor tulburări funcționale sau organice. Indiferent de tipul de aritmie, numărul de aritmii poate fi exprimat ca procent din numărul total de bătăi ale inimii. În mod normal, nu ar trebui să existe mai mult de 1-2% din aritmii, adică. 1-2 contracții aritmice la 100 de bătăi ale inimii. Deoarece un număr crescut de aritmii este un semn al dezvoltării patologiei, acest indicator trebuie tratat cu prudență. La evaluarea aritmiilor, este deosebit de important să se țină seama de așa-numitele „praguri critice” - valorile limită ale indicatorului de exces, care necesită asistență medicală imediată. Indicatorul de aritmii nu este inclus în evaluarea PARS și este emis separat în încheiere. Acest lucru se datorează, în primul rând, semnificației clinice a aritmiilor și, în al doilea rând, faptului că în analiza matematică a ritmului cardiac, aritmiile individuale sunt excluse din calcule și interpolate de valorile învecinate ale intervalelor RR.
Dacă există mai mult de 2-4% dintre aritmii în gama de intervale RR, mai ales dacă acestea nu sunt aritmii unice, ci de grup, atunci nu se calculează un număr de indicatori. Acest lucru se aplică pe deplin analizei spectrale.


