05.09.2019
Inflamaţie. Inflamație: caracteristici generale, patomorfologia inflamației alterative și exsudative.
Informatii generale
Inflamaţie- o reacție locală complexă vascular-mezenchimală la afectarea tisulară cauzată de acțiunea diferiților agenți. Această reacție are ca scop distrugerea agentului care a cauzat deteriorarea și repararea țesutului deteriorat. Inflamația, o reacție dezvoltată în cursul filogenezei, are un caracter protector și adaptativ și poartă elemente nu numai de patologie, ci și de fiziologie. O astfel de semnificație dublă pentru corpul inflamației este o caracteristică particulară a acesteia.
Cei care stau mult timp ar trebui să stea puțin în acest timp de odihnă pentru a-și odihni picioarele și picioarele. Antonio Carlos Ligotsky Campos; Alessandra Borges-Branco; Ann Carolina Groth. Procesul de furtună este comun tuturor rănilor, indiferent de agentul care l-a provocat. Procesul de vindecare este împărțit în trei faze: inflamație, proliferare sau granulare, remodelare sau maturare. Colagenul este cea mai abundentă proteină din corpul uman și este, de asemenea, o componentă majoră a matricei extracelulare a țesuturilor.
Este structurat într-o rețea densă și dinamică ca rezultat al depunerii și reabsorbției constante. Țesutul cicatricial este rezultatul unei interacțiuni între sinteza, fixarea și degradarea acestuia. Există mai multe moduri de a evalua vindecarea rănilor. Studiile recente s-au concentrat pe modularea vindecării pe nivel molecular, în încercarea de a evita complet cicatricile patologice.
Încă de la sfârșitul secolului al XIX-lea, I.I. Mechnikov credea că inflamația este o reacție adaptativă a organismului dezvoltată în cursul evoluției, iar una dintre cele mai importante manifestări ale sale este fagocitoza de către microfage și macrofage a agenților patogeni și astfel asigurând recuperarea organismului. Dar funcția reparatorie a inflamației a fost pentru I.I. Mechnikov este ascuns. Subliniind caracterul protector al inflamației, el credea în același timp că puterea de vindecare a naturii, care este reacția inflamatorie, nu este încă o adaptare care a ajuns la perfecțiune. Potrivit lui I.I. Mechnikov, dovada acestui lucru sunt bolile frecvente însoțite de inflamație și decesele cauzate de acestea.
Cuvinte cheie: Tratamentul rănilor. Procesul de vindecare este comun tuturor rănilor, indiferent de agentul care l-a provocat. Este împărțit în trei faze: inflamație, proliferare sau granulare, remodelare sau maturare. Colagenul este cea mai abundentă proteină din corpul uman și este, de asemenea, componenta principală a rănilor matricei. Colagenul este organizat într-o rețea densă și dinamică rezultată din depunerea și reabsorbția constantă de colagen. Cicatricea plăgii este rezultatul unei interacțiuni între sinteza, degradarea și remodelarea țesuturilor.
Etiologia inflamației
Factorii care provoacă inflamația pot fi biologici, fizici (inclusiv traumatici), chimici; sunt de origine endogene sau exogene.
La factori fizici, care provoacă inflamație includ radiații și energie electrică, mare și temperaturi scăzute, diverse tipuri de leziuni.
Studii recente au încercat să influențeze procesul, folosind fie nutrienți, fie medicamente, pentru a obține o recuperare mai rapidă după trauma chirurgicală. Procesul de furtună este comun tuturor rănilor, indiferent de agentul cauzat de acesta, este sistemic și dinamic și este direct legat de conditii generale organism 12. Vindecarea rănilor constă într-o cascadă ideală și coordonată de evenimente celulare, moleculare și biochimice care interacționează pentru a repara țesuturile.
Clarke a reclasificat recent acest proces în trei etape, împărțite în: o fază inflamatorie, o fază de proliferare sau de granulare și o fază de remodelare sau maturare 15. Leziunile tisulare - stimulul inițial pentru procesul de vindecare - pun elementele din sânge în contact cu colagenul și alte substanțe ale matricei extracelulare, provocând degranularea trombocitelor și activând cascadele de coagulare și complement. Acest lucru duce la eliberarea mai multor mediatori vasoactivi și chemotactici, care conduc la un proces de rutină prin atragerea celulelor inflamatorii în zona rănii 61.
factori chimici inflamația poate fi diferită substanțe chimice, toxine și otrăvuri.
Dezvoltarea inflamației este determinată nu numai de influența unuia sau altuia factor etiologic, ci și de particularitatea reactivității organismului.
Morfologia și patogeneza inflamației
Inflamaţie poate fi exprimat prin formarea unui focar microscopic sau a unei zone extinse, au nu numai un caracter focal, ci și difuz. Uneori, inflamația apare în sistemul de țesuturi, apoi vorbește despre sistemică leziuni inflamatorii ( boli reumatismale cu leziuni inflamatorii sistemice ale țesutului conjunctiv, vasculită sistemică etc.). Uneori este dificil să se facă distincția între inflamația localizată și cea sistemică.
Am trecut în revistă teze de master și teze de doctorat realizate în linia de cercetare „Cocația de organe și țesuturi” a programului postuniversitar în chirurgie clinică Universitatea Federală din Parana. Articole considerate relevante au fost folosite și incluse în referințele la această lucrare. Endoteliul și trombocitele deteriorate stimulează cascada de coagulare. Trombocitele joacă un rol cheie în tratament. Cheagul este format din colagen, trombocite si trombina, care servesc drept rezervor proteic pentru sinteza citokinelor si factorilor de crestere, crescand efectele acestuia.
Inflamația se dezvoltă în zonă histion şi constă din următoarele faze care se dezvoltă succesiv: 1) alterare; 2) exudație; 3) proliferarea celulelor hematogene și histiogene și, mai rar, a celulelor parenchimatoase (epiteliu). Relația dintre aceste faze este prezentată în Schema IX.
Modificare- afectarea țesuturilor este faza initiala inflamație și manifestă alt fel distrofie și necroză. În această fază a inflamației, are loc o eliberare de substanțe biologic active - mediatori inflamatori. Aceasta - lansator inflamație, care determină cinetica răspunsului inflamator.
Astfel, răspunsul inflamator începe cu vasodilatație și creșterea permeabilității vasculare, favorizând chemotaxia. Neutrofilele sunt primele celule care ajung la rană, cu concentrație maximă 24 de ore după accidentare. Sunt atrași de substanțele chimiotactice secretate de trombocite. Neutrofilele aderă la peretele endotelial prin legarea de selectine. Neutrofilele produc radicali liberi care contribuie la distrugerea bacteriilor și sunt înlocuiți treptat de macrofage 11.
Aceștia joacă un rol cheie la sfârșitul procesării inițiate de neutrofile și contribuția lor principală este secreția de citokine și factori de creștere, pe lângă promovarea angiogenezei, fibroplaziei și sintezei matricei extracelulare 11, care este fundamentală pentru trecerea la faza proliferativă.
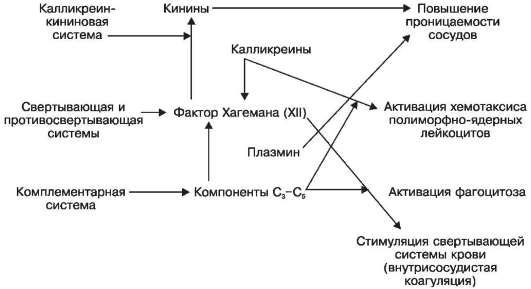
Mediatorii inflamatori pot fi de origine plasmatică (umorală) și celulară (țesut). Mediatori de origine plasmatică- sunt reprezentanți ai sistemelor kalikrein-kinină (kinine, kalikreine), coagulare și anticoagulare (factorul XII de coagulare a sângelui, sau factor Hageman, plasmină) și complementare (componentele C 3 -C 5). Mediatorii acestor sisteme cresc permeabilitatea microvaselor, activează chemotaxia leucocitelor polimorfonucleare, fagocitoza și coagularea intravasculară (Schema X).
Faza proliferativă constă din patru etape majore: epitelizare, angiogeneză, formarea țesutului de granulație și depunerea de colagen. Această fază începe la aproximativ 4 zile după accidentare și continuă până la aproximativ sfârșitul celei de-a doua săptămâni. Epitelizarea apare precoce. Dacă membrana bazală nu este deteriorată, celulele epiteliale migrează în sus și straturile normale ale epidermei sunt restabilite după trei zile. Dacă membrana bazală este deteriorată, celulele epiteliale ale marginilor plăgii încep să se înmulțească în încercarea de a restabili bariera de protecție 32.
Mediatori de origine celulară asociat cu celule efectoare - mastocite (bazofile tisulare) și leucocite bazofile, care eliberează histamina, serotonina, o substanță de anafilaxie care reacţionează lent etc.; trombocitele producând, pe lângă histamina, serotonină și prostaglandine, și enzime lizozomale; leucocite polimorfonucleare bogate în leucokine
Angiogeneza este stimulată de factorul de necroză tumorală alfa și se caracterizează prin migrarea celulelor endoteliale și formarea capilară necesară pentru o vindecare adecvată. Partea finală a fazei proliferative este formarea țesutului de granulație. Fibroblastele și celulele endoteliale sunt celulele principale ale fazei proliferative. Fibroblastele din țesuturile adiacente migrează către rană, dar trebuie activate pentru a-și opri repausul.
Faza de maturare sau remodelare. Cea mai importantă caracteristică a acestei faze este depunerea de colagen într-o manieră organizată, deci aceasta este cea mai importantă din punct de vedere clinic. Colagenul obtinut initial este mai subtire decat colagenul prezent in pielea normala si are o orientare paralela cu pielea. În timp, colagenul original este reabsorbit și se formează colagen mai gros de-a lungul liniilor de tensiune. Aceste modificări se reflectă într-o creștere a rezistenței la tracțiune a plăgii. Reorganizarea noii matrice - proces important vindecare.
Schema IX. Fazele inflamației
Schema X. Acțiunea mediatorilor inflamatori de origine plasmatică (umorală).
 mi, enzime lizozomale, proteine cationice și proteaze neutre. Celulele efectoare care produc mediatori inflamatori sunt, de asemenea, celule ale răspunsurilor imune - macrofage care își eliberează monokinele (interleukina I) și limfocitele care produc limfokine (interleukina II). Nu numai că este asociat cu mediatori de origine celulară permeabilitate crescută a microvaselor
și fagocitoză;
ei au acțiune bactericidă,
cauză alterare secundară
(histoliză), includ mecanisme imunitare
într-un răspuns inflamator reglementează proliferarea
și diferențierea celulară
pe domeniul inflamației, care vizează repararea, compensarea sau înlocuirea focarului de afectare cu țesut conjunctiv (Schema XI). Conductorul interacțiunilor celulare în domeniul inflamației este macrofage.
mi, enzime lizozomale, proteine cationice și proteaze neutre. Celulele efectoare care produc mediatori inflamatori sunt, de asemenea, celule ale răspunsurilor imune - macrofage care își eliberează monokinele (interleukina I) și limfocitele care produc limfokine (interleukina II). Nu numai că este asociat cu mediatori de origine celulară permeabilitate crescută a microvaselor
și fagocitoză;
ei au acțiune bactericidă,
cauză alterare secundară
(histoliză), includ mecanisme imunitare
într-un răspuns inflamator reglementează proliferarea
și diferențierea celulară
pe domeniul inflamației, care vizează repararea, compensarea sau înlocuirea focarului de afectare cu țesut conjunctiv (Schema XI). Conductorul interacțiunilor celulare în domeniul inflamației este macrofage.
Fibroblastele și leucocitele secretă colagenaze, care contribuie la liza matricei vechi. Vindecarea are succes atunci când există un echilibru între sinteza noii matrice și lingerea matricei vechi, cu succes când depunerea este mai mare. Chiar și după un an, rana va avea colagen mai puțin organizat decât pielea sănătoasă și rezistența la tracțiune nu va reveni niciodată la 100%, ajungând la aproximativ 80% după trei luni 12.
Colagenul este cea mai abundentă proteină din țesutul conjunctiv în faza de vindecare. Diferite diferențe în compoziția lor chimică le determină functii biologice. Până în prezent, au fost descrise 19 izoforme de colagen, codificate de o singură genă. Prezența bogată a glicinei și a prolinei este necesară pentru ca molecula de colagen matură să își asume o structură triplu elicoidal. Degradarea colagenului începe devreme și este foarte activă în timpul proces inflamator. Digestia lui are loc în mediul extracelular și este mediată de colagenaze specifice.
Mediatorii de origine plasmă și celulară sunt interconectați și funcționează pe principiul unei reacții autocatalitice cu feedback și sprijin reciproc (vezi Schemele X și XI). Acțiunea mediatorilor este mediată de receptorii de pe suprafața celulelor efectoare. De aici rezultă că schimbarea unor mediatori de către alții în timp determină o modificare a formelor celulare în domeniul inflamației - de la un leucocit polimorfonuclear pentru fagocitoză la un fibroblast activat de monokine macrofage pentru reparare.
Sunt cunoscute patru tipuri de colagenaze: ser și metaloproteinaze. Activitatea colagenazei este controlată de citokinele eliberate în principal de celulele inflamatorii, endoteliale, fibroblastice și keratinocite. Astfel, formarea unei matrice extracelulare este o consecință a echilibrului dintre depunerea și degradarea colagenului.
Colagenul este componenta principală a matricei extracelulare a țesuturilor. Cantitatea de colagen este modificată în colon în perioada postoperatorie anastomoza colonului, în special în zona perianastomozei 29. Această modificare se datorează interacțiunii dintre sinteza, fixarea și degradarea acestuia în țesutul cicatricial. Având în vedere cele de mai sus, astăzi metodele de tracțiune sunt considerate standardul de aur pentru evaluarea vindecării rănilor.
Exudația- faza care urmeaza rapid alterarii si eliberarii neurotransmitatorilor. Constă dintr-un număr de etape: reacția patului microcirculator cu încălcări ale proprietăților reologice ale sângelui; permeabilitate vasculară crescută la nivelul microvasculaturii; exudarea componentelor plasmei sanguine; emigrarea celulelor sanguine; fagocitoză; formarea de exudat și infiltrat de celule inflamatorii.
Analiza histologică și densitometria colagenului. Microscopia optică este o tehnică utilizată pentru evaluarea procesului de vindecare a anastomozelor intestinale și este utilizată pe scară largă în studii clinice și experimentale. Importanța sa reală este într-o oarecare măsură pusă sub semnul întrebării de subiectivitatea în evaluare. Cu toate acestea, atunci când este efectuat de patologi cu experiență și imparțial, poate furniza date cantitative care sunt critice pentru analiza și compararea proceselor de cicatrizare.
O altă metodă histologică utilă, în principal în evaluarea și diferențierea tipurilor de colagen, este polarizarea cu picrosirius. Imunohistochimia este metoda de diagnosticare, care are ca scop detectarea antigenului unei celule sau al unui țesut, folosind un anticorp specific îndreptat împotriva acestei componente celulare 53 este utilizarea de anticorpi specifici cunoscuți și manipulați chimic în așa fel încât, după legarea de antigenele sau țesuturile sale celulare, datorită diverse reacții și utilizarea cromogenilor, duce la o schimbare de culoare vizibilă la microscopie optică, indicând un antigen specific și cuantificându-l 60.
Schema XI. Acțiunea mediatorilor inflamatori de origine celulară (țesut).
nia
 Reacția patului de microcirculație cu încălcări ale proprietăților reologice ale sângelui- unul dintre cele mai strălucitoare semne morfologice ale inflamației. Modificările microvaselor încep cu un spasm reflex, o scădere a lumenului arteriolelor și precapilarelor, care este rapid înlocuită de o extindere a întregii rețele vasculare a zonei de inflamație și, mai ales, postcapilare și venule. Hiperemia inflamatorie determină creșterea temperaturii (calor)și roșeață (rubor) zona inflamata. Cu un spasm inițial, fluxul de sânge în arteriole devine accelerat și apoi încetinit. LA vase limfatice, ca și în sânge, mai întâi are loc o accelerare a fluxului limfatic și apoi încetinirea acestuia. Vasele limfatice debordează cu limfă și leucocite.
Reacția patului de microcirculație cu încălcări ale proprietăților reologice ale sângelui- unul dintre cele mai strălucitoare semne morfologice ale inflamației. Modificările microvaselor încep cu un spasm reflex, o scădere a lumenului arteriolelor și precapilarelor, care este rapid înlocuită de o extindere a întregii rețele vasculare a zonei de inflamație și, mai ales, postcapilare și venule. Hiperemia inflamatorie determină creșterea temperaturii (calor)și roșeață (rubor) zona inflamata. Cu un spasm inițial, fluxul de sânge în arteriole devine accelerat și apoi încetinit. LA vase limfatice, ca și în sânge, mai întâi are loc o accelerare a fluxului limfatic și apoi încetinirea acestuia. Vasele limfatice debordează cu limfă și leucocite.
Pentru a studia vindecarea, se folosește definiția angiogenezei și a miofibroblastelor. Studii experimentale recente au demonstrat o corelație directă între rezistența maximă la tracțiune și cuantificarea vasculară și a miofibroblastelor în evaluarea vindecării țesuturilor 4, 48.
Biologia moleculară a oferit cuantificarea factorilor de creștere prin reacții complexe folosind material genetic găsit în țesutul de granulație a plăgii. Într-o teză de doctorat recentă, Pereira a studiat factorii de creștere din rănile pielii și a concluzionat că doza lor este direct corelată cu morfometria colagenului 41.
În țesuturile avasculare (cornee, valve cardiace), la începutul inflamației, predomină fenomenele de alterare, iar apoi vasele din zonele învecinate cresc (aceasta se întâmplă foarte repede) și sunt incluse în reacția inflamatorie.
Modificări ale proprietăților reologice ale sângelui consta in faptul ca in venule si postcapilare dilatate cu flux sanguin lent, distributia leucocitelor si eritrocitelor in fluxul sanguin este perturbata. Leucocitele polimorfonucleare (neutrofile) ies din curentul axial, se adună în zona marginală și sunt situate de-a lungul peretelui vasului. margine-
Cheloizi hipertrofici și cicatrici. Cheloizii și cicatricile hipertrofice sunt tulburări de vindecare și se diferențiază prin comportamentul clinic; cheloizii se extind dincolo de incizia 52, în timp ce cicatricile hipertrofice rămân limitate la incizia 33.
Ambele se datorează unui răspuns inflamator excesiv în timpul tratamentului, cu pierderea controlului normal între sinteza și degradare 1. Printre factorii implicați în patogeneza acestuia includ leziunea, disfuncția fibroblastelor, nivelurile crescute de factori de creștere sau alte citokine și reducerea apoptozei. Sunt mai frecvente la negri și oameni orientali.
intregul aranjament al neutrofilelor este inlocuit cu lor marginea în picioare, care precede emigrareîn afara vasului.
Modificări ale hemodinamicii și tonusului vascular în focarul inflamației duc la stazăîn postcapilare și venule, care este înlocuită tromboză. Aceleași modificări apar și în vasele limfatice. Astfel, odată cu fluxul continuu de sânge în focarul inflamației, ieșirea acestuia, precum și limfa, sunt perturbate. Blocarea vaselor de sânge și limfatice eferente permite focalizării inflamației să acționeze ca o barieră care împiedică generalizarea procesului.
Nu există nicio diferență histologică între cicatricile cheloide și cele hipertrofice, dar microscopia electronică observată în jurul materiei amorfe din fibroblastele cheloide 20. Există o activitate metabolică mai mare și prezența anticorpilor antinucleari în 55 de cheloizi. Chiar și astăzi cea mai buna metoda tratamentul cicatricilor hipertrofice și cheloide este prevenirea. Procedurile chirurgicale inutile 49 ar trebui evitate, iar dacă acest lucru nu este posibil, rănile trebuie închise cu stres minim. De asemenea, este important de menționat că îngrijirea locală, cum ar fi hemostaza, manipularea adecvată a țesuturilor, utilizarea suturilor monofilament și manipularea țesuturilor imobilizate sunt factori preventivi importanți.
Creșterea permeabilității vasculare la nivelul microvasculaturii este unul dintre semnele esențiale ale inflamației. Întreaga gamă de modificări tisulare, originalitatea formelor de inflamație sunt în mare măsură determinate de starea de permeabilitate vasculară, de adâncimea leziunii sale. Un rol important în implementarea permeabilității crescute a vaselor microvasculare aparține ultrastructurilor celulare deteriorate, ceea ce duce la micropinocitoză crescută. asociat cu permeabilitate vasculară crescută exudarea în țesuturi și cavități ale părților lichide ale plasmei, emigrarea celulelor sanguine, educaţie exudat(revărsat inflamator) și infiltrat celular inflamator.
Exudația părțile constitutive plasmă sângele este considerat ca o manifestare a unei reacții vasculare care se dezvoltă în patul de microcirculație. Se exprimă în ieșirea din vas a componentelor lichide ale sângelui: apă, proteine, electroliți.
Emigrarea celulelor sanguine acestea. ieșirea lor din fluxul sanguin prin peretele vaselor de sânge se realizează cu ajutorul mediatorilor chemotactici (vezi Schema X). După cum sa menționat deja, emigrarea este precedată de situația marginală a neutrofilelor. Ele aderă la peretele vasului (în special în postcapilare și venule), apoi formează procese (pseudopodia) care pătrund între celulele endoteliale - emigrarea interendotelială(Fig. 63). Neutrofilele traversează membrana bazală, cel mai probabil pe baza fenomenului tixotropie(tixotropie - scăderea izometrică reversibilă a vâscozității coloizilor), adică. trecerea gelului membranar la sol atunci când celula atinge membrana. În țesutul perivascular, neutrofilele își continuă mișcarea cu ajutorul pseudopodiilor. Procesul de migrare a leucocitelor se numește leucodiapedeză,și eritrocite - eritrodiapedeză.
Fagocitoză(din greaca. phagos- devoreaza si kitos- receptacul) - absorbția și digestia de către celule (fagocite) a diverselor corpuri atât de natură vii (bacterii), cât și neînsuflețite (corpi străini). Fagocitele pot fi o varietate de celule, dar în inflamație, neutrofilele și macrofagele sunt de cea mai mare importanță.
Fagocitoza este asigurată de o serie de reacții biochimice. În timpul fagocitozei, conținutul de glicogen din citoplasma fagocitei scade, ceea ce este asociat cu glicogenoliza anaerobă îmbunătățită, care este necesară pentru a genera energie pentru fagocitoză; substanțele care blochează glicogenoliza inhibă și fagocitoza.
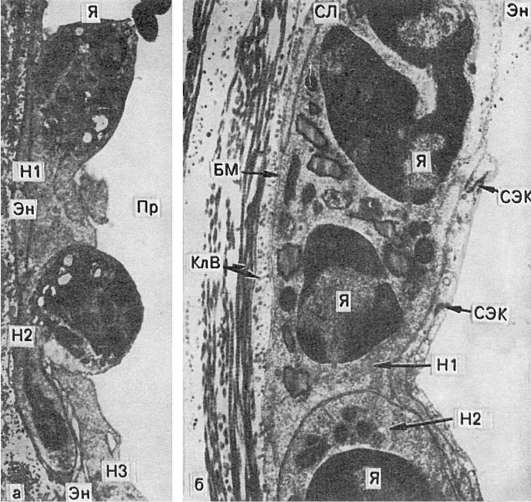 Orez. 63. Emigrarea leucocitelor prin peretele vasului în timpul inflamației:
Orez. 63. Emigrarea leucocitelor prin peretele vasului în timpul inflamației:
a - unul dintre neutrofile (H1) este aproape adiacent endoteliului (En), celălalt (H2) are un nucleu bine definit (N) și pătrunde în endoteliu (En). Majoritatea acestor leucocite sunt localizate în stratul subendotelial. Pe endoteliul din această zonă sunt vizibile pseudopode ale celui de-al treilea leucocit (H3); Pr - lumenul vasului. x9000; b - neutrofilele (SL) cu nuclei bine conturați (N) sunt situate între endoteliu și membrana bazală (BM); joncțiunile celulelor endoteliale (ECC) și fibrelor de colagen (CLF) din spatele membranei bazale. x20.000 (conform Flory și Grant)
Se formează un obiect fagocitar (bacterie) înconjurat de o citomembrană invaginată (fagocitoză - pierderea citomembranei fagocitare). fagozom. Când fuzionează cu un lizozom, fagolizozom(lizozom secundar), în care digestia intracelulară se realizează cu ajutorul enzimelor hidrolitice - fagocitoză finalizată(Fig. 64). În fagocitoza completă, proteinele cationice antibacteriene ale lizozomilor neutrofili joacă un rol important; ele ucid microbii, care sunt apoi digerați. În cazurile în care microorganismele nu sunt digerate de fagocite, mai des de macrofage și se înmulțesc în citoplasma lor, ele vorbesc despre fagocitoză incompletă, sau endocitobioza. A lui
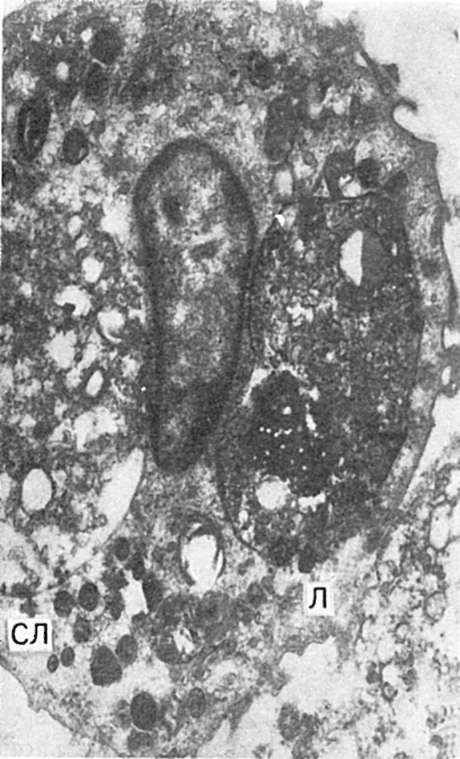 Orez. 64. Fagocitoză. Macrofag cu fragmente de leucocite fagocitate (SL) și incluziuni lipidice (L). electronogramă. x 20.000.
Orez. 64. Fagocitoză. Macrofag cu fragmente de leucocite fagocitate (SL) și incluziuni lipidice (L). electronogramă. x 20.000.
explicată din multe motive, în special, prin faptul că lizozomii macrofagilor pot conține o cantitate insuficientă de proteine cationice antibacteriene sau sunt complet lipsiți de ele. Astfel, fagocitoza nu este întotdeauna o reacție de protecție a organismului și uneori creează premisele pentru diseminarea microbilor.
Formarea de exudat și infiltrat de celule inflamatorii completează procesele de exudare descrise mai sus. Exudarea părților lichide ale sângelui, emigrarea leucocitelor, diapedeza eritrocitelor duc la apariția în țesuturile sau cavitățile corpului afectate a unui lichid inflamator - exudat. Acumularea de exudat în țesut duce la creșterea volumului acestuia (tumoare) compresie nervoasă și durere (dolor), a cărui apariție în timpul inflamației este, de asemenea, asociată cu influența mediatorilor (bradikinină), la o încălcare a funcției unui țesut sau organ (functio laesa).
De obicei, exudatul conține mai mult de 2% proteine. În funcție de gradul de permeabilitate al peretelui vasului, diferite proteine pot pătrunde în țesut. Cu o ușoară creștere a permeabilității barierei vasculare, prin aceasta pătrund în principal albuminele și globulinele și, cu un grad ridicat de permeabilitate, împreună cu acestea ies și proteine moleculare mari, în special fibrinogen. În unele cazuri, neutrofilele predomină în exudat, în altele - limfocite, monocite și histiocite, în altele - eritrocite.
Odată cu acumularea de celule exsudate în țesuturi, și nu partea sa lichidă, ei vorbesc infiltrat de celule inflamatorii,în care pot predomina atât elementele hematogene cât şi cele histiogene.
Proliferare(reproducția) celulelor este faza finală a inflamației, care vizează refacerea țesutului deteriorat. Numărul de celule cambiale mezenchimale, limfocite B și T și monocite crește. Când celulele se înmulțesc în focarul inflamației, se observă diferențierea și transformarea celulelor (Schema XII): celulele mezenchimale cambiale se diferențiază în fibroblaste; limfocitele B
Schema XII. Diferențierea și transformarea celulelor în timpul inflamației
 da naștere la educație celule plasmatice. Limfocitele T, aparent, nu se transformă în alte forme. Monocitele dau naștere histiociteși macrofage. Macrofagele pot fi o sursă de educație epitelioidși celule gigantice(celule de corpuri străine și Pirogov-Langhans).
da naștere la educație celule plasmatice. Limfocitele T, aparent, nu se transformă în alte forme. Monocitele dau naștere histiociteși macrofage. Macrofagele pot fi o sursă de educație epitelioidși celule gigantice(celule de corpuri străine și Pirogov-Langhans).
În diferite stadii de proliferare a fibroblastelor, produse activitățile lor – proteine colagenși glicozaminoglicani, apărea argirofilși fibre de colagen, substanță intercelularățesut conjunctiv.
În procesul de proliferare în timpul inflamației, este, de asemenea, implicat epiteliu(vezi Schema XII), care este deosebit de pronunțată la nivelul pielii și mucoaselor (stomac, intestine). În acest caz, epiteliul în proliferare poate forma excrescențe polipe. Proliferarea celulară în domeniul inflamației servește drept reparație. În același timp, diferențierea structurilor epiteliale proliferante este posibilă numai cu maturarea și diferențierea țesutului conjunctiv (Garshin V.N., 1939).
Inflamația cu toate componentele sale apare numai în etapele ulterioare ale dezvoltării fetale. La făt, nou-născut și copil, inflamația are o serie de caracteristici. Prima caracteristică a inflamației este predominarea componentelor alternative și productive, deoarece acestea sunt filogenetic mai vechi. A doua caracteristică a inflamației asociate cu vârsta este tendința proces local la distributie si generalizare datorita imaturitatii anatomice si functionale a organelor de imunogeneza si a tesuturilor de bariera.
Reglarea inflamației efectuate cu ajutorul hormonal, nervos și factori imunitari. S-a stabilit că unii hormoni, precum hormonul somatotrop (GH) al glandei pituitare, deoxicorticosteronul, aldosteronul, cresc răspunsul inflamator. (hormoni proinflamatori) alții - glucocorticoizii și hormonul adrenocorticotrop (ACLT) al glandei pituitare, dimpotrivă, o reduc (hormoni antiinflamatori). substanțe colinergice, prin stimularea eliberării mediatorilor inflamatori,
acționează ca hormonii proinflamatori și adrenergic, inhibă activitatea mediatorului, se comportă ca hormonii antiinflamatori. Severitatea reacției inflamatorii, rata dezvoltării și natura acesteia sunt afectate de starea de imunitate. Inflamația decurge mai ales rapid în condiții de stimulare antigenică (sensibilizare); în astfel de cazuri se vorbeşte despre imun, sau alergică, inflamație(vezi Procese imunopatologice).
Exod inflamația este diferită în funcție de etiologia sa și de natura cursului, de starea corpului și de structura organului în care se dezvoltă. Produsele de degradare a țesuturilor suferă clivaj enzimatic și resorbție fagocitară, are loc resorbția produselor de descompunere. Mulțumită proliferarea celulară focarul inflamației este înlocuit treptat de celulele țesutului conjunctiv. Dacă focarul inflamației a fost mic, poate apărea restaurarea completă a țesutului anterior. Cu un defect tisular semnificativ, se formează o cicatrice la locul focalizării.
Terminologia și clasificarea inflamației
În cele mai multe cazuri, denumirea inflamației unui anumit țesut (organ) este de obicei compusă prin adăugarea finalului la numele latin și grecesc al organului sau țesutului. -este, iar la rusă - -it. Deci, inflamația pleurei este desemnată ca pleurită- pleurezie, inflamație a rinichilor - nefrită- nefrită, inflamație a gingiilor - gingivita- gingivita etc. Inflamația unor organe are denumiri speciale. Deci, inflamația faringelui se numește angină (din greacă. ancho- suflet, stoarcere), pneumonie - pneumonie, inflamație a unui număr de cavități cu acumulare de puroi în ele - empiem (de exemplu, empiem al pleurei), inflamație purulentă a foliculului de păr cu cel adiacent glanda sebaceeși țesături - furuncul (din lat. furiare- înfurie), etc.
Clasificare. Se ține cont de natura derulării procesului și de formele morfologice, în funcție de predominanța fazei exsudative sau proliferative a inflamației. După natura fluxului, ele disting inflamație acută, subacută și cronică, prin predominanţa fazei exudative sau proliferative a reacţiei inflamatorii - exudativ și.
Până de curând, printre formele morfologice de inflamație, inflamație alternativă,în care predomină alterarea (inflamația necrotică), iar exsudația și proliferarea sunt extrem de slabe sau deloc exprimate. În prezent, existența acestei forme de inflamație este negata de majoritatea patologilor pe motiv că în așa-numita inflamație alternativă nu există, în esență, o reacție vascular-mezenchimală (exudație și proliferare), care este esența reacției inflamatorii. Astfel, în acest caz, nu vorbim despre inflamaţie oh oh necroză. Conceptul de inflamație alternativă a fost creat de R. Virchow, care a pornit de la „teoria sa nutritivă” a inflamației (s-a dovedit a fi eronată), așa că a numit inflamație alternativă parenchimatoase.
Forme morfologice de inflamație
Inflamație exudativă
Inflamație exudativă caracterizată prin predominanţa exsudaţiei şi formarea exsudatului în ţesuturi şi cavităţile corpului. În funcție de natura exudatului și de localizarea predominantă a inflamației, se disting următoarele tipuri de inflamație exsudativă: 1) seroasă; 2) fibrinos; 3) purulent; 4) putred; 5) hemoragic; 6) cataral; 7) mixt.
Inflamație seroasă. Se caracterizează prin formarea de exudat care conține până la 2% proteine și o cantitate mică elemente celulare. Cursul inflamației seroase este de obicei acut. Apare mai des în cavitățile seroase, mucoase și meninge, mai rar în organele interne, piele.
Tabloul morfologic. LA cavități seroase se acumulează exudat seros - un lichid tulbure, sărac în elemente celulare, printre care predomină celulele mezoteliale dezumflate și neutrofilele singulare; scoicile devin pline de sânge. Aceeași imagine reiese și pentru meningita seroasa. Cu inflamație membrana mucoasă, care devin și sângele, mucusul și celulele epiteliale dezumflate sunt amestecate cu exudatul, catar seros membrana mucoasă (vezi descrierea de mai jos catar). LA ficat fluidul se acumulează în spaţiile perisinusoidale (Fig. 65), în miocardului între fibrele musculare în rinichi - în lumenul capsulei glomerulare. Inflamație seroasă piele, de exemplu, cu o arsură, se exprimă prin formarea de vezicule care apar în grosimea epidermei, umplute cu un revărsat tulbure. Uneori, exudatul se acumulează sub epidermă și îl exfoliază din țesutul subiacent cu formarea de vezicule mari.
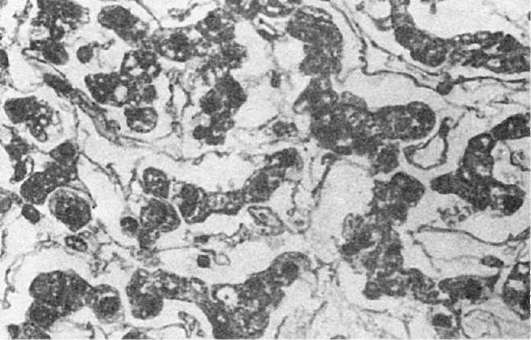 Orez. 65. Hepatită seroasă
Orez. 65. Hepatită seroasă
Cauză inflamația seroasă sunt diverși agenți infecțioși (mycobacterium tuberculosis, diplococul Frenkel, meningococul, shigella), expunerea la factori termici și chimici, autointoxicarea (de exemplu, cu tireotoxicoză, uremie).
Exod inflamația seroasă este de obicei favorabilă. Chiar și o cantitate semnificativă de exudat poate fi absorbită. În organele interne (ficat, inimă, rinichi), scleroza se dezvoltă uneori ca urmare a inflamației seroase în cursul ei cronic.
Sens determinat de grad tulburări funcționale. În cavitatea cămășii inimii, efuziunea împiedică activitatea inimii, în cavitatea pleurală duce la colapsul (comprimarea) plămânului.
inflamație fibrinoasă. Se caracterizează prin formarea unui exudat bogat în fibrinogen, care în țesutul afectat (necrotic) se transformă în fibrină. Acest proces este facilitat de eliberarea unei cantități mari de tromboplastină în zona de necroză. Inflamația fibrinoasă este localizată în membranele mucoase și seroase, mai rar în grosimea organului.
Tabloul morfologic. Pe suprafața membranei mucoase sau seroase apare o peliculă gri-albicioasă (inflamație „membranoasă”). În funcție de adâncimea necrozei tisulare, de tipul de epiteliu al membranei mucoase, pelicula poate fi conectată lejer cu țesuturile subiacente și, prin urmare, poate fi ușor separată sau ferm și, prin urmare, dificil de separat. În primul caz, se vorbește despre crupus, iar în al doilea - despre varianta difterică a inflamației fibrinoase.
Inflamație crupoasă(din scotia. grup- film) apare cu necroza tisulara superficiala si impregnarea maselor necrotice cu fibrina (Fig. 66). Filmul, asociat vag cu țesutul subiacent, face ca membrana mucoasă sau seroasă să fie plictisitoare. Uneori se pare că coaja este, parcă, stropită cu rumeguș. membrană mucoasă se îngroașă, se umflă, dacă filmul este separat, apare un defect de suprafață. Membrana seroasă devine aspră, parcă acoperită cu fire de păr - fibrină. Cu pericardită fibrinoasă în astfel de cazuri, se vorbește despre o „inimă păroasă”. Printre organe interne inflamația crupusă se dezvoltă în plămân - pneumonie crupusă (vezi. pneumonie).
Inflamație difterică(din greaca. diftere- peliculă pieloasă) se dezvoltă cu necroză tisulară profundă şi impregnarea maselor necrotice cu fibrină (Fig. 67). Se dezvoltă pe membrana mucoasă. Filmul fibrinos este strâns lipit de țesutul subiacent; atunci când este respins, apare un defect profund.
Varianta de inflamație fibrinoasă (cropoasă sau difterică) depinde, după cum sa menționat deja, nu numai de profunzimea necrozei tisulare, ci și de tipul de epiteliu care căptușește mucoasele. Pe mucoasele acoperite cu epiteliu scuamos (cavitatea bucala, faringe, amigdale, epiglota, esofag, adevarat corzi vocale, colul uterin), filmele sunt de obicei strâns asociate cu epiteliul, deși necroza și prolapsul de fibrină sunt uneori limitate doar la acoperirea epitelială. Asta explica-
 Se datorează faptului că celulele epiteliului scuamos sunt strâns legate între ele și cu țesutul conjunctiv subiacent și, prin urmare, „țin ferm” filmul. În mucoasele acoperite cu epiteliu prismatic (tractul respirator superior, tract gastrointestinal etc.), legătura epiteliului cu țesutul subiacent este liberă, astfel încât filmele rezultate sunt ușor separate împreună cu epiteliul chiar și cu pierderi profunde de fibrină. Semnificația clinică a inflamației fibrinoase, de exemplu, în faringe și trahee este inegală chiar și cu aceeași cauză a apariției acesteia (durere în gât difteric și traheită croupoasă în difterie).
Se datorează faptului că celulele epiteliului scuamos sunt strâns legate între ele și cu țesutul conjunctiv subiacent și, prin urmare, „țin ferm” filmul. În mucoasele acoperite cu epiteliu prismatic (tractul respirator superior, tract gastrointestinal etc.), legătura epiteliului cu țesutul subiacent este liberă, astfel încât filmele rezultate sunt ușor separate împreună cu epiteliul chiar și cu pierderi profunde de fibrină. Semnificația clinică a inflamației fibrinoase, de exemplu, în faringe și trahee este inegală chiar și cu aceeași cauză a apariției acesteia (durere în gât difteric și traheită croupoasă în difterie).
Motivele inflamațiile fibrinoase sunt diferite. Poate fi cauzată de diplococi Frenkel, streptococi și stafilococi, agenți patogeni ai difteriei și dizenteriei, mycobacterium tuberculosis și virusurile gripale. Pe lângă agenții infecțioși, inflamația fibrinoasă poate fi cauzată de toxine și otrăvuri de origine endogenă (de exemplu, cu uremie) sau exogenă (cu otrăvire sublimată).
curgere inflamația fibrinoasă este de obicei acută. Uneori (de exemplu, cu tuberculoza membranelor seroase), este cronică.
Exod inflamația fibrinoasă a membranelor mucoase și seroase nu este aceeași. Pe membranele mucoase după respingerea filmelor, rămân defecte de diferite adâncimi - ulcere; cu inflamatia croupoasa sunt superficiale, cu difterie sunt profunde si lasa in urma modificari cicatriciale. Pe membranele seroase este posibilă resorbția exudatului fibrinos. Cu toate acestea, masele de fibrină suferă adesea organizare, ceea ce duce la formarea de aderențe între foile seroase ale pleurei, peritoneului și cămașa cardiacă. Ca urmare a inflamației fibrinoase, poate apărea o creștere excesivă completă a cavității seroase cu țesut conjunctiv - aceasta obliterarea.
Sens inflamația fibrinoasă este foarte mare, deoarece formează baza morfologică a multor boli (difterie, dizenterie),
observată cu intoxicaţie (uremie). Odată cu formarea de filme în laringe, trahee, există pericolul de asfixie; cu respingerea filmelor în intestin, este posibilă sângerare din ulcerele rezultate. După ce a suferit o inflamație fibrinoasă, pot rămâne ulcere cicatrici pe termen lung nevindecabile.
Inflamație purulentă. Se caracterizează prin predominanța neutrofilelor în exsudat. Neutrofile în descompunere, care se numesc corpuri purulente,împreună cu partea lichidă a exsudatului formează puroi. De asemenea, conține limfocite, macrofage, celule moarte ale țesuturilor, microbi. Puroiul este un lichid tulbure, gros, care are o culoare galben-verzuie. O trăsătură caracteristică a inflamației purulente este histoliza, datorită efectului asupra țesuturilor enzimelor proteolitice ale neutrofilelor. Inflamația purulentă apare în orice organ, orice țesut.
Tabloul morfologic. Inflamația purulentă, în funcție de prevalența ei, poate fi reprezentată de un abces sau flegmon.
abces (abces)- inflamație purulentă focală, caracterizată prin formarea unei cavități umplute cu puroi (Fig. 68). În timp, abcesul este delimitat de un arbore de țesut de granulație, bogat în capilare, prin ai cărui pereți are loc o emigrare crescută a leucocitelor. Formată ca și cum învelișul abcesului. În exterior, este format din fibre de țesut conjunctiv care sunt adiacente țesutului neschimbat, iar în interior - țesut de granulație și puroi, care este reînnoit continuu datorită eliberării de corpuri purulente prin granulații. Abcesul care produce puroi se numește membrana piogenă.
Flegmon - inflamație purulentă difuză, în care exudatul purulent se răspândește difuz între elementele tisulare, impregnând, exfoliind și lizand țesuturile. Cel mai adesea, flegmonul este observat acolo unde exudatul purulent își poate face ușor drum, adică. de-a lungul straturilor intermusculare, de-a lungul tendoanelor, fasciei, in țesut subcutanat, de-a lungul trunchiurilor neurovasculare etc.
Există flegmoni moi și tari. Flegmon moale caracterizată prin absența focarelor vizibile de necroză tisulară, flegmon dur- prezența unor astfel de focare care nu suferă fuziune purulentă, în urma căreia țesutul devine foarte dens; țesutul mort este îndepărtat. Flegmo-
 pe tesutul adipos (celulita) se caracterizeaza prin distributie nelimitata. Poate exista o acumulare de puroi în cavitățile corpului și în unele organe goale, care se numește empiem
(empiem al pleurei, vezicii biliare, apendice etc.).
pe tesutul adipos (celulita) se caracterizeaza prin distributie nelimitata. Poate exista o acumulare de puroi în cavitățile corpului și în unele organe goale, care se numește empiem
(empiem al pleurei, vezicii biliare, apendice etc.).
Cauză inflamația purulentă sunt mai des microbi piogeni (stafilococ, streptococ, gonococi, meningococi), mai rar diplococi Frenkel, bacili tifoizi, mycobacterium tuberculosis, ciuperci etc. Inflamația purulentă aseptică este posibilă atunci când anumite substanțe chimice intră în țesut.
curgere inflamația purulentă poate fi acută și cronică. Inflamație purulentă acută, reprezentat de un abces sau flegmon, tinde să se răspândească. Ulcerele, care topesc capsula organului, se pot sparge în cavitățile învecinate. Între abces și cavitatea în care a spart puroiul, există pasaje fistuloase.În aceste cazuri, este posibil să se dezvolte empiem. Inflamația purulentă, atunci când se răspândește, trece la organele și țesuturile învecinate (de exemplu, pleurezia apare cu un abces pulmonar, iar peritonita apare cu un abces hepatic). Cu un abces și flegmon, se poate obține un proces purulent limfogenși răspândire hematogenă, care duce la dezvoltare septicopiemie(cm. Septicemie).
Inflamație cronică supurată se dezvoltă atunci când abcesul este încapsulat. În același timp, scleroza se dezvoltă în țesuturile din jur. Dacă puroiul în astfel de cazuri găsește o cale de ieșire, apare pasaje fistuloase cronice, sau fistule, care sunt deschise prin piele afară. Dacă pasajele fistuloase nu se deschid, iar procesul continuă să se răspândească, abcesele pot apărea la o distanță considerabilă de focarul primar al inflamației purulente. Astfel de ulcere îndepărtate sunt numite abces sinterizat, sau bazin. Cu un curs lung, inflamația purulentă se răspândește prin fibrele libere și formează dungi extinse de puroi, provocând intoxicație severă și ducând la epuizarea organismului. În rănile complicate de supurația plăgii, a epuizarea ranilor, sau febră purulent-resorbtivă(Davydovsky I.V., 1954).
Exod inflamația purulentă depinde de prevalența sa, de natura cursului, de virulența microbilor și de starea corpului. În cazurile adverse, poate apărea generalizarea infecției, se dezvoltă sepsis. Dacă procesul este delimitat, abcesul este deschis spontan sau chirurgical, ceea ce duce la eliberarea de puroi. Cavitatea abcesului este umplută cu țesut de granulație, care se maturizează și se formează o cicatrice în locul abcesului. Un alt rezultat este, de asemenea, posibil: puroiul din abces se îngroașă, se transformă în detritus necrotic, care suferă pietrificare. Inflamația purulentă prelungită duce adesea la amiloidoza.
Sens inflamația purulentă este determinată în primul rând de capacitatea sa de a distruge țesuturile (histoliză), ceea ce face posibilă răspândirea procesului purulent prin contact, limfogen și hematogen.
cale. Inflamația purulentă stă la baza multor boli, precum și a complicațiilor acestora.
Inflamație putridă(gangrenos, ichorus, din greacă. sângele zeilor- icor). De obicei, se dezvoltă ca urmare a pătrunderii bacteriilor putrefactive în locul inflamației, provocând descompunerea țesuturilor cu formarea de gaze urât mirositoare.
Inflamație hemoragică. Apare atunci când exudatul conține o mulțime de globule roșii. În dezvoltarea acestui tip de inflamație, rolul nu este doar al unei permeabilitati puternic crescute a microvaselor, ci și al chimiotaxiei negative în raport cu neutrofilele. Inflamația hemoragică apare în bolile infecțioase severe - antrax, ciumă, gripă etc. Uneori există atât de multe eritrocite încât exudatul seamănă cu o hemoragie (de exemplu, cu meningoencefalita cu antrax). Adesea, inflamația hemoragică se alătură altor tipuri de inflamație exudativă.
Rezultatul inflamației hemoragice depinde de cauza care a provocat-o.
Catar(din greaca. catarreo- curgere în jos), sau Qatar. Se dezvoltă pe mucoase și se caracterizează excreție copioasă exudat pe suprafața lor (Fig. 69). Exudatul poate fi seros, mucos, purulent, hemoragic, iar celulele descuamate sunt întotdeauna amestecate cu el. epiteliul tegumentar. Catarul poate fi acut sau cronic. Catar acut caracteristic unui număr de infecții (de exemplu, catarul acut al suprafeței tractului respirator cu infecţii respiratorii acute). În același timp, o schimbare de la un tip de catar la altul este caracteristică - catarul seros este mucos, iar mucosul este purulent sau purulent-hemoragic. Catar cronic apare atât în boli infecțioase (bronșită cronică catarrală purulentă) cât și neinfectioase (gastrita cronică catarrală). Catarul cronic este însoțit de atrofie (catar atrofic) sau hipertrofie (catar hipertrofic) membrană mucoasă.
 Orez. 69. bronșită catarală
Orez. 69. bronșită catarală
Motivele catarul sunt diferite. Cel mai adesea, catarurile sunt de natură infecțioasă sau infecțioasă-alergică. Se pot dezvolta în timpul autointoxicației (gastrită și colită catarrală uremică), datorită expunerii la agenți termici și chimici.
Sens inflamația catarală este determinată de localizarea sa, intensitatea, natura cursului. Cea mai mare valoare dobândesc cataruri ale mucoaselor tractului respirator, adesea luând un caracter cronic și având consecințe severe (emfizem, pneumoscleroză). Nu mai puțin important este catarul gastric cronic, care contribuie la dezvoltarea unei tumori.
Inflamație mixtă.În acele cazuri când un alt tip de exudat se unește, se observă inflamație mixtă. Apoi se vorbește despre inflamația sero-purulentă, sero-fibrinoasă, purulent-hemoragică sau fibrinos-hemoragică. Mai des, se observă o schimbare a tipului de inflamație exsudativă cu adăugarea unei noi infecții, o schimbare a reactivității corpului.
Inflamație proliferativă (productivă).
Inflamație proliferativă (productivă). caracterizat printr-o predominanţă a proliferării elementelor celulare şi tisulare. Modificările alterative și exsudative trec în plan secund. Ca urmare a proliferării celulare, se formează infiltrate celulare focale sau difuze. Pot fi polimorfocelulare, limfocitare monocitare, macrofage, plasmocite, epitelioide, gigantice etc.
Inflamația productivă apare în orice organ, orice țesut. Se disting următoarele tipuri de inflamație proliferativă: 1) interstițială (interstițială); 2) granulomatos; 3) inflamație cu formarea de polipi și veruci genitale.
Inflamație interstițială (interstitială). Se caracterizează prin formarea unui infiltrat celular în stromă - miocard (Fig. 70), ficat, rinichi, plămâni. Infiltratul poate fi reprezentat de histiocite, monocite, limfocite, plasmocite, mastocite, neutrofile simple, eozinofile. Progresia inflamației interstițiale duce la dezvoltarea țesutului conjunctiv fibros matur - se dezvoltă scleroză (vezi Diagrama XII).
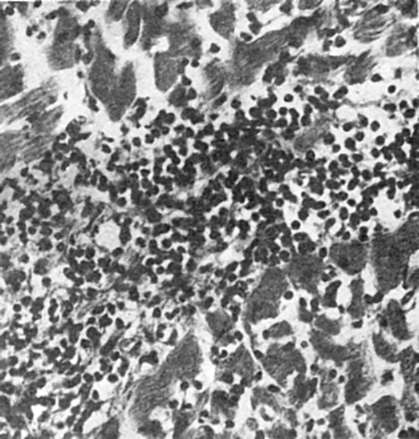 Orez. 70. Miocardită interstițială (interstitială).
Orez. 70. Miocardită interstițială (interstitială).
Dacă există multe plasmocite în infiltratul celular, atunci ele se pot transforma în formațiuni sferice omogene, care se numesc bile hialip, sau corpi fuchsinofili(Corpi Roussel). Extern, organele cu inflamație interstițială se modifică puțin.
Inflamație granulomatoasă. Se caracterizează prin formarea de granuloame (noduli) rezultate din proliferarea și transformarea celulelor capabile de fagocitoză.
Morfogeneza granuloamele constau în 4 etape: 1) acumularea de fagocite monocitare tinere în locul afectarii tisulare; 2) maturarea acestor celule în macrofage și formarea unui granulom macrofag; 3) maturarea și transformarea fagocitelor și macrofagelor monocitare în celule epitelioide și formarea unui granulom cu celule epitelioide; 4) fuziunea celulelor epitelioide (sau macrofagelor) și formarea celulelor gigantice (celule ale corpurilor străine sau celule Pirogov-Langhans) și celule epitelioide sau granulom cu celule gigantice. Celulele gigantice sunt caracterizate printr-un polimorfism semnificativ: de la 2-3-nucleare la simplaste gigantice care conțin 100 de nuclee sau mai mult. În celulele gigantice ale corpurilor străine, nucleele sunt distribuite uniform în citoplasmă, în celulele Pirogov-Langhans - în principal de-a lungul periferiei. Diametrul granuloamelor, de regulă, nu depășește 1-2 mm; mai des se găsesc doar la microscop. Rezultatul granulomului este scleroza.
Astfel, ghidat caracteristici morfologice, trebuie distinse trei tipuri de granuloame: 1) granulom macrofag (granulom simplu sau fagocitom); 2) granulom cu celule epitelioide (epiteloidocitom); 3) granulom cu celule gigantice.
În funcție de nivelul metabolismului, granuloamele se disting cu niveluri scăzute și ridicate de metabolism. Granuloame cu nivel scăzut schimb valutar apar atunci când sunt expuse la substanțe inerte (corpi străini inerți) și constau în principal din celule gigantice de corpuri străine. Granuloame cu nivel inalt schimb valutar apar sub actiunea stimulilor toxici (mycobacterium tuberculosis, lepra etc.) si sunt reprezentate de noduli de celule epitelioide.
Etiologie granulomatoza este variată. Există granuloame infecțioase, neinfecțioase și neidentificate. Granuloame infecțioaseîntâlnit cu tifos și febră tifoidă, reumatism, rabie, encefalită virală, tularemie, bruceloză, tuberculoză, sifilis, lepră, sclerom. Granuloame neinfecțioase apar cu boli de praf (silicoza, talcoza, azbestoza, bisinoza etc.), efectele medicamentoase (hepatita granulomatoasa, boala oleogranulomatoasa); apar si in jurul corpurilor straine. La granuloame de natură necunoscută includ granuloamele în sarcoidoză, bolile Crohn și Horton, granulomatoza Wegener etc. Ghidat după etiologie, în prezent se distinge un grup boli granulomatoase.
Patogeneza granulomatoza este ambiguă. Se știe că sunt necesare două condiții pentru dezvoltarea unui granulom: prezența unor substanțe capabile să stimuleze
lyat sistemul de fagocite monocitare, maturarea și transformarea macrofagelor și rezistența stimulului la fagocite. Aceste condiții sunt percepute în mod ambiguu de către sistemul imunitar. În unele cazuri, un granulom, în celulele epitelioide și gigantice, a cărui activitate fagocitară este brusc redusă, în caz contrar, fagocitoza, este înlocuită cu endocitobioză, devine o expresie. reacții de hipersensibilitate de tip întârziat.În aceste cazuri, se vorbește despre granulom imunitar, care are de obicei o morfologie epitelioid-celulară cu celule gigantice Pirogov-Langhans. În alte cazuri, când fagocitoza în celulele granulomului este relativ suficientă, se vorbește despre granulom non-imun, care este reprezentat de obicei printr-un fagocitom, mai rar printr-un granulom cu celule gigantice, format din celule de corpi straini.
Granuloamele sunt, de asemenea, împărțite în specifice și nespecifice. specific se numesc acele granuloame, a căror morfologie este relativ specifică pentru o anumită boală infecțioasă, al cărei agent cauzal poate fi găsit în celulele granulomului în timpul examenului histobacterioscopic. Granuloamele specifice (anterior erau la baza așa-numitei inflamații specifice) includ granuloamele în tuberculoză, sifilis, lepră și sclerom.
granulom tuberculos are următoarea structură: în centrul ei există un focar de necroză, de-a lungul periferiei - un arbore de celule epitelioide și limfocite cu un amestec de macrofage și celule plasmatice. Între celulele epitelioide și limfocite se află celule gigantice Pirogov-Langhans (Fig. 71, 72), care sunt foarte tipice pentru granulomul tuberculos. Atunci când este impregnat cu săruri de argint, printre celulele granulomului se găsește o rețea de fibre argirofile. Un număr mic de capilare sanguine se găsesc numai în zonele exterioare
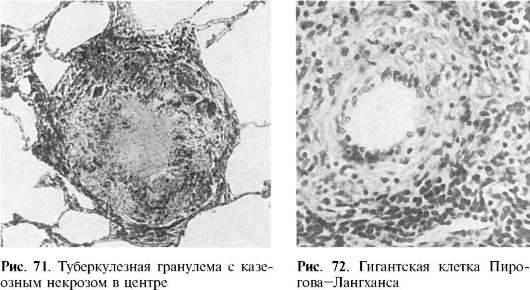 tubercul. Mycobacterium tuberculosis este detectat în celulele gigantice atunci când este colorat conform Ziehl-Neelsen.
tubercul. Mycobacterium tuberculosis este detectat în celulele gigantice atunci când este colorat conform Ziehl-Neelsen.
reprezentat de un focar extins de necroză, înconjurat de un infiltrat celular de limfocite, plasmocite și celule epitelioide; Celulele gigantice Pirogov-Langhans sunt rare (Fig. 73). Gumma se caracterizează prin formarea rapidă a țesutului conjunctiv în jurul focarului de necroză cu multe vase cu endoteliu proliferant (endovasculită). Uneori, într-un infiltrat celular, este posibil să se dezvăluie un treponem palid prin metoda argintării.
Granulom de lepră (leprom) Este reprezentat de un nodul, format în principal din macrofage, precum și din limfocite și plasmocite. Dintre macrofage se disting celulele mari cu vacuole grase care conțin lepră de micobacterium ambalate sub formă de bile. Aceste celule, foarte caracteristice lepromelor, sunt numite Celulele de lepră ale lui Virchow(Fig. 74). În descompunere, ei eliberează micobacterii, care sunt localizate liber printre celulele lepromei. Numărul de micobacterii din lepromă este enorm. Leproamele se unesc adesea pentru a forma țesut de granulație lepromatos bine vascularizat.
Sclerom granulom este format din plasmă și celule epitelioide, precum și din limfocite, printre care există multe bile hialine. Apariția unor macrofage mari cu o citoplasmă ușoară, numite celule Mikulich.În citoplasmă, agentul cauzal al bolii este detectat - bastoane Volkovich-Frisch (Fig. 75). Scleroza semnificativă și hialinoza țesutului de granulație sunt, de asemenea, caracteristice.
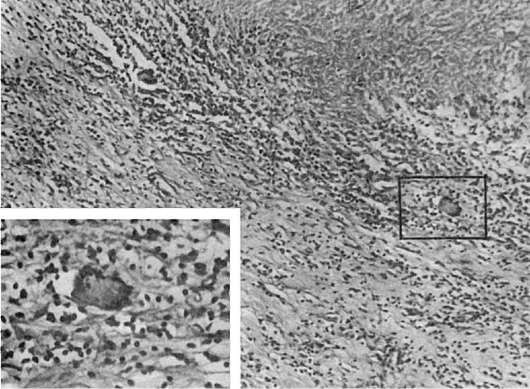 Orez. 73. Granulom sifilitic (guma)
Orez. 73. Granulom sifilitic (guma)
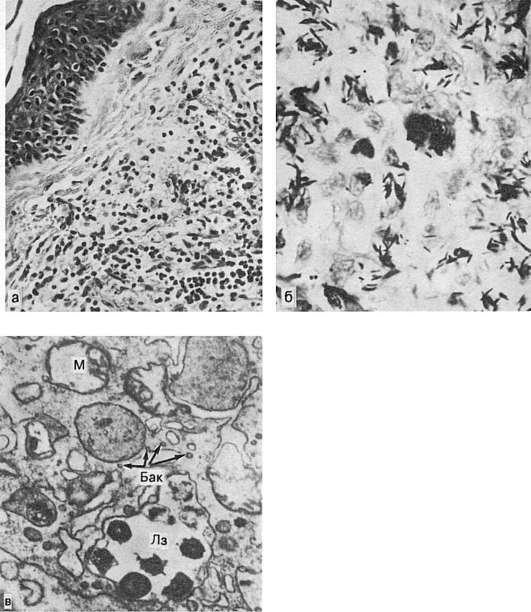 Orez. 74. Lepră:
Orez. 74. Lepră:
a - leproma cu forma lepromatoasa; b - un număr mare de micobacterii în nodul lepros; c - Celula de lepră a lui Virchow. În celulă există acumulări de micobacterii (Buck), un număr mare de lizozomi (Lz); distrugerea mitocondriilor (M). electronogramă. x25.000 (conform lui David)
 Orez. 75. Celula lui Mikulich în sclerom. În citoplasmă (C) sunt vizibile vacuole uriașe, care conțin bacili Volkovich-Frisch (B). PzK - celule plasmatice (după David). x7000
Orez. 75. Celula lui Mikulich în sclerom. În citoplasmă (C) sunt vizibile vacuole uriașe, care conțin bacili Volkovich-Frisch (B). PzK - celule plasmatice (după David). x7000
Granuloame nespecifice nu au trăsăturile caracteristice inerente granuloamelor specifice. Acestea apar într-un număr de boli infecțioase (de exemplu, granuloame tifoide și tifoide) și neinfecțioase (de exemplu, granuloame de silicoză și azbestozitate, granuloame de corp străin).
Exod dublu granulom - necroză sau scleroză, a cărei dezvoltare este stimulată de monokinele (interleukina I) ale fagocitelor.
Inflamație productivă cu formarea de polipi și veruci genitale. O astfel de inflamație se observă pe membranele mucoase, precum și în zonele care mărginesc epiteliul scuamos. Se caracterizează prin creșterea epiteliului glandular împreună cu celulele țesutului conjunctiv subiacent, ceea ce duce la formarea multor papile mici sau formațiuni mai mari numite polipi. Astfel de creșteri de polipoză sunt observate cu inflamația prelungită a membranei mucoase a nasului, stomacului, rectului, uterului, vaginului etc. În zonele epiteliului scuamos, care este situat în apropierea prismaticului (de exemplu, în anus, organe genitale), membranele mucoase sunt separate, iritând constant epiteliul scuamos, duce la creșterea atât a epiteliului, cât și a stromei. Ca rezultat, apar formațiuni papilare - veruci genitale. Ele sunt observate în sifilis, gonoree și alte boli însoțite de inflamație cronică.
curgere inflamația productivă poate fi acută, dar în majoritatea cazurilor cronică. Curs acut inflamația productivă este caracteristică unui număr de boli infecțioase(tifoid și tifos, tularemie, reumatism acut, glomerulită acută), curs cronic- pentru majoritatea proceselor productive intermediare la nivelul miocardului, rinichilor, ficatului, mușchilor, care se termină în scleroză.
Exod Inflamația productivă este diferită în funcție de tipul acesteia, de natura cursului și de caracteristicile structurale și funcționale ale organului și țesutului în care apare. Inflamația cronică productivă duce la dezvoltarea focală sau difuză scleroză organ. Dacă în același timp se dezvoltă deformarea (ridarea) organului și restructurarea lui structurală, atunci se vorbește despre ciroză. Acestea sunt nefrociroza ca rezultat al glomerulonefritei cronice productive, ciroza hepatică ca rezultat hepatită cronică, pneumociroza ca rezultat al pneumoniei cronice etc.
Sens inflamația productivă este foarte mare. Se observă în multe boli și, cu un curs lung, poate duce la scleroză și ciroză a organelor și, prin urmare, la insuficiența lor funcțională.
PRELEȚIA Nr. 5. Inflamația
Inflamația este o reacție complexă de protecție stromal-vasculară a organismului ca răspuns la acțiunea unui factor patologic.
În funcție de etiologie, se disting 2 grupe de inflamații:
1) banal;
2) specifice.
Specific este inflamația, care este cauzată de anumite cauze (patogeni). Aceasta este inflamația cauzată de Mycobacterium tuberculosis, inflamație în lepră (lepră), sifilis, actinomicoză. Inflamatiile cauzate de alti factori biologici (E. coli, coci), factori fizici, chimici sunt inflamatii banale.
În funcție de timpul cursului inflamației, există:
1) acută - durează 7-10 zile;
2) cronică - se dezvoltă de la 6 luni sau mai mult;
3) inflamatie subacuta - durata este intre acuta si cronica.
După morfologie (clasificarea anatomopatologică), se disting inflamația exudativă și proliferativă (productivă). Cauzele inflamației pot fi chimice, fizice sau biologice.
Fazele inflamației sunt alterarea, proliferarea și exudația. În faza de alterare se produce leziuni tisulare, care se manifestă patologic sub formă de distrugere și necroză. Au loc activarea și eliberarea de substanțe biologic active, adică sunt lansate procese de mediere. Mediatorii inflamației de origine celulară sunt mastocitele, trombocitele, bazofilele, limfocitele și monocitele; mediatori ai genezei plasmei - sistemul colecreina-chinină, sisteme complementare, de coagulare și anti-coagulare. Acțiunile acestor mediatori afectează cursul următoarei faze a inflamației - exudația. Mediatorii cresc permeabilitatea vaselor microvasculare, activează chemotaxia leucocitară, coagularea intravasculară, alterarea secundară în chiar focarul inflamației și activarea mecanismelor imune. În timpul exsudației în focarul de inflamație, arterială și congestie venoasă crește permeabilitatea peretelui vascular. Prin urmare, lichidul, proteinele plasmatice și, de asemenea, celulele sanguine încep să treacă în focarul inflamației. Coagularea intravasculară are loc cu deformarea vaselor din vasele de evacuare ale focarului de inflamație și astfel focarul este izolat. Proliferarea se caracterizează prin faptul că în focarul inflamației, celulele sanguine se acumulează în număr mare, precum și celulele de origine histogenă. Neutrofilele apar după câteva minute. Leucocitele îndeplinesc funcția de fagocitoză. Neutrofilele după 12 ore pierd glicogenul, se umplu cu grăsime și se transformă în corpuri purulente. Monocitele care au părăsit patul vascular sunt macrofage (simple și complexe) care sunt capabile de fagocitoză. Dar au puțini sau deloc cationi proteici bacterici, astfel încât macrofagele nu efectuează întotdeauna fagocitoză completă (endocitobioză), adică agentul patogen nu este distrus din organism, ci este absorbit de macrofag. Există trei tipuri de macrofage. Macrofagele simple sunt transportate în celulele epitelioide, sunt alungite, au un singur nucleu și arată ca un epiteliu (în tuberculoză). Celulele gigantice, care sunt de 15 până la 30 de ori mai mari decât celulele normale, provin din fuziunea mai multor celule epitelioide. Au formă rotundă, iar nucleii sunt localizați clar la periferie și se numesc celule Pirogov-Langhans. Celula gigantică a corpurilor străine se poate transforma instantaneu în histiocite. Sunt rotunde, iar nucleii sunt situati in centru.
Inflamația exudativă este o inflamație în care predomină procesele exsudative. Condiții de apariție:
1) impactul factorilor dăunători asupra vaselor microvasculare;
2) prezența unor factori speciali de patogenitate (flora piogenă, izolarea chemotaxiei); distinge între tipuri independente și neindependente de inflamație exsudativă. Speciile independente apar pe cont propriu, iar speciile neindependente li se alătură. Independent includ inflamația seroasă, fibrinoasă și purulentă. La dependent - inflamație catarrală, hemoragică și putrefactivă. Se distinge și inflamația mixtă - aceasta este o combinație de cel puțin 2 tipuri de inflamație.
Inflamația seroasă se caracterizează prin acumularea părții lichide a exudatului care conține aproximativ 2,5% proteine și diverse formele celulare(trombocite, leucocite, macrofage) și celule ale țesuturilor locale. Exudatul este similar cu transudatul care apare cu congestie venoasă, insuficiență cardiacă. Diferența dintre exudat și transudat este că prezența proteinei oferă un efect optic Gindal special - opalescență, adică strălucirea unei soluții coloidale în lumina transmisă. Localizare peste tot - în piele, mucoase, seroase și în parenchimul organelor; de exemplu, arsuri de gradul doi care formează vezicule. În cavitățile seroase, acumulările de lichid se numesc pericardită exudativă, pleurezie și peritonită. Membranele în sine sunt edematoase, pletorice, iar între ele există un lichid. Organele parenchimatoase devin mărite, flasc, pe tăietură țesutul este plictisitor, gri, asemănător cu carnea fiartă. Vederi microscopice: spații intercelulare extinse, goluri între celule, celulele sunt în stare de distrofie. Exudatul comprimă organele, perturbând funcția acestora. Dar practic rezultatul este favorabil, uneori trebuie să eliberați cantități mari de exudat. Rezultatul inflamației seroase în organele parenchimatoase este scleroza focală mică difuză și tulburările funcționale.
Inflamație fibrinoasă: exudatul este reprezentat de fibrinogen. Fibrinogenul este o proteină din sânge care, trecând dincolo de vasele de sânge, se transformă în fibrină insolubilă. Pe suprafețele organelor filmului se formează fire de fibrină care se împletesc - cenușii, de diferite grosimi. Apare pe membranele mucoase, seroase, precum și pe piele. În funcție de modul în care filmul este conectat la suprafață, există croupoase (formate pe membranele mucoase căptușite cu un epiteliu cu un singur strat) - dacă filmul este ușor separat de țesutul subiacent și difterie (pe epiteliu stratificat) - dacă filmul este slab despartite. Rezultatul inflamației fibrinoase depinde de tipul de inflamație. Filmele crupoase se caracterizează prin detașare ușoară, în timp ce membrana bazală nu suferă, are loc epitelizarea completă. Pe membranele seroase - respingerea filmului în cavitate, care nu are întotdeauna timp să fie resorbită de macrofage și are loc organizarea. Ca urmare, între foile parietale și viscerale ale membranei seroase corespunzătoare se formează aderențe fibroase - aderențe care limitează mobilitatea organelor. Dacă s-au format filme în tubul de respirație, atunci când sunt respinse, ele pot înfunda lumenul acestuia, provocând astfel asfixie. O astfel de complicație este o adevărată crupă (apare, în special, cu difterie). Este necesar să-l distingem de o crupă falsă care se dezvoltă cu stenoză a tubului respirator cu edem, cel mai adesea de natură alergică, cu SARS. Difteria are, în general, un rezultat favorabil din punct de vedere anatomic. Cu difterie, "inima de tigru", se poate observa miocardita parenchimatoasa severa. Uneori, sub filme se formează defecte profunde - eroziune, ulcere.
Cu inflamație purulentă, exudatul este reprezentat de leucocite polimorfonucleare, include leucocite moarte, țesuturi distruse. Culoare de la alb la galben-verde. localizare omniprezentă. Motivele sunt variate; în primul rând - flora cocică. Flora piogenă include stafilococi și streptococi, meningococi, gonococi și coli - intestinali, Pseudomonas aeruginosa. Unul dintre factorii de patogenitate ai acestei flore sunt așa-numitele leucocidine, acestea provocând o creștere a chemotaxiei leucocitelor asupra lor și moartea lor. În viitor, odată cu moartea leucocitelor, apar factori care stimulează chemotaxia noilor leucocite în focarul inflamației. Enzimele proteolitice, care sunt eliberate în timpul distrugerii, sunt capabile să-și distrugă atât propriile țesuturi, cât și țesuturile corpului. Prin urmare, există o regulă: „vedeți puroi - lăsați-l afară” pentru a preveni distrugerea propriilor țesuturi.
Există următoarele tipuri de inflamație purulentă.
1. Flegmon- difuză, difuză, fără limite clare, inflamație purulentă. Are loc infiltrarea difuză de către leucocite a diferitelor țesuturi (cel mai adesea - grăsime subcutanată, precum și pereții organelor goale, intestine - apendicita flegmonoasă). Inflamația flegmonoasă poate apărea în parenchimul oricărui organ.
2. Abces- inflamatie purulenta focala, delimitata. Alocați abcesul acut și cronic. Un abces acut are o formă neregulată, o margine neclară, neclară și nu există nicio degradare în centru. Un abces cronic are o formă regulată, cu limite clare și o zonă de degradare în centru. Claritatea graniței se datorează faptului că țesutul conjunctiv crește de-a lungul periferiei abcesului. În peretele unui astfel de abces se disting mai multe straturi - stratul interior este reprezentat de o membrană piogenă de țesut de granulație, iar partea exterioară a peretelui este formată din țesut conjunctiv fibros. Atunci când un abces este conectat la mediul extern cu ajutorul canalelor anatomice (în plămâni), în cavitate se formează un spațiu de aer, iar puroiul este situat orizontal (acest lucru se observă pe radiografie).
3. empiem- inflamație purulentă în cavitățile anatomice (empiem al pleurei, sinusurile maxilare, vezica biliara). Rezultatul inflamației purulente depinde de dimensiunea, forma, localizarea focarelor. Exudatul purulent se poate rezolva, uneori se dezvoltă scleroza - cicatrici ale țesutului. O complicație sub formă de eroziune a țesuturilor înconjurătoare de către enzimele proteolitice poate duce la formarea de fistule - canale prin care abcesul este golit în exterior (auto-curățare) sau în membrana seroasă (de exemplu, un abces pulmonar poate duce la dezvoltarea empiemului pleural, a ficatului - până la peritonită purulentă etc.); sângerare; epuizare; intoxicație etc.
Inflamație catarrală - mucusul este amestecat cu exudatul. Există o scurgere de exsudat de pe suprafața inflamată. Localizare tipică - mucoase. Rezultatul inflamației catarale este refacerea completă a mucoasei. În catarul cronic este posibilă atrofia mucoasei (rinită cronică atrofică).
Inflamația hemoragică se caracterizează prin amestecul de celule roșii din sânge la exudat. Exudatul devine roșu, apoi, pe măsură ce pigmenții sunt distruși, devine negru. De obicei când infecții virale precum gripa, rujeola, variola naturala (neagra), cu intoxicatii endogene, de exemplu, intoxicatie cu zgura azotata in cronice insuficiență renală. Este tipic pentru agenții patogeni ai infecțiilor deosebit de periculoase, care sunt puternice în virulență.
Inflamația putridă (gangrenoasă) apare ca urmare a atașării florei putrefactive, în primul rând fusospirochetale, la focarele de inflamație. Este mai frecventă în organele care au legătură cu mediul extern: gangrena putrefactivă a plămânilor, membrelor, intestinelor etc. Țesuturile în descompunere sunt terne, cu un miros specific fetid.
Inflamație mixtă. Se vorbește despre asta atunci când există o combinație de inflamație (seros-purulentă, seros-fibrinoasă, purulent-hemoragică sau fibrinos-hemoragică).
Productiv (inflamație proliferativă) - predomină faza de proliferare, având ca rezultat formarea de infiltrate celulare focale sau difuze, care pot fi polimorfo-celulare, limfocitare, macrofage, plasmocelulare, gigantice și epitelioide. Una dintre principalele condiții pentru dezvoltarea inflamației proliferative este stabilitatea relativă a factorilor dăunători în timpul medii interioare organism, capacitatea de a persista în țesuturi.
Caracteristicile inflamației proliferative:
1) curs ondulatoriu cronic;
2) localizarea în principal în țesuturile conjunctive, precum și în țesuturile ale căror celule au capacitatea de a prolifera - epiteliul pielii, intestinele.
În morfologie, trăsătura cea mai caracteristică este formarea țesutului de granulație. Țesutul de granulație este un țesut conjunctiv tânăr, imatur, în creștere. Formarea sa este determinată de proprietățile biologice clasice. Creșterea și funcționarea țesuturilor sunt procese antagoniste. Dacă țesutul începe să funcționeze bine, atunci creșterea sa încetinește și invers. Macroscopic, tesutul de granulatie este rosu, cu o suprafata granulara lucioasa si este predispus la sangerare. Substanța principală este translucidă, prin urmare, capilarele pline cu sânge strălucesc prin ea, de unde culoarea roșie. Țesătura este granulară, deoarece genunchii ridică substanța principală.
Soiuri de inflamație productivă:
1) interstițial sau interstițial;
2) granulomatos;
4) creșteri hipertrofice.
Inflamația intermediară se dezvoltă de obicei în stroma organelor parenchimatoase; este difuză. Poate apărea în interstițiul plămânilor, miocardului, ficatului, rinichilor. Rezultatul acestei inflamații este scleroza difuză. Funcția organelor în scleroza difuză se deteriorează brusc.
Inflamația granulomatoasă este o inflamație productivă focală în care apar focare în țesut din celulele care au capacitatea de a fagocitoză. Aceste leziuni se numesc granuloame. Inflamația granulomatoasă apare în reumatism, tuberculoză, boli profesionale- la depunerea pe plămâni a diferitelor substanțe minerale și alte substanțe. Imagine macroscopică: granulomul este mic, diametrul său este de 1-2 mm, este abia vizibil cu ochiul liber. Structura microscopică a granulomului depinde de faza de diferențiere a celulelor fagocitare. Precursorul fagocitelor este considerat a fi un monocit, care se diferențiază într-un macrofag, apoi într-o celulă epitelioidă și apoi într-o celulă multinucleată gigantică. Există două tipuri de celule multinucleate: celula gigantică cu corp străin și celula multinucleară gigantică Pirogov-Langhans. Granuloamele sunt împărțite în specifice și nespecifice. O variantă specifică a inflamației granulomatoase productive se numește specifică, care este cauzată de agenți patogeni specifici și care se dezvoltă pe bază imunitară. Agenții patogeni specifici sunt Mycobacterium tuberculosis, treponemul palid, ciupercile actinomicete, lepra mycobacterium, agenții cauzatori ai rinoscleromului.
Caracteristicile inflamației specifice:
1) curs cronic ondulat fără tendință de autovindecare;
2) capacitatea agenților patogeni de a provoca dezvoltarea tuturor celor 3 tipuri de inflamații, în funcție de starea de reactivitate a organismului;
3) o modificare a reacțiilor inflamatorii ale țesuturilor datorită unei modificări a reactivității imunologice a organismului;
4) din punct de vedere morfologic, inflamația se caracterizează prin formarea unor granule specifice, care au o structură caracteristică în funcție de agentul patogen.
Inflamația în tuberculoză: Mycobacterium tuberculosis este capabil să provoace inflamații alterative, exsudative, proliferative. Inflamația alternativă se dezvoltă cel mai adesea cu hipoergie, care este cauzată de o scădere a apărării organismului. Morfologic se manifestă prin necroză cazeoasă. Inflamația exudativă apare de obicei în condiții de hiperergie - sensibilitate crescută la antigene, toxine ale micobacteriilor. Mycobacterium, atunci când intră în organism, este capabil să persistă acolo mult timp, în legătură cu aceasta, se dezvoltă sensibilizarea.
Tabloul morfologic: focarele sunt localizate în diverse corpuriși țesături. Initial, in focare se acumuleaza exudatul seros, fibrinos sau mixt, ulterior focarele sufera necroza cazeoasa. Dacă boala este detectată înainte de necroza cazeoasă, atunci tratamentul poate duce la resorbția exudatului. Inflamația productivă se dezvoltă în condiții de imunitate nesterilă tuberculoasă specifică. Manifestarea morfologică va fi formarea unor granule tuberculoase specifice (sub formă de „bob de mei”). Microscopic: focarul miliar este format din celule epitelioide și celule gigantice Pirogov-Langhans. La periferia granulomului sunt de obicei numeroase limfocite. Din punct de vedere imunologic, aceste granuloame reflectă hipersensibilitate de tip întârziat. Rezultat: de obicei necroză cazeoasă. Cel mai adesea în centrul granulomului este un mic focar de necroză.
Clasificarea macroscopică a focarelor de inflamație tuberculoasă
Focurile sunt clasificate în 2 grupe: miliare și mari. Focarele miliare sunt cel mai adesea productive, dar pot fi alterative și exudative. Din focarele mari, există:
1) acinos; macroscopic, seamănă cu un trifoi, deoarece este format din trei focare miliare lipite împreună; există și productive și alternative;
2) focalizare cazeoasă - ca mărime este asemănătoare cu un dud sau cu zmeura. Culoare neagră. Inflamația este practic întotdeauna productivă, pigmenții adsorb țesutul conjunctiv;
3) lobular;
4) segmentare;
5) focare lobare.
Focarele lobare sunt focare exsudative. Rezultate - cicatrici, rareori necroză. În focarele exsudative - încapsulare, pietrificare, osificare. Pentru focarele mari, formarea unei coliziuni secundare este caracteristică, are loc lichefierea maselor dense. Masele lichide pot fi golite, cavitățile rămân în afara și în locul acestor focare - cavități.
Inflamație în sifilis. Există sifilis primar, secundar, terțiar. Sifilisul primar - inflamația este cel mai adesea exudativă, deoarece este cauzată de reacții hiperergice. Imaginea morfologică: manifestarea unui șancru dur la locul introducerii spirochetei este un ulcer cu fundul strălucitor și marginile dense. Densitatea depinde de masivitatea infiltratului celular inflamator (din macrofage, limfocite, fibroblaste). De obicei, șancrul este cicatrici. Sifilisul secundar durează de la câteva luni până la câțiva ani și este însoțit de o stare instabilă de restructurare. sistem imunitar. Există și o reacție hiperergică la bază, deci inflamația este exudativă. Caracterizat prin spirochemie. Sifilisul secundar apare cu recidive, în care se observă erupții cutanate - exantem pe piele și enantem pe membranele mucoase, care dispar fără urmă (fără cicatrici). Cu fiecare recidivă, specific reacții imune, ca urmare, numărul de erupții cutanate scade. Inflamația devine productivă în a 3-a fază a bolii - cu sifilisul terțiar. Granuloame sifilitice specifice formate - gume. Macroscopic, în centrul gumei sifilitice există un focar de necroză glutinosă, în jurul acestuia există un țesut de granulație cu cantitate mare vase și celule - macrofage, limfocite, plasmocite, de-a lungul periferiei există țesut de granulație, care trece în țesut cicatricial. Localizare peste tot - intestine, oase, etc. Rezultatul gingiei este cicatrici cu desfigurare (deformare grosolană a organului). A doua variantă a cursului inflamației productive în sifilisul terțiar este inflamația interstițială (interstitială). Cea mai frecventă localizare în ficat și în aortă este aortita sifilitică. Imagine macroscopică: intima aortică arată ca pielea de șagreu (fin îmbrăcată). Microscopic, infiltrația gingioasă difuză este vizibilă în medii și adventice, iar prin metode de colorare diferențială, distrugerea cadrului elastic al aortei. Rezultatul este o expansiune locală (anevrism aortic), care se poate rupe și se poate forma și un cheag de sânge.
Granuloamele nespecifice nu au trăsături caracteristice. Se găsesc într-o serie de boli infecțioase (cu reumatism, tifos, febră tifoidă) și bolile netransmisibile(pentru scleroza, corpuri străine). Rezultatul este dublu - cicatrici sau necroză. Cicatricea se formează mică, dar întrucât boala este cronică, ca și reumatismul, numărul de cicatrici crește cu fiecare nou atac, deci și gradul de scleroză crește. În cazuri rare, granuloamele suferă necroză, ceea ce indică o evoluție nefavorabilă a bolii.
Creșterile hipertrofice sunt polipi și condiloame. Aceste structuri se formează în timpul inflamație cronicăîn care sunt implicate ţesutul conjunctiv şi epiteliul. Polipii se dezvoltă cel mai adesea în membrana mucoasă a colonului, în stomac, în cavitatea nazală și condiloame - pe piele, lângă anusși tractul genital. Ambele seamănă cu o tumoare, dar nu le aparțin, deși este posibil să se transforme polipii și condiloamele într-o tumoare, mai întâi benignă, apoi malignă. Formațiunile hipertrofice diferă de tumori prin prezența infiltrației inflamatorii în stroma lor. Formațiunile hipertrofice sunt îndepărtate cu ajutorul operațiilor, este important să se trateze boala de bază.
| |


