07.08.2019
O metodă pentru tratamentul bolilor limfoproliferative. Tratamentul medicamentos al bolilor limfoproliferative.
limfoame maligne. procesele limfoproliferative. Limfomul lui Hodgkin.
Neoplasmele care emană din elementele ganglionului limfatic sau ale țesutului limfoid extraganglionar se numesc LIMFOAM. Limfoamele sunt clasificate ca boli ale țesutului hematopoietic - hemoblastoze, dintre care se disting leucemiile (2/3) și sarcoamele (hematosarcoame), care reprezintă 1/3. Leucemia se caracterizează printr-o leziune primară măduvă osoasă; pentru hemoblastoze, este caracteristic că și în prima etapă este caracteristică dezvoltarea creșterilor tumorale focale din elemente ale țesutului hematopoietic fără afectarea măduvei osoase (ganglionii limfatici). Există criterii comune între ele: leucemia poate fi însoțită de o leziune noduli limfatici, neuroteci, pleura și așa mai departe. Hemoblastozele pot, atunci când sunt diseminate, să capteze măduva osoasă (leucolizare) sau să se generalizeze (hematosarcomatoză). În clasificarea histologică a hematosarcoamelor, există:
A. LIMFOSARCOAME (nodular, difuz), sinonim - limfoame non-Hodgkin:
limfocitar,
limfoplasmocitar,
prolimfocitar,
limfoblastice,
imunoblastice,
Tumora (limfom) Burkitt.
B. Limfogranulomatoza (boală, limfom Hodgkin)
C. ciuperca micoză
D.RETICULOSARCOM
E. PLASMOCITOM
F. LIMFOAMELE NECLASIFICATE
G. ALTE (MASTOCITOM, GRANULOM EOSINOFIL).
Limfomul Hodgkin, Limfogranulomatoza este o tumoră malignă a ganglionilor limfatici și a sistemului limfatic cu posibilă implicare ulterioară a altor organe; Substratul patomorfologic al tumorii sunt celule mari multinucleate de Berezovsky-Sternberg, Pirogov-Reed. Boala a fost descrisă pentru prima dată în 1832 de Thomas Hodgkin, iar în 1865 s-a format această nosologie. În 1904, la Congresul al VII-lea al patologilor germani, a fost introdus termenul de LIMFOGRANULOMOZĂ, iar în 2001, în cea mai recentă recomandare a OMS, a fost propus termenul de LIMFOM Hodgkin pentru a se referi la această boală. Până în prezent, factorii etiologici nu au fost pe deplin stabiliți. Există mai multe teorii cu privire la apariția limfoamelor Hodgkin:
Infecțioasă - în familiile cu pacienți LGM, incidența este de aproape 3 ori mai mare. Este descris un caz de îmbolnăvire simultană a mai multor colegi de clasă cu limfom Hodgkin. Potrivit câțiva oameni de știință, tuberculoza, difterobacilul, ciupercile, stafilococii, coli capabile să provoace această patologie.
virale -
Imunodeficiență – scădere reactivitate imună, rezultând o tendință la infecții virale, herpes, dezvoltarea de tumori solide, un nivel ridicat de prostaglandine, monocitoză (un semn de suprimare a limfocitelor T-B).
Tumora - respectă legile progresiei tumorale, unicentricității, metastazelor, răspândirii celule atipice căile hematogene şi limfatice.
Încălcarea funcției imunității celulare este exprimată printr-o scădere a răspunsului la mitogeni în cultură și o scădere a reacției de hipersensibilitate întârziată cu administrarea intradermică de tuberculină și antigene T-dependenți. În plus, cu LGM, există o încălcare a interacțiunii limfocitelor T și B. Încălcarea funcției supresoare a limfocitelor T în manifestarea hipergammaglobulinemiei. Clinic - o tendință la infecții virale, o tendință la citopenii autoimune, o scădere a rezistenței la infecții bacteriene. Majoritatea oamenilor de știință aderă la originea unicentrică a limfomului Hodgkin.
Prevalență și epidemiologie
În Rusia, incidența limfomului Hodgkin a fost de 2,3 la 100 de mii de populație, în Statele Unite - 2,8 la 100 de mii. Bărbații se îmbolnăvesc de câteva ori mai des decât femeile. Incidența apare la orice vârstă, dar curba are două vârfuri - 15-35 de ani, iar al doilea după 50. Recent, a fost pusă sub semnul întrebării prezența unui al doilea vârf. Femeile predomină în rândul pacienților tineri, iar bărbații predomină în rândul grupelor de vârstă mai înaintată. Femeile predomină în rândul pacienților tineri. Printre pacienții din grupele mai în vârstă se numără bărbați.
Factorii etiologici ai proceselor limfoproliferative.
Numeroase studii au observat o relație între infecția cu virusul Epstein-Barr și incidența limfomului. Mai mult, la pacientii infectati, riscul de a dezvolta limfom Hodgkin este de 3 ori mai mare decat la o populatie neinfectata. De asemenea Risc ridicat apariția limfomului Hodgkin la pacienții cu mononucleoză infecțioasă. Cu toate acestea, patogeneza limfomului Hodgkin rămâne neclară. În prezent, printre numeroasele teorii ale originii celulelor Berezovsky-Sternberg se distinge ipoteza oamenilor de știință germani: celulele mononucleare mari (Hodgkin) și Berezovsky-Reed-Sternberg sunt rezultatul proliferării monoclonale a celulelor B mature provenite din centrul germinativ. a foliculului ganglionilor limfatici. Aceste celule, evitând apoptoza, au câștigat posibilitatea proliferării necontrolate. În același timp, principala verigă în patogeneza acestei patologii este blocul apoptozei. Markerii imunologici cu valoare diagnostică diferențială sunt antigenele CD15 și CD30, de obicei în absența CD45 și expresia rară a CD20 de către celulele Berezovsky-Reed-Sterntberg. Limfomul Hodgkin este însoțit de suprimarea imunității celulelor T. Pacienții sunt susceptibili la diferite infecții virale, în primul rând herpetice (H. Zoster). Rareori, limfomul Hodgkin este combinat cu tuberculoza.
Caracteristici patologice.
Diagnosticul limfomului Hodgkin se stabilește exclusiv histologic și este considerat de încredere numai dacă sunt găsite celule specifice binucleare sau multinucleare Berezovsky-Reed-Sternberg. Un examen citologic este obligatoriu în prima etapă a diagnosticului pentru a elabora un plan de examinare. Cu toate acestea, această metodă nu este întotdeauna posibilă pentru a stabili o variantă a limfomului Hodgkin și a face un diagnostic diferențial cu diferite tipuri de limfoame non-Hodgkin mari. Pentru un examen histologic adecvat, ganglionul trebuie îndepărtat în întregime, deoarece un diagnostic complet este posibil doar la examinarea structurii întregului ganglion. Acest lucru se datorează faptului că situațiile nu sunt neobișnuite când doar o parte a ganglionului limfatic îndepărtat este afectată de tumoră. În situații complexe de diagnostic diferențial, este necesar să se efectueze un studiu imunomorfologic al țesutului tumoral.
Conform clasificării morfologice internaționale moderne, se disting 4 variante histologice ale limfomului Hodgkin clasic:
1) cu scleroză nodulară (nodulară).
2) celulă mixtă;
3) limfom Hodgkin clasic bogat în limfocite (limfom Hodgkin clasic bogat în limfocite);
4) cu epuizare (sau suprimare) limfoidă de tipul fibrozei difuze sau așa-numitul tip reticular.
Limfohistiocitară. Proliferarea limfoidă severă a histiocitelor. Acumulare difuz-focală și neuniformă de eozinofile și celule plasmatice. Există puține celule caracteristice ale lui Berezovsky - Reed - Sternberg. Nu există focare de necroză.
Varianta mixta. Compoziția celulară pestriță a ganglionului limfatic cu un număr mare de celule Berezovsky - Reed - Sternberg cu focare de necroză. Mai des, întregul nod este afectat, dar este posibilă o leziune focală a nodului.
scleroza nodulara. Dezvoltarea straturilor fibroase grosiere de țesut conjunctiv care împart ganglionul limfatic în noduri separate, în care celulele tipice Berezovsky-Reed-Sternberg, focare de necroză pe fundalul acumulării de neutrofile și histiocite.
Depleția limfoidă. Dezvoltarea haotică a țesutului conjunctiv, o scădere semnificativă a numărului de celule, proliferarea histiocitelor atipice și a celulelor Berezovsky-Reed-Sternberg.
Particularitatea limfomului Hodgkin clasic este determinată de substratul său morfologic: prezența unui granulom polimorfocelular format din limfocite, neutrofile, eozinofile, histiocite, plasmocite, printre care celule Hodgkin mari unice-nucleare și gigantice bi-sau multinucleare Berezovsky-Reed- Celulele Sternberg sunt rareori localizate. În diferite grade, fenomenele de fibroză pot fi exprimate, există focare de necroză. Modelul normal al structurii în ganglionul limfatic afectat este șters treptat. Dintre varietatea elementelor de granulom, doar celulele Hodgkin și Berezovsky-Reed-Sternberg sunt celule tumorale (aneuploidia și clonalitatea lor au fost dovedite). Toate celelalte elemente celulare - limfocite, histiocite, plasmocite, eozinofile etc. - constituie o componentă reactivă și nu sunt tumorale; se crede că acestea reflectă reacția țesutului limfoid la proliferarea celulelor Berezovsky-Reed-Sternberg.
Varianta cu scleroza nodulara este mai frecventa la pacientii tineri, printre care predomina femeile. În această variantă sunt mai multe stadii incipiente cu afectarea ganglionilor doar deasupra diafragmei. Particularitatea arhitectonică a țesutului tumoral se datorează prezenței firelor de colagen care împart nodul în zone rotunjite - noduli.
Varianta celulară mixtă apare predominant la pacienții din grupa de vârstă mai înaintată. Această variantă are o imagine morfologică clasică, când modelul structurii ganglionului limfatic este șters, iar celulele Hodgkin și celulele tumorale Berezovsky-Reed-Sternberg sunt rar împrăștiate printre limfocite, eozinofile, histiocite etc.
Limfomul Hodgkin clasic bogat în limfocite este rar. Examenul histologic al ganglionului limfatic arată că printre celulele reactive predomină limfocitele mici, în timp ce celulele Hodgkin și Berezovsky-Reed-Sternberg sunt puține. Această variantă a limfomului Hodgkin are evoluția cea mai favorabilă - rata de supraviețuire la 15 ani a pacienților ajunge la 90%.
Varianta depletiei limfoide este foarte rara. Dintre fibroza difuză se găsesc mici acumulări de diferite elemente celulare, predomină celulele tumorale Berezovsky-Reed-Sternberg. Varianta se caracterizează printr-un prognostic prost.
Cel mai adesea și aproximativ în proporții egale, există variante cu scleroză nodulară și cu celule mixte (30-45% fiecare) și la fel de rare (până la 10%) - bogate în limfocite și cu depleție limfoidă.
Diagnosticul diferențial al limfomului Hodgkin se realizează cu limfoame cu celule mari, atât de natură a celulelor B cât și a celulelor T: de asemenea, cu limfadenită nespecifică. Celulele asemănătoare celulelor Hodgkin și de tip Pirogov-Langhans (elemente celulare mari, multinucleate) pot apărea în tuberculoză și actinomicoză și pot cauza dificultăți de diagnostic. Cu toate acestea, absența celulelor Berezovsky-Reed-Sternberg multinucleate permite, de regulă, un diagnostic diferențial chiar și la nivelul microscopiei cu lumină.
tablou clinic.
Există 3 forme de curgere.
Acut - caracterizat printr-un debut rapid, temperatură corporală ridicată, adinamie, transpirații abundente, afectarea ficatului, plămânilor etc.
Subacută - există o progresie necontrolată a procesului, anemie, epuizare.
Specificarea localizării primare la aceste forme este imposibilă.
Cronică - (92% din cazuri) durata medie a diagnosticului este de aproximativ 3 luni din momentul manifestărilor clinice (tuberculoză, reumatism, limfadenită, mononucleoză, infecții, sifilis).
Simptome generale – se manifestă printr-o creștere a temperaturii corpului până la subfebril, număr febril, care durează până la 2-3 zile cu bună toleranță, caracter remisiv, slăbiciune. Transpirație crescută (mai des noaptea), mâncărimi ale pielii - limitate sau generalizate. Scădere în greutate - 10% sau mai mult din greutatea corporală, dureri la nivelul articulațiilor, mușchilor, dureri de cap.
Examinarea pacienţilor cu.
Tratamentul pacientilor cu
Rezultatele tratamentului și supraviețuirea la cinci ani
Termenul „boli limfoproliferative” este folosit pentru a descrie un grup de boli maligne care provin din țesutul limfoid. Acestea includ leucemia limfocitară, limfomul Hodgkin și limfoamele non-Hodgkin.
Leucemii limfoide cronice
Leucemiile limfoide cronice includ leucemiile limfocitare cronice (celule B și celulele T), leucemia prolimfocitară și leucemia cu celule păroase. Leucemia limfocitară cronică cu celule B este cea mai frecventă.
Spre deosebire de leucemia limfoblastică acută, leucemia limfocitară cronică afectează aproape întotdeauna persoanele de vârstă mijlocie și persoanele în vârstă. Tratamentul are ca scop reducerea numărului total de limfocite și este indicat numai pacienților cu o creștere semnificativă a numărului de limfocite în măduva osoasă și cu dezvoltarea anemiei, trombocitopeniei și neutropeniei, sau în cazul unei creșteri semnificative a limfei. ganglionii sau splina. Prognoza la terapie medicamentoasă nu se îmbunătățește, dar adecvat tratament simptomatic poate îmbunătăți calitatea vieții.
Clorambucilul este medicamentul de elecție în prima etapă a tratamentului și este utilizat fie timp îndelungat în doze mici de 2-4 mg oral o dată pe zi, fie în doze mari intermitent (20 mg/m2) 2-3 zile. Îmbunătățirea se observă la peste 50% dintre pacienți. Un mijloc alternativ este ciclofosfamida la 1-2 mg/kg pe zi.
Pacienții cu trombocitopenie autoimună sau anemie hemolitică pot fi tratați cu o cură scurtă de prednisolon (60 mg pe zi pentru stadiul inițial, reducând doza la întreținere pe măsură ce se îmbunătățește). Pacienții cu supresie medulară trebuie, de asemenea, tratați cu prednison înainte de a începe tratamentul cu clorambucil.
Radioterapia este utilizată cu o creștere semnificativă a masei ganglionilor limfatici, iar cu splenomegalie se recurge la splenectomie.
limfomul lui Hodgkin
Tactica de gestionare a unui pacient cu limfom Hodgkin depinde de stadiul bolii (Tabelul 1). Baza împărțirii tumorii în stadii este un prognostic bun în stadiile I și 2A cu radioterapie, iar în stadiile ΙΠΒ și IV, prognosticul nu este atât de favorabil și este necesară chimioterapia.
Numai pentru tratamentul în stadiile 2B și 3A terapie cu radiatii sau radioterapie în combinație cu chimioterapia într-o secvență diferită în funcție de localizarea bolii.
Tabelul 1. Managementul unui pacient cu limfom Hodgkin pe baza etapelor evoluției bolii (modificarea sistemului Ann Arbor Rye)
| Etapă | Definiție |
|
Boala este limitată la un grup de ganglioni limfatici sau o zonă non-limfatică |
Iradierea zonei implicate |
|
Boala limitată la mai mult de un grup de ganglioni limfatici cu sau fără implicarea localizată a țesutului înconjurător pe o parte a diafragmei |
Iradierea zonei implicate |
|
Implicarea ganglionilor și/sau a splinei de ambele părți ale diafragmei cu sau fără implicarea localizată a țesutului înconjurător |
vezi textul |
|
Boala diseminata |
Chimioterapia |
Etapele sunt împărțite în tipurile A (asimptomatice) și B (simptomatice, adică scădere în greutate, febră, transpirații nocturne).
Au fost dezvoltate mai multe terapii medicamentoase pentru limfomul Hogkin. Așa-numita metodă „MORR” asigură remisiunea la aproximativ 60-80% dintre pacienți după 3-6 cure.
Nu există dovezi că terapia de întreținere îmbunătățește prognosticul. Rata de supraviețuire timp de 5 ani este de 50-70%. În stadiul IV al bolii, metodele alternative la „MOPP”, folosind ABVD (adriamicină, bleomicina, vinblastină și dacarbazină) în stadiul inițial de utilizare pot asigura remisiunea la 90% dintre pacienți.
Limfomul non-Hodgkin
Spre deosebire de limfomul Hodgkin, prognosticul pentru această boală este mai puțin favorabil. Deși clasificarea bolii poate fi efectuată prin analogie cu limfomul Hodgkin, nu există o strategie terapeutică clară. Acest lucru se datorează parțial faptului că majoritatea pacienților merg la medic deja în stadiul III sau IV al bolii. Clasificarea histologică devine un ghid pentru alegerea unei strategii de tratament. În funcție de tipul, mărimea și distribuția celulelor, se disting limfoame de grad scăzut, mediu și înalt.
Limfoamele non-Hodgkin de grad scăzut au un prognostic bun, dar nu sunt vindecabile, deși ocazional, când sunt diagnosticate în stadiul I, pacienții pot fi tratați cu radioterapie. În alte etape, tratamentul nu este necesar dacă nu există simptome severe sau o creștere a masei tumorale atunci când clorambucilul 10 mg/zi pe cale orală este utilizat timp de 2 săptămâni cu cure repetate până la efectul terapeutic. Frecvența remisiunii este mai mare de 60%.
Limfoamele de grad înalt sunt în majoritatea cazurilor diseminate deja în momentul diagnosticării. Tratamentul este cu o combinație medicamente. Eficiența este de aproximativ 60-70%. Un exemplu tipic chimioterapia combinată este o combinație de „CHOP”, care este utilizată în cicluri cu repetare la fiecare 3 săptămâni, în total 6 cursuri:
C - ciclofosfamidă 750 mg/m 2 intravenos în prima zi;
D - hidroxidaunomicina (doxorubicină) 50 mg/m 2 intravenos în prima zi;
O - onkovin (vincristină) 1,4 mg/m 2 intravenos în prima zi;
P - prednisolon 25 mg de 4 ori pe zi pe cale orală de la a 1-a până la a 5-a zi.
Tratamentul pentru limfomul limfoblastic poate fi similar cu cel pentru leucemia limfoblastică.
În corpul uman nu există doar vase de sânge, ci și așa-numitele vase „albe”. Erau cunoscuți de multă vreme, iar la mijlocul secolului al XVIII-lea cunoștințele despre sistemul limfatic au devenit mai extinse. Din păcate, bolile limfoproliferative nu sunt neobișnuite și pot apărea în orice organ.
sistem limfatic
Joacă un rol destul de important în funcționarea unei persoane: datorită sistemului limfatic, nutrienții sunt transportați, excesul de lichid interstițial este îndepărtat. O altă abilitate importantă este de a oferi imunitate. Lichidul care îndeplinește aceste sarcini se numește limfa. Are o culoare transparentă, compoziția este dominată de limfocite. Cea mai mică unitate structurală a sistemului sunt capilarele. Acestea trec în vase, care sunt atât intraorganice, cât și extraorganice. Structura lor include și supape care împiedică curgerea inversă a fluidului. Cele mai mari se numesc colecționari. În ele se acumulează lichidul din organe interne si altele mari O alta componenta pe care o are sistemul limfatic (fotografia este situata mai jos) sunt ganglionii. Acestea sunt formațiuni rotunde care au diametre diferite (de la jumătate de milimetru până la 5 centimetri). Ele sunt situate în grupuri de-a lungul traseului vaselor. Funcția principală este filtrarea limfatică. Aici este curățat de microorganismele dăunătoare.
Organe limfatice
Următoarele organe fac, de asemenea, parte din sistemul limfatic uman: amigdalele, splina, măduva osoasă. Limfocitele care se formează în timus se numesc celule T. Caracteristica lor este circulația continuă între limfă și sânge. Particulele care se formează în măduva osoasă se numesc celule B. Ambele tipuri după maturare sunt răspândite în tot corpul. Celulele B rămân în organele limfoide. Acest lucru le oprește migrația. LA cavitate abdominală găzduiește un alt organ mare, care este parte integrantă a sistemului limfatic, este splina. Este format din două părți, una dintre ele (pulpa albă) generează anticorpi. 
Acest grup de boli se bazează pe creșterea limfocitelor. Dacă apar modificări în măduva osoasă, atunci se folosește termenul „leucemie”. Tumorile sistemului limfatic care apar în țesutul din afara măduvei osoase se numesc limfoame. Conform statisticilor, cel mai adesea astfel de boli apar la pacienții mai în vârstă. La bărbați, acest diagnostic apare în Mai mult decât la femei. Această boală este caracterizată printr-un focar de celule, care în cele din urmă începe să crească. Alocați grad scăzut, mediu și înalt, care caracterizează malignitatea procesului.
Cauze posibile
Printre cauzele care pot provoca boli limfoproliferative, se numără un anumit grup de virusuri. Factorul eredității joacă, de asemenea, un rol important. Bolile de piele care durează mult timp (de exemplu, psoriazisul) pot declanșa creșterea neoplasmelor maligne. Și, desigur, radiațiile afectează în mod semnificativ acest proces. Radiațiile, unii alergeni, substanțele toxice activează procesul de creștere a celulelor.
limfoame. Diagnosticare
Un tip de neoplasm malign al sistemului limfatic este limfomul. Simptomele din stadiile inițiale pot să nu fie foarte pronunțate. 
Există o creștere care nu este dureroasă. Un alt semn izbitor este oboseala, și într-o măsură destul de mare. Pacientul se poate plânge transpirație excesivă noaptea, o pierdere semnificativă și bruscă a greutății corporale. Este posibilă și mâncărimea.Temperatura corpului crește uneori, mai ales seara. Aceste simptome trebuie alertate dacă nu dispar după câteva săptămâni. Pentru tratament eficient Este foarte important să se determine tipul de limfom. Când diagnosticați, luați în considerare locația, aspect tumora, tipul de proteină care se află la suprafața sa. Specialistul prescrie un examen medical complet, un test de sânge pentru celulele canceroase și un diagnostic al organelor interne. Pentru mai multe informații, este necesară o biopsie. La microscop, celulele afectate au un aspect specific.
Tratamentul limfomului
Metode de tratament această boală ca urmare a. Chimioterapia sau radioterapia (folosind raze X) sunt folosite pentru a distruge neoplasmul. Se folosește o combinație de medicamente, acestea sunt distribuite în organism și pot distruge și acele celule care nu au putut fi diagnosticate. După chimioterapie, măduva osoasă este și ea afectată, așa că poate fi necesar să fie transplantată. Se efectuează atât din materialul donator, cât și direct din măduva osoasă a pacientului (este îndepărtat în prealabil înainte de începerea procedurilor). Bolile limfoproliferative sunt, de asemenea, susceptibile de terapie biologică, dar este predominant experimentală. Se bazează pe utilizarea unor substanțe care sunt sintetizate din celulele pacientului. Pentru a obține un rezultat bun, este necesar să urmați cu atenție instrucțiunile medicului curant, să luați medicamentele la timp și să acordați atenția cuvenită nutriției. 
leucemie. Tabloul clinic
Boala se caracterizează printr-o modificare a celulelor hematopoietice, în care elementele sănătoase ale măduvei osoase sunt înlocuite cu cele afectate. Nivelul limfocitelor din sânge crește semnificativ. În funcție de ce celule au renascut, boala este izolat leucemia limfocitară (modificări ale limfocitelor), leucemie mieloidă (mielocitele sunt afectate). Puteți determina tipul de boală la microscop și prin analiza proteinei. Boala limfoproliferativă (ce este, a fost descris mai sus) în acest caz are, desigur, două forme: cronică și acută. Ultima este destul de grea. În acest caz, este necesar un tratament imediat, deoarece celulele sunt imature și nu își pot îndeplini funcțiile. Forma cronică poate dura mulți ani. 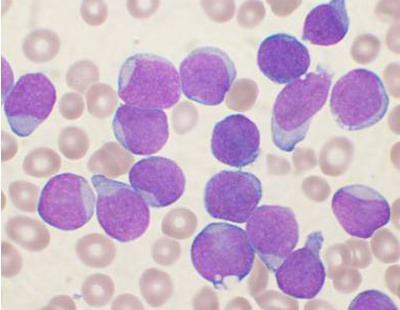
Persoanele în vârstă sunt adesea diagnosticate. Boala decurge destul de lent și numai pentru stadii târzii se observă tulburări în procesul de formare a sângelui. Simptomele includ umflarea ganglionilor limfatici și a splinei, frecvente boli infecțioase, pierdere în greutate, transpirație. Adesea astfel de boli limfoproliferative sunt descoperite întâmplător.
 Există trei etape ale bolii: A, B, C. Primul afectează 1-2 ganglioni limfatici, al doilea - 3 sau mai mulți, dar nu există anemie și trombocitopenie. La a treia se observă aceste stări. Pe primele etape experții nu recomandă terapia, deoarece o persoană își păstrează stilul obișnuit de viață. În același timp, este important să se respecte regimul zilnic, medicul poate da sfaturi cu privire la nutriție. Se efectuează terapie restaurativă. Tratament leucemie limfocitară cronică ar trebui început atunci când există semne de progresie. Include chimioterapie, radioterapie.Odată cu creșterea rapidă a organului, poate fi necesară îndepărtarea splinei.
Există trei etape ale bolii: A, B, C. Primul afectează 1-2 ganglioni limfatici, al doilea - 3 sau mai mulți, dar nu există anemie și trombocitopenie. La a treia se observă aceste stări. Pe primele etape experții nu recomandă terapia, deoarece o persoană își păstrează stilul obișnuit de viață. În același timp, este important să se respecte regimul zilnic, medicul poate da sfaturi cu privire la nutriție. Se efectuează terapie restaurativă. Tratament leucemie limfocitară cronică ar trebui început atunci când există semne de progresie. Include chimioterapie, radioterapie.Odată cu creșterea rapidă a organului, poate fi necesară îndepărtarea splinei.
Limfoamele cutanate sunt un grup eterogen de boli clinic și morfologic, la bază proces patologicîn care apare în principal în piele proliferarea malignă a limfocitelor.
Eterogenitatea limfoamelor maligne a fost stabilită în funcție de tipul de limfocit proliferativ, de apartenența acestuia la o anumită populație și subpopulație.
Distribuția limfocitelor în piele în funcție de fenotip la pacienții cu limfoame este aceeași ca și la persoanele sănătoase: limfocitele T sunt localizate în principal în epidermă și straturile superioare ale dermului, iar limfocitele B în straturile mijlocii și profunde ale dermului. . În consecință, tumorile cu celule T ocupă în principal straturile superioare ale dermei, în timp ce procesele limfoproliferative B apar în straturile profunde ale dermei și nu sunt de natură epidermotropă. Numărul de limfoame cu celule T cutanate (TKL) depășește semnificativ numărul de limfoame cu celule B (BCL); Limfoamele T reprezintă 65% din toate limfoamele cutanate maligne, limfoamele B pentru 25% și limfoamele neclasificate pentru 10%.
Cel mai adesea, TCL se înregistrează la vârstnici, deși există cazuri izolate de boală chiar și la copii. Barbatii se imbolnavesc de 2 ori mai des decat femeile.
Etiologie și patogeneză. Etiologia bolii nu a fost elucidată. La fel de factor etiologic dezvoltarea TKL a pielii, retrovirusuri precum virusul limfotrop uman de tip I (HTVL-I) sunt în prezent luate în considerare, ceea ce cauzează leucemie cu celule T la adulți. Dezvoltarea celei mai frecvente forme de TKL, micoza fungoide, este asociată cu retrovirusul C, care se găsește la pacienții la nivelul pielii, sânge periferic, celulele Langerhans. Anticorpii împotriva HTVL-I sunt detectați la mulți pacienți cu micoză fungoide.
Rolul factorilor ereditari este posibil. De exemplu, antigenele de histocompatibilitate B-5 și B-35 se găsesc adesea la pacienții cu limfoame cutanate foarte maligne, A-10 în limfoamele mai puțin agresive și B-8 predominant la pacienții cu micoză fungoidă eritrodermică.
dermatoze cronice pe termen lung, cum ar fi neurodermatita, Dermatita atopica, psoriazisul etc., contribuie la persistența pe termen lung a limfocitelor în infiltratele inflamatorii, care, pe fondul influenței factorilor de promovare în condiții de supraveghere imunitară afectată, pot contribui la apariția unei clone de limfocite maligne și, astfel, dezvoltarea unui proces proliferativ malign.
Radiațiile ionizante, radiațiile UV, diverși compuși chimici cu proprietăți cancerigene și unii alergeni joacă un anumit rol în geneza limfoamelor. Acești factori pot duce la apariția unei clone de limfocite „genotraumatice” datorită activării proto-oncogenelor sau inactivării genei supresoare tumorale și, astfel, inițiază procesul de malignizare a limfocitelor.
Reacțiile imunopatologice în TKL liber sunt efectuate în piele de limfocite și celule ale micromediului: keratinocite și celule Langerhans. Celulele limfocitelor au capacitatea de a recircula continuu în piele. Funcția principală a acestor celule este eliminarea materialului antigenic. Nivelul de recirculare a limfocitelor în timpul stimulării antigenice cronice crește de 10 ori sau mai mult, ceea ce duce la un aflux crescut de limfocite în piele. Pe de o parte, acest proces este util, deoarece limfocitele sunt implicate în reacții protectie imunitara, dar pe de altă parte, crește riscul apariției unei clone mutante de limfocite.
În TCL cutanat, există o proliferare predominantă a limfocitelor T-helper, care au caracteristici funcționale și membranare similare cu limfocitele T-helper sănătoase.
Asta permite perioadă lungă de timp își îndeplinesc funcțiile imunologice. În plus, membranele acestor limfocite exprimă antigenul limfocitar asociat pielii, care contribuie la afinitatea pe termen lung a celulelor T-helper pentru piele. Cu toate acestea, odată cu creșterea masei clonei tumorale, proprietățile funcționale ale limfocitelor se pierd, în special, antigenul funcțional limfocitar (LFA-1). În același timp, antigenul nuclear al celulelor în proliferare (Ki-67, un marker al malignității limfocitelor) apare pe membranele celulare ale limfocitelor, iar genele supresoare tumorale (P-53) sunt inactivate. Acești factori indică o scădere a supravegherii antitumorale, pierderea afinității și duc la extinderea celulelor tumorale în straturile profunde ale dermei și adesea în organele interne. În prezent, a fost identificat un rol special în transformarea tumorii și proliferarea limfocitelor T (celule ale micromediului). celulele Langerhans și keratinocite. Primele sunt o componentă importantă a sistemului macrofagic al pielii, care, la rândul său, face parte din sistemul de supraveghere imunitară. Funcția principală a acestor celule este de a prezenta informații antigenice limfocitelor T. În plus, celulele Langerhans sunt capabile să influențeze diferențierea și proliferarea limfocitelor T, să stimuleze generarea de limfocite citotoxice. Aceste funcții ale celulelor Langerhans sunt îndeplinite datorită sintezei de citokine, în primul rând interleukina-6. Cu stimularea antigenică prelungită, posibil virală, are loc o scădere a numărului de celule Langerhans și o scădere a utilității lor funcționale, ceea ce perturbă supravegherea imună și, astfel, duce la supraviețuirea și extinderea clonei maligne a limfocitelor T. Se știe că keratinocitele sporesc mult activitatea celulelor Langerhans prin „prezentarea” antigenelor limfocitelor T. În plus, sunt capabili să sintetizeze citokine, dintre care interleukina 1 (IL-1) este cea mai semnificativă funcțional. S-a stabilit că IL-1 este identică cu factorul de activare a timocitelor epidermice (ETAF) și este capabilă să activeze limfocitele T. Odată cu producția crescută a acestei citokine la pacienții cu TCL, afluxul de limfocite către leziuni este asociat cu exocitoza ulterioară în epidermă până la formarea de microabcese Potrier în ea, precum și proliferarea limfocitelor în derm. Limfocitele stimulate cu IL-1 sintetizează o altă citokină, IL-2 (factor de creștere a celulelor T), care este de o importanță cheie în patogeneza TCL cutanată. Producția crescută de IL-2 la pacienții cu TKL este, de asemenea, asociată cu înfrângerea presupusului virus limfotrop al subpopulației de limfocite T-helper, ceea ce îi face capabili de creștere „nemuritoare”.
Astfel, procesul de formare a TCL al pielii începe cu activarea limfocitelor sub influența diverșilor factori cancerigeni și apariția unei clone de celule T dominante. Când apare în piele, capacitatea sa de a efectua controlul antitumoral variază într-o mare măsură, determinând dinamica procesului la pacienții cu TCL - de la focare cu plăci petetice până la dezvoltarea de tumori mari și moarte.
Clasificare. Cea mai comună în Europa este clasificarea Kiel modificată, care ține cont de parametrii histologici și citologici ai limfoamelor. În funcție de dinamica dezvoltării TCL cutanate, de gradul de diferențiere a celulelor tumorale și de micromediu, acestea sunt împărțite în tumori de grad scăzut (I), mediu (II) și înalt (III) de malignitate.
Pentru diagnosticul TCL cutanat, este necesar să se evalueze tipul de erupții cutanate (pete, plăci, tumori), rata de apariție a acestora, datele histologice, citologice, radiologice și tomografice, rezultatele parametrilor sanguini clinici și biochimici, starea acestora. a ganglionilor limfatici. Studiile măduvei osoase sunt justificate doar în cazurile în care celulele tumorale se găsesc în ganglionii limfatici și/sau în sânge.
LIMFOAMELE T-CELULE
tablou clinic. TK-PC se caracterizează prin polimorfismul erupțiilor cutanate sub formă de pete, plăci, tumori. Cea mai comună formă de TCL a pielii este micoza fungoide, în timpul căreia există trei forme: clasică, eritrodermică și decapitată. Fiecare dintre aceste forme are un grad diferit de malignitate, de exemplu; clasic se caracterizează prin scăzut sau grad mediu malignitate (TKL I-II), și decapitat - mare (TKL-III).
Forma clasică de micoză fungoideîn aval se împarte în trei stadii: eritematos-squamos, infiltrativ-placă și tumorală. Clinic, prima etapă seamănă cu eczema, dermatita seboreică, parapsoriazisul în plăci. Erupțiile pot exista ani de zile și pot dispărea spontan. Criteriile de diagnostic pentru prima etapă sunt mâncărimea persistentă care nu dispare în ciuda tratamentului, erupțiile cutanate neobișnuite care nu sunt caracteristice dermatozelor benigne, iar vârsta pacienților este de obicei peste 50 de ani. În a doua etapă, a plăcii infiltrative, se formează leziuni la locul erupțiilor cutanate preexistente și a pielii aparent sănătoase. Plăcile sunt bine definite, au o culoare roșu închis, cu o tentă maronie. Consistența lor seamănă cu „cartonul gros”. În această etapă, poate exista limfadenopatie. În a treia stadiu terminal dezvoltarea bolii, se observă apariția unor tumori nedureroase de consistență dens elastică de culoare galben-roșie. Aspectul unor astfel de tumori seamănă adesea cu capace de ciuperci. Tumorile pot apărea peste tot. Apariția tumorilor indică apariția metastazelor limfocitelor maligne la ganglionii limfatici și organele viscerale. Trebuie remarcat faptul că leziunile extracutanate sunt mai puțin tipice pentru micoza fungoide și pentru întregul grup de TCL cutanate, în comparație cu leziunile cutanate. limfoame cu celule B. Acestea variază de la 15 la 100%, cu o medie de 72%. Ganglionii limfatici, splina, ficatul și plămânii sunt cel mai frecvent afectați. Speranța medie de viață a pacienților cu forma clasică de micoză fungoide din momentul diagnosticării este de 7,2-8 ani.
Forma eritrodermică a micozei fungoide iar varianta sa leucemică (sindromul Sezary) se caracterizează prin dezvoltarea rapidă a eritrodermiei (1-2 luni), de obicei fără erupții prealabile, mâncărimi incontrolabile, umflături, hiperemie universală, peeling puternic lamelar. Aproape întotdeauna însoțită de hipercheratoză palmoplantară și rărirea difuză a părului piele. Toate grupurile de ganglioni limfatici sunt puternic mărite. O leucocitoză pronunțată este caracteristică - mai mult de 15.000-20.000 de celule pe 1 mm, în limfocitograme - cel puțin 10% din celulele Cesari. Aceste celule sunt T-helper maligne, ai căror nuclei au o suprafață cerebriformă pliată, cu invaginări profunde ale membranei nucleare. Rezultatul letal este observat după 2-4 ani.
Forma fără cap de micoză fungoideîncepe cu apariția bruscă a tumorilor, fără erupții prealabile. Această formă de TKLK este caracterizată un grad înalt malignitate și este privită ca o manifestare a limfosarcomului. Rezultatul letal apare în decurs de 1 an.
Din punct de vedere histologic, principalele criterii de diagnostic pentru micoza fungoide în stadiile incipiente sunt acantoza cu procese largi, hiperplazia și compactarea keratinocitelor bazale, degenerarea vacuolară a unei părți a celulelor bazale, mitozele atipice în diferite straturi ale epidermei, epidermotropismul infiltratului cu pătrunderea limfocitelor în epidermă. În derm se determină mici infiltrate în jurul vaselor. Printre celulele infiltratelor, sunt singure celule mononucleare cu nuclei hipercromici – celule „micotice”. În a doua etapă, tabloul histologic devine mai distinct.
Severitatea infiltratului dermic și epidermotropismul celulelor infiltratului cresc semnificativ, drept urmare limfocitele maligne pătrund în epidermă, formând acumulări sub formă de microabcese Potrier. În a treia etapă, acantoza poate fi fie masivă, fie, dimpotrivă, nesemnificativă din cauza atrofiei epidermei. Infiltrația epidermei de către limfocitele tumorale, care formează multiple microabcese Potrier, este în creștere. Proliferate ocupă întreaga grosime a dermului, pătrunzând în țesut adipos subcutanat, și devine mai monomorfă. Predomină formele blastice de limfocite.
Tratament. CTLC în stadiile incipiente, reprezentate de erupții cutanate și plăci, au un prognostic relativ favorabil cu o supraviețuire a pacienților peste 5 ani. În stadiul tumoral la pacienții cu sindrom Cesari, prognosticul este semnificativ mai rău, durata medie viata nu ajunge la mai mult de 3 ani.
Tratamentul TCL în stadiile incipiente fără limfadenopatie se efectuează cu corticosteroizi externi, fotochimioterapie, terapie cu fascicul de electroni, interleukine și retinoizi aromatici. Dintre medicamentele corticosteroizi în stadiile incipiente ale TCL, cel mai mare efect terapeutic au derivați de prednisolon, betametazonă, dexametazonă.
Eficienţă Metoda de terapie PUVA se bazează pe formarea selectivă a legăturilor încrucișate covalente ale psoralenilor cu ADN în celulele T-helper în proliferare, ceea ce inhibă diviziunea acestora.
Tehnici: pacienții iau 8-metoxipsoralsn pe cale orală cu o rată de 0,6 mg/ct greutate corporală cu 2 ore înainte de iradiere. În acest timp, medicamentul are timp să se acumuleze în piele cât mai mult posibil. Iradierea se efectuează în funcție de tipul de piele, începând de la 0,25-1,0 J/cm2, crescând doza la fiecare 2-3 proceduri cu 0,5 J/cm-. Se efectuează 30-35 de proceduri. În stadiul tumoral și la pacienții cu eritrodermie, eficacitatea terapiei PUVA este semnificativ redusă datorită locației profunde a proliferării. În aceste cazuri se folosesc metode combinate: PUVA + citostatic (prospidin); PUVA + interferon; PUVA + retinoizi (terapia rePUVA).
Folosit cu succes interferonii alfa, beta și gama. Aceste citokine joacă un rol central în diferențierea celulară. Atât dozele mari (50 MU/m2), cât și dozele mici (3 MU/m2) sunt utilizate de 3 ori pe săptămână. Durata remisiunii cu monoterapia cu interferoni variază de la 5 la 10 luni. În prezent, clinica folosește în principal alfa-interferoni recombinanți: roferon, reaferon (alfa-2a-interferon) și intron-A (alfa-2p-interferon). Combinația de interferoni cu alte metode de terapie are o mai pronunțată efect de vindecare(interferoni + PUVA, interferoni + citostatice, interferoni + retinoizi aromatici).
Terapia cu fascicul de electroni (CRT) se efectuează la pacienții cu TCL în 2 versiuni: local sau total.
Această tehnică este utilizată în principal în progresia limfomului folosind un betatron sau un accelerator liniar cu o putere de 6-10 Mev. Iradierea pacienților se efectuează de 1-4 ori pe săptămână și o doză de 1-6 grn. Doza de curs este de 30-40 Gy. Avantajul CRT față de PCT constă în efectul asupra proliferării tumorii pe toată adâncimea pielii și a unei părți a țesutului adipos subcutanat (la o distanță de până la 10-20 mm), ceea ce nu poate fi realizat prin alte metode.
Efectele secundare ale radioterapiei includ dermatita, atrofia pielii, alopecia și pielea uscată.
Fotofereza (fotochimioterapia extracorporală) – metoda noua terapia TCL cutanată, care constă în aportul oral psoralen (8-metoxipsoralen) cu iradiere UVA extracorporală a sângelui periferic al pacientului.
Mecanismul de acțiune al fotosensibilizatorilor se explică prin formarea unui răspuns imun puternic în organismul unui pacient cu TKL la introducerea limfocitelor T deteriorate, adică se efectuează un fel de „vaccinare” a pacientului împotriva limfocitelor tumorale. . Psoralenul este cel mai tropical pentru celulele maligne. Ca urmare a reacțiilor fotochimice, are loc moartea lor, totuși, markerii celulelor tumorale sunt păstrați.
Retinoizi aromatici(acid 13-cisretinoic (izotretinoin, etretinat) capabile să inhibe proliferarea celulară, încetinind diferențierea acestora. Izotretinoina și etretinatul sunt prescrise în doze de 0,5-1 mg/kg greutate corporală timp de 2-3 luni. Combinația de retinoizi aromatici cu terapia PUVA (terapia rePUVA) are o eficacitate terapeutică mai pronunțată.
Monochimioterapia presupune utilizarea diferitelor citostatice: medicamente alchilante (ciclofosfamidă, embihină, prospidină, spirobromină etc.); vincalcaloizi (vincristină, vinblastină, etoposidă); antimetaboliți (metotrexat); antibiotice antitumorale (adriamicină, bruneomicina etc.); derivați de platină (cisplatină); corticosteroizi (prednisolon etc.).
Ciclofosfamidă utilizat pe cale orală, intramusculară sau intravenoasă, 200 mg pe zi, pentru o cură de 3-8 g; metotrexat - oral la 2,5-5 mg pe zi, intramuscular la 5-20 mg o dată pe săptămână, pentru o cură de 100-250 mg; prospidină 100-200 mg intramuscular, pe cură 3-4 g; adriamicină 30-50 mg o dată pe săptămână intravenos timp de 4 săptămâni; vincristină 1 mg intravenos o dată pe săptămână timp de 4-6 săptămâni.
Adăugarea de prednisolon în doză de 20-40 mg pe zi sporește semnificativ efectul antitumoral al monochimioterapiei. Dacă este necesar, cursurile de chimioterapie se repetă la fiecare 5-6 luni. În ciuda tratamentului cu un singur medicament, monochimioterapia poate provoca efecte secundare caracteristice citostaticelor: imunosupresia, suprimarea măduvei osoase, au efect toxic asupra diferitelor organe parenchimatoase. Prin urmare, atunci când se efectuează monochimioterapie, este necesară monitorizarea constantă a modificărilor din sânge, imunogramă și starea organelor viscerale.
Polichimioterapia indicat în stadiile târzii ale CTLC ca cel mai optim tratament pentru pacienții cu limfoame cutanate cu grad ridicat de malignitate. Administrarea simultană a medicamentelor anticancer cu diferite mecanisme de acțiune (polichimioterapia) se datorează faptului că fiecare dintre citostatice poate inhiba un anumit stadiu al sintezei ADN-ului în celula tumorală în fazele G, M– și S și, astfel, poate conduce la o suprimare mai sigură a proliferării tumorii.
În acest scop, au fost propuse numeroase regimuri polichimioterapeutice: prospidin 100 mg intramuscular, pentru o cură de 3-4 g, vincristină 1 mg intravenos o dată pe săptămână timp de 4 săptămâni și prednisolon în doză de 20-30 mg pe zi timp de 3 săptămâni. . cu o scădere treptată a dozei de 2,5 mg pe zi. Conform celei de-a doua scheme, ciclofosfamida 600 mg intramuscular 1 dată pe săptămână este utilizată în combinație cu vincristină 1 mg intravenos 1 dată pe săptămână și prednisolon 20-30 mg pe zi timp de 2-3 săptămâni, cu o reducere treptată a dozei. Cu eficacitatea primelor două cure de tratament, se repetă de 3-4 ori cu întreruperi
LIMFOAMELE B-CELULE
tablou clinic. Limfoamele cu celule B ale pielii (CLCL) sunt caracterizate prin leziuni rapid progresive ale pielii, ganglionilor limfatici și organelor interne. Celulele tumorale sunt reprezentate de limfocitele B, care pot păstra funcțiile celulelor sănătoase pentru o perioadă lungă de timp; au capacitatea de a se diferenția în plasmocite. Spre deosebire de limfocitele T, celulele B nu posedă epidermotropism și, prin urmare, se găsesc în principal în dermul reticular. După natură și severitate curs clinic Există trei tipuri de piele ON.
Mai întâi tastați ON apare la toate grupele de vârstă, dar incidența maximă apare la bătrânețe și se manifestă în principal prin placă și elemente nodulare. Acest tip de limfom se caracterizează printr-un curs relativ benign. Malignitatea se formează după 20-30 de ani de la debutul bolii. Apare la fel de des atât la bărbați, cât și la femei. La formă de placă(reticuloză primară a pielii), procesul începe cu apariția unor pete de culoare maro deschis sau galben-roz, contururi rotunjite cu un model folicular. Petele se infiltrează treptat, transformându-se în plăci cu peeling lamelar mic. Elementele pot fi localizate pe față, trunchi, membre. O astfel de infiltrare pronunțată a pielii, mai ales în zona feței, duce la formarea faciesului leonin. Infiltrarea ulterioară a plăcilor contribuie la transformarea lor în noduri emisferice dense, care se dezintegrează în curând cu formarea de ulcere profunde, care sângerează ușor. forma innodata Skin ON se caracterizează prin apariția mai multor noduli pe pielea aparent sănătoasă, fără pete sau plăci prealabile. Nodurile de consistență densă au o culoare galbenă sau maronie, o suprafață netedă, de la 2 la 5 cm în diametru. Adesea, astfel de noduri nu suferă dezintegrare, ci regresează, lăsând în urmă atrofie și hiperpigmentare. Nu există senzații subiective. Pe măsură ce procesul progresează, aceste erupții cutanate devin numeroase și cresc brusc în dimensiune.
Al doilea, tipul mai malign de piele ON decurge ca forma nodulară a reticulozei primare (stadiul II) sau reticulosarcomatoza Gottron. Infiltratul tumoral este compus din celule B cu un grad mai mic de diferențiere. Boala atinge punctul culminant după 2-5 ani de la debutul primelor manifestări. Clinic, erupțiile sunt reprezentate de mai multe noduri mari de 3-5 cm în diametru, de culoare roșu închis, de consistență dens elastică, cu peeling ușor. Pe măsură ce boala progresează, nodulii se diseminează. În paralel, se observă pătrunderea celulelor maligne în ganglionii limfatici și organele interne.
Al treilea tip este caracterizat de cea mai pronunțată malignitate a limfocitelor B. Tumoarea proliferează este compusă predominant din imunoblaste. Clinic se formează inițial un nodul profund de culoare albăstruie-violet, consistență densă, de 3-5 cm în diametru. După 3-6 luni, diseminarea procesului are loc sub forma a numeroase noduri. Limfadenopatia se unește și se observă degradarea erupțiilor tumorale. Durata bolii este de 1-2 ani.
Histologic, HCL al pielii dezvăluie infiltrate constând din limfocite B de diferite grade de malignitate. Deci, dacă în forma de placă a VCL în infiltrat, împreună cu limfocite, se găsesc multe histiocite și fibroblaste și un număr mic de limfoblaste, atunci în erupțiile nodulare de HCL, proliferarea este predominant imunoblaste.
Tratament. Terapia cu fascicul de electroni cu doze focale totale de 30-40 Gy este cea mai eficientă în formă de placă de VCL. În forma nodulară a VCL, este indicat să se utilizeze diverse regimuri polichimioterapeutice: CVP-ciclofosfamidă, vincristină și prednisolon sau CAVP-ciclofosfamidă, adriamicină, vincristină și prednisolon.
Grupul limfoproliferativ include un grup de tumori ale sistemului limfatic provenite din limfocitele B și T: leucemie limfoblastică acută, toate formele de leucemie limfocitară cronică, inclusiv leucemia cu celule păroase, care este de obicei descrisă ca o unitate nosologică independentă; procesele limfoproliferative ar trebui să includă și neoplasmele limfocitare extramedulare - limfocitoame și limfosarcoame și tumori limfocitare și plasmocitare secretoare de imunoglobuline - hemoblastoze paraproteinemice; precum și tumori limfocitare cutanate - boala Cesari, micoză fungoide și leziuni cutanate cu celule B.
Leucemie limfocitară cronică
Leucemia limfocitară cronică este tumoră benignă, substratul său sunt predominant limfocite mature morfologic. Boala se manifesta prin leucocitoza limfatica, cresterea excesiva limfocitara difuza in maduva osoasa, ganglionii limfatici mariti, splina si ficat.
Mecanismul de dezvoltare
Principal semne externe leucemia limfocitara cronica - leucocitoza limfatica si marirea ganglionilor limfatici, iar mai tarziu a splinei si ficatului - se datoreaza cresterii limfocitelor.
Deoarece diferite clone de limfocite sunt implicate în procesul tumoral în leucemia limfocitară cronică în cazuri diferite, strict vorbind, forma nosologică a „leucemiei limfocitare cronică” ar trebui să fie formată din multe boli, deși au o serie de caracteristici comune. Analiza celulară a leucemiei limfocitare cronice relevă deja o varietate de variante celulare: predominanța formelor cu plasmă îngustă sau, dimpotrivă, cu plasmă largă, celule cu nuclei mai tineri sau aproximativ picnotici, cu citoplasmă bazofilă pronunțată sau aproape incoloră.
Clonele de limfocite cu un set aberant de cromozomi au fost obținute în forme T prin acționarea asupra limfocitelor cu PHA ca mitogen. În leucemia limfocitară B, pentru a provoca diviziunea limfocitelor, a luat efectul unor mitogeni polivalenți: virusul Epstein-Barr, lipopolizaharidă din E coli. Datele cariologice dovedesc nu numai clonalitatea, ci și natura mutațională a leucemiei limfocitare cronice și apariția subclonelor pe măsură ce procesul se dezvoltă, după cum se poate aprecia din evoluția modificărilor cromozomiale în cazuri individuale.
S-a dovedit că majoritatea limfocitelor B leucemice din leucemia limfocitară cronică conțin imunoglobulină citoplasmatică monoclonală sau, mai degrabă, lanțul greu al imunoglobulinei. Monoclonalitatea imunoglobulinei citoplasmatice este mai ușor de dovedit decât superficială. Detectarea imunoglobulinei citoplasmatice în limfocitele B ale leucemiei limfocitare cronice confirmă presupunerea că aceste limfocite sunt celule ale uneia dintre etapele incipiente ale diferențierii limfocitelor B și evidențiază conținutul scăzut de imunoglobuline de pe suprafața lor.
Citopenia în leucemia limfocitară cronică poate fi natură diferită. Deși leucemia limfocitară cronică provine cel mai adesea dintr-o celulă progenitoare a limfocitelor B, poate crește nivelul de supresori T din sânge și splină. Un conținut crescut al acestor celule, care nu sunt de natură tumorală, poate duce la suprimarea proliferării celulelor - precursorii hematopoiezei, în special BFU-E, celule precursoare de granulocite-macrofage - CFU-GM și, eventual, cele comune. celula - precursorul mielopoiezei.
O alta geneza a citopeniei in leucemia limfocitara cronica este autoimuna, asociata cu formarea de anticorpi la celulele hematopoietice, la maturizarea celulelor maduvei osoase sau la maturizarea elementelor din sange si maduva osoasa. Natura autoimună a distrugerii eritrocitelor în leucemia limfocitară cronică este dovedită prin apariția unui test Coombs direct pozitiv, iar distrugerea în sine este dovedită prin reticulocitoză în sânge, continut ridicat eritrocite în măduva osoasă, durata de viață scurtă a eritrocitelor, bilirubinemie. Dacă anemia nu este însoțită de reticulocitoză, iar conținutul de eritrocariocite este crescut în măduva osoasă și există bilirubinemie indirectă, atunci se poate presupune liza intramedulară a eritrocariocitelor. Natura imună a anemiei este dovedită în aceste cazuri printr-un test de hemaglutinare agregată pozitiv.
În plus, procesul citolitic poate fi cauzat de celulele leucemice înseși, dacă au proprietăți funcționale ucigașe.
Clinica
De mulți ani, se poate observa doar limfocitoza - 40-50%, deși numărul total de leucocite fluctuează în jurul limitei superioare a normei. Ganglionii limfatici pot fi de dimensiuni normale, dar cresc odata cu diferite infectii, iar dupa eliminarea procesului inflamator se reduc la dimensiunea initiala.
Ganglionii limfatici se măresc treptat, de obicei în principal la nivelul gâtului, axile, apoi procesul se extinde la mediastin, cavitatea abdominală, poală. Există fenomene nespecifice comune tuturor leucemiilor: oboseală, slăbiciune, transpirație. În stadiile incipiente ale bolii, în cele mai multe cazuri, nu se dezvoltă anemie și trombocitopenie.
Limfocitoza din sânge crește treptat; 80-90% din limfocite, de regulă, se observă cu înlocuirea aproape completă a măduvei osoase cu limfocite. Răspândirea țesutului limfatic în măduva osoasă poate să nu inhibe producția de celule normale ani de zile. Chiar și atunci când se ajunge la un număr mare de leucocite în sânge, 100.000 în 1 µl sau mai mult, adesea nu există anemie, numărul de trombocite este normal sau ușor redus.
Studiile măduvei osoase arată o creștere a conținutului de limfocite în mielogramă - de obicei mai mult de 30%, precum și creșteri caracteristice ale celulelor limfoide, adesea difuze.
Structura limfocitelor în leucemia limfocitară cronică nu are caracteristici stabile și tipice. Se poate schimba în cursul bolii sub influența infecții virale. Spre deosebire de alte leucemii, predominanța celulelor cu același nume în sânge (în acest caz, limfocite) nu înseamnă predominanța celulelor leucemice, întrucât atât limfocitele B ale clonei leucemice, cât și un număr crescut de limfocite T policlonale sunt adesea în circulație în același timp. În sânge, majoritatea celulelor sunt limfocite mature, care nu diferă de cele normale. Alături de astfel de celule pot exista elemente limfocitare cu un nucleu mai omogen, care nu au încă cromatina grosieră buloasă a unui limfocit matur, cu o margine largă a citoplasmei, care uneori, ca în mononucleoza infectioasa, are iluminare perinucleară. Nucleii celulari pot avea o răsucire particulară a buclelor sau pot fi în mod regulat rotunji; există și nuclee în formă de fasole; citoplasma este cu contururi rupte, uneori cu elemente de „pilozitate”, dar fără caracteristicile histochimice ale leucemiei cu celule păroase.
Un semn caracteristic al leucemiei limfocitare cronice este nucleele dărăpănate ale limfocitelor - umbrele lui Humnrecht. Numărul lor nu este un indicator al severității procesului.
La începutul bolii, prolimfocitele și limfocitele in formula leucocitară de obicei nu.
Pe această bază, se distinge o formă prolimfocitară de leucemie limfocitară cronică. Uneori, o astfel de leucemie poate apărea cu secreția de imunoglobuline monoclonale.
Pe măsură ce boala progresează, în sânge încep să apară prolimfocite și limfoblaste unice. Numărul lor mare apare doar în stadiul terminal al bolii.
Stadiile leucemiei limfocitare cronice. În etapa inițială a procesului, există o ușoară creștere a mai multor ganglioni limfatici din unul sau două grupuri, leucocitoza nu depășește 30 × 10 3 - 50 × 10 3 în 1 μl și, cel mai important, nu există tendința de a crestere vizibila de-a lungul lunilor. În această etapă, pacienții rămân sub observație și nu se efectuează citostatice. Stadiul avansat se caracterizează prin creșterea leucocitozei, mărirea progresivă sau generalizată a ganglionilor limfatici, apariția infecțiilor recurente și citopenii autoimune. Această etapă necesită terapie activă. Stadiul terminal include cazuri de transformare malignă a leucemiei limfocitare cronice.
Diagnosticul leucemiei limfocitare cronice nu este dificil. Criteriile sunt următoarele: limfocitoză absolută în sânge, mai mult de 30% din limfocitele din măduva osoasă punctează cu hiperplazie limfatică difuză în trepanatul măduvei osoase. Mărirea ganglionilor limfatici și a splinei este un semn opțional al leucemiei limfocitare cronice, dar atunci când este implicat în proces, se observă proliferarea difuză a limfocitelor în aceste organe. Un semn de diagnostic auxiliar al proliferării tumorii limfatice sunt umbrele lui Gumprecht într-un frotiu de sânge.
Leucemia limfocitară cronică trebuie diferențiată de un alt proces tumoral limfocitar cu celule mature - limfocitomul. Se distinge de limfocitom prin localizarea predominantă a proliferării limfatice în măduva osoasă, natura sa difuză în acest organ, precum și în altele implicate în proces, confirmată de examenul histologic.
Complicații
Toate sau unele dintre cele 3 imunoglobuline testate în mod obișnuit (A, G și M) pot fi reduse. În procesele de secreție limfoproliferative, împreună cu creșterea imunoglobulinei monoclonale, nivelul imunoglobulinelor normale scade de obicei. În situații de diagnostic îndoielnic, cu limfocitoză scăzută, o scădere a nivelului imunoglobulinelor normale poate servi drept argument în favoarea procesului limfoproliferativ. Cu toate acestea, o imagine tipică este posibilă pentru nivel normalγ-globuline și imunoglobuline în serul sanguin. Hipogammaglobulinemia nu este asociată cu durata bolii și severitatea limfocitozei. Se poate datora unei încălcări a interacțiunii dintre limfocitele T și B, un conținut crescut de supresori T, incapacitatea limfocitelor B leucemice de a răspunde la limfokinele produse de limfocitele T normale.
Hipersensibilitatea la infecții la pacienții cu leucemie limfocitară cronică este una dintre cele factori critici ducând la moarte. Motivele acestei susceptibilitati nu sunt pe deplin clare si, aparent, sunt mai multe dintre ele. Potrivit lui E. G. Bragina, tendința la complicații infecțioase nu este întotdeauna paralelă cu hipogamaglobulinemia, poate fi și cu un nivel normal de γ-globuline în ser. Complicațiile infecțioase frecvente nu sunt întotdeauna paralele cu creșterea leucocitozei.
Frecvența pneumoniei, în special în leucemia limfocitară cronică, este promovată de infiltrarea limfatică în sine. țesut pulmonar, o creștere a foliculilor limfatici ai arborelui bronșic, ducând la prăbușirea întregului sau a unei părți a plămânului, afectarea ventilației plămânilor și a funcției de drenare a bronhiilor. De obicei, aceste fenomene cresc odată cu evoluția bolii. Complicațiile frecvente sunt procese inflamatoriiîn fibre cauzate de stafilococ sau bacterii gram-negative.
În același timp, susceptibilitatea crescută la infecție, care este definită de termenul „infecțiozitate”, în stadiul inițial al procesului, aparent, este asociată cu defecte ale răspunsului imun, tulburări în interacțiunea limfocitelor T și B. . Cursuri insuficiente de terapie cu antibiotice pot contribui la recurența și cursul prelungit al infecțiilor. În spitalele specializate și în care se acumulează pacienți cu imunosupresie severă și apar noi tulpini patogene de agenți patogeni, de multe ori izbucnesc „epidemii” deosebite.
Mai des, pacienții suferă de herpes zoster ( herpes zoster). Poate fi atât tipic, cât și generalizat, determinând o leziune completă a pielii, în timp ce erupția segmentară locală a veziculelor devine rapid confluentă. Erupțiile herpetice pot capta și mucoasele tractului digestiv, bronhiile. Are loc aceeași pierdere herpes simplex (herpes simplex), varicelă.
La pacienții cu leucemie limfocitară cronică, există adesea o infiltrație pronunțată la locul mușcăturilor de țânțar; cu mușcături multiple, este posibilă o intoxicație severă.
Complicațiile imunocomplexe ale leucemiei limfocitare cronice și ale altor boli limfoproliferative sunt rare. Ele pot fi exprimate prin sindromul Shenlein-Genoch, polinevrita.
În leucemia limfocitară cronică, există adesea infiltrarea perechii VIII de nervi cranieni cu pierdere a auzului, senzație de „congestie” și tinitus. Ca și în cazul altor leucemii, se poate dezvolta neuroleucemie; de regulă, aceasta este o exacerbare terminală, când meningele sunt infiltrate cu celule limfoide tinere. Tabloul clinic al neuroleucemiei nu diferă de cel din leucemie acută; în meninge, procesul ar putea fi eliminat prin administrarea intralombară de citosar cu metotrexat. Concomitent cu infiltrarea meningelor, poate apărea și infiltrarea substanței cerebrale, pentru tratamentul căreia este necesară iradierea. Sindromul radicular, cauzat de infiltrarea limfatică a rădăcinilor, apare de obicei în stadiul terminal al bolii.
Una dintre manifestările severe ale leucemiei limfocitare cronice - pleurezie exudativă. Natura sa poate fi diferită: pleurezie para- sau metapneumonică cu o infecție banală, pleurezie tuberculoasă, infiltrație limfatică a pleurei, compresie sau ruptură a ductului limfatic toracic. Cu pleurezia de origine infecțioasă în exudat, împreună cu limfocite, există multe neutrofile. Odată cu infiltrarea pleurei, compresia și ruptura ductului limfatic, exudatul va fi limfatic, dar dacă lichidul provine din duct, acesta va conține o cantitate mare de grăsime (lichid chilos).
Tratamentul activ trebuie să fie în timp util, deoarece îndepărtarea forțată repetată a exsudat pleural duce rapid la epuizare, edem hipoalbuminemic. Când ductul toracic este rupt, este indicată restaurarea chirurgicală a integrității acestuia.
Pacienții mor în principal din cauza gravă complicatii infectioase, epuizare crescândă, sângerări, anemie, creștere sarcomică.
De regulă, în leucemia limfocitară cronică, nu există o schimbare calitativă a comportamentului celulelor tumorale pentru o lungă perioadă de timp. Semne de progresie cu ieșire celule patologice scăpa de sub control al medicamentelor citostatice poate să nu fie pe tot parcursul bolii.
Dacă procesul trece totuși în stadiul terminal, atunci are aceleași semne ca și în alte leucemii (inhibarea germenilor hematopoietici normali, înlocuirea totală a măduvei osoase cu celule blastice).
Trecerea leucemiei limfocitare cronice la stadiul terminal este mai des însoțită de creșterea sarcomului în ganglionul limfatic decât de o criză blastică. Astfel de ganglioni limfatici încep să crească rapid, capătă o densitate pietroasă, se infiltrează și comprimă țesuturile învecinate, provocând umflături și dureri, care nu sunt caracteristice stadiului avansat al leucemiei limfocitare cronice. Adesea, creșterea sarcomului în ganglionii limfatici este însoțită de o creștere a temperaturii. Uneori, aceste noduri sunt situate în țesut subcutanat fata, trunchiul, membrele, sub mucoasa din cavitatea bucala, nasul si vasele care cresc in ele le dau aspectul unei hemoragii; numai densitatea și bombarea unei astfel de „hemoragii” indică natura acesteia.
În stadiul terminal, al cărui început este uneori imposibil de stabilit, este foarte greu de descifrat creșterea bruscă a temperaturii. Poate fi din cauza transformării sarcomului a procesului; atunci trebuie aplicată o terapie citostatică suficient de puternică. Cu aceeași probabilitate, cu leucemia limfocitară cronică prelungită, este posibilă o infecție, în primul rând tuberculoasă (infiltrarea tuberculoasă a plămânilor cu granulocitopenie nu este întotdeauna detectată). În aceste situații, determinarea cauzei creșterii temperaturii durează mult timp și necesită utilizarea consecventă a medicamentelor bacteriostatice.
Una dintre manifestările stadiului terminal al bolii poate fi insuficiența renală severă din cauza infiltrației parenchimului organului de către celulele tumorale. Oprirea bruscă a urinării ar trebui să conducă întotdeauna medicul la o astfel de presupunere. Dacă sunt excluse toate celelalte cauze de afectare a rinichilor, atunci trebuie efectuată iradierea rinichilor, care elimină rapid urinarea perturbată.
Prognoza
Recuperarea după leucemia limfocitară nu a fost observată până de curând. În unele cazuri, complexul a permis obținerea de îmbunătățiri pe termen lung. Speranța de viață a pacienților variază într-un interval foarte larg - de la câteva luni până la 2-3 decenii.
Forme de leucemie limfocitară cronică
Clasificarea leucemiei limfocitare cronice se bazează pe morfologice și semne clinice inclusiv răspunsul la tratament.
Există următoarele forme:
1) benign;
2) progresiv (clasic);
3) tumoră;
4) splenomegalică (splină mărită);
5) măduvă osoasă;
6) leucemie limfocitară cronică complicată de citoliză;
7) prolimfocitar;
8) leucemie limfocitară cronică, care apare cu paraproteinemie;
9) leucemie cu celule păroase;
10) Celulă T.
Forma benignă de leucemie limfocitară cronică determină o creștere foarte lentă, sesizabilă doar pe parcursul anilor, dar nu lunilor, o creștere a limfocitozei în sânge în paralel cu o creștere a numărului de leucocite. În primele etape, ganglionii fie nu sunt măriți, fie cei cervicali sunt foarte puțin măriți. Cu o infecție, există o limfocitoză mare de 2-3 × 10 4 (20-30 mii) în 1 μl, care dispare împreună cu o complicație infecțioasă. O creștere foarte lentă a limfocitozei până la o creștere vizibilă a ganglionilor limfatici poate dura ani sau decenii. În tot acest timp, pacienții sunt sub observație la dispensar, sunt pe deplin capabili să lucreze, li se interzice doar creșterea insolației. Analizele de sânge cu numărătoarea trombocitelor și reticulocitelor se fac o dată la 1-3 luni. Cu forma descrisă, până în momentul în care deteriorarea stării poate necesita tratament, în multe cazuri nu fac o puncție sternală diagnostică, un examen histologic al ganglionului limfatic. Aceste studii rănesc semnificativ psihicul pacientului, care adesea nu are nevoie de medicamente citostatice până la sfârșitul zilelor sale.
Forma progresivă (clasică) de leucemie limfocitară cronicăîncepe la fel ca benign, dar numărul de leucocite crește de la lună la lună, la fel ca și dimensiunea ganglionilor limfatici. Consistența nodurilor poate fi aluoasă, moale sau ușor elastică.
Terapia citostatică pentru acești pacienți este de obicei prescrisă cu o creștere vizibilă a tuturor manifestărilor bolii, leucocitoză și dimensiunea ganglionilor limfatici în primul rând.
Forma tumorală a leucemiei limfocitare cronice. O caracteristică a acestei forme, care i-a determinat numele, este o creștere semnificativă și consistența densă a ganglionilor limfatici cu leucocitoză scăzută. Amigdalele sunt mărite, adesea sunt aproape închise între ele. Mărirea splinei este de obicei moderată, dar uneori semnificativă, adesea iese la câțiva centimetri de sub marginea costală.
În formula leucocitelor, este reținut un procent suficient de neutrofile - 20% sau mai mult. În măduva osoasă, de obicei nu mai mult de 20-40% din limfocite, deși poate fi, de asemenea, complet deteriorat.
În ciuda hiperplaziei semnificative a țesutului limfatic, intoxicația nu este foarte pronunțată pentru o lungă perioadă de timp, spre deosebire de limfosarcomul generalizat, cu care această formă de leucemie limfocitară cronică este adesea confundată.
Forma măduvei osoase a leucemiei limfocitare cronice limfadenia osoasă. Pancitopenie cu progresie rapidă, înlocuirea totală sau parțială a măduvei osoase cu limfocite mature cu creștere difuză. Ganglionii limfatici nu sunt măriți, splina, cu excepții foarte rare, nu este nici mărită, ficatul este de dimensiuni normale. Din punct de vedere morfologic, se remarcă omogenitatea structurii cromatinei nucleare, uneori este picnotică, mai rar există elemente de structuralitate, care seamănă departe cu explozia; citoplasmă cu bazofilie pronunțată, îngustă, adesea zdrențuită. Anterior, această formă ducea rapid pacienții la moarte, speranța de viață depășea rar 2 ani (14-26 luni).
Introducerea regimului VAMP în terapia acestei forme de boală, precum și modernizarea sa în continuare, au făcut posibilă obținerea de îmbunătățiri și prelungirea semnificativă a vieții pacienților.
Leucemia limfocitară cronică, complicată de citoliză, nu este o formă independentă. Poate atât o creștere semnificativă a ganglionilor limfatici, cât și absența limfadenopatiei, leucocitoza limfatică poate fi foarte mare, sau boala decurge conform unei variante subleucemice tumorale. Distrugerea eritrocitelor se explică prin reticulocitoză, creșterea nivelului de bilirubină și a procentului de eritrocariocite în măduva osoasă, iar forma imună se explică printr-un test Coombs direct pozitiv. Dizolvarea trombocitară crescută este definită de trombocitopenie, megacariocitoză ridicată sau normală în măduva osoasă.
Este mult mai dificil să se determine dizolvarea crescută a granulocitelor, deoarece conținutul precursorilor lor în măduva osoasă nu poate fi determinat pe fondul proliferării limfatice complete. Cu un anumit grad de probabilitate, o descompunere crescută a granulocitelor poate fi judecată după dispariția lor bruscă din sângele periferic.
În unele cazuri, leucemia limfocitară cronică, care apare cu citoliză, este însoțită de o creștere semnificativă a temperaturii. Dispariția parțială a oricărui germen din măduva osoasă sugerează citoliză intramedulară.
Forma prolimfocitară a leucemiei limfocitare cronice, așa cum este descris în literatură (Volkova M.A.; Taylor şi colab), diferă în primul rând prin morfologia limfocitelor, care în frotiuri (sânge și măduvă osoasă), amprentele au un nucleol mare clar, condensarea cromatinei în nucleu, după cum arată microscopia electronică, este moderat exprimată și în principal de-a lungul periferiei. În preparatele histologice ale ganglionilor limfatici și ale splinei în această formă de leucemie, limfocitele conțin și nucleoli. Aceste celule nu au caracteristici citochimice. Caracteristica imunologică dezvăluie fie natura celulelor B sau T a leucemiei limfocitare, de cele mai multe ori prima. Spre deosebire de limfocitele B ale leucemiei limfocitare cronice tipice, cu această formă, pe suprafața limfocitelor leucemice se găsește o abundență de imunoglobuline, mai des de tip M sau D.
Caracteristicile clinice ale acestei forme sunt dezvoltarea rapidă, o creștere semnificativă a splinei și o creștere moderată a ganglionilor limfatici periferici.
Leucemie limfocitară cronică cu paraproteinemie, se caracterizează prin obișnuit tablou clinic una dintre formele enumerate anterior ale procesului, dar este însoțită de M- sau G-gamapatie monoclonală.
formă de celule păroase. Denumirea formei provine de la caracteristicile structurale ale limfocitelor care o reprezintă. Aceste celule au un nucleu „tiner”: omogen, uneori asemănător cu nucleul structural al blastelor, alteori resturi de nucleoli, având adesea o formă neregulată și contururi neclare. Citoplasma celulelor este diversă: poate fi largă și are marginea festonată, poate fi zdrențuită, neînconjurând celula pe tot perimetrul, poate avea muguri asemănătoare firelor de păr sau vilozități. În unele cazuri, citoplasma limfocitelor în această formă de leucemie limfocitară cronică este bazofilă, mai des de culoare gri-albastru. Nu există granularitate în citoplasmă. Caracteristicile structurii limfocitelor, care fac să suspecteze o formă de celule păroase de leucemie limfocitară cronică, sunt vizibile la microscopul cu lumină, dar mai detaliat - într-un microscop cu contrast de fază și cu microscopie electronică.
Testul de diagnostic care confirmă diagnosticul de leucemie cu celule păroase este caracterizarea citochimică a celulelor leucemice.
Se știe că limfocitele din această formă de leucemie au o anumită capacitate de a absorbi particulele de latex. Aceste caracteristici ale celulelor leucemice cu celule păroase fac de înțeles îndoielile de lungă durată cu privire la natura lor limfatică.
Metodele imunologice au arătat că în cele mai multe cazuri este o formă cu celule B de leucemie limfocitară cronică, deși au fost descrise cazuri de leucemie limfocitară T cu celule păroase. Limfocitele normale originale din care a provenit leucemia cu celule păroase sunt încă necunoscute.
Tabloul clinic al leucemiei cu celule păroase este destul de caracteristic: citopenie moderată până la severă, mărirea splinei, dimensiuni normale ganglionii limfatici periferici.
În trepanatul măduvei osoase se poate observa creșterea interstițială a celulelor leucemice, care, de regulă, nu se formează proliferează și nu înlocuiesc complet țesutul hematopoietic și grăsimea. Histologia splinei sugerează creștere difuză limfocite leucemice atât în pulpa roșie, cât și în cea albă, ștergând structura acestui organ.
Cursul leucemiei cu celule păroase variază. El, ca și alte forme de leucemie limfocitară cronică, poate să nu dea semne de progresie ani de zile. Există granulocitopenie, care uneori duce la complicații infecțioase fatale, și trombocitopenie cu sindrom hemoragic.
în formă de T. Leucemia limfocitară cronică, reprezentată de limfocitele T, apare în aproximativ 5% din cazuri. Infiltrarea leucemică în această formă de leucemie, spre deosebire de boala Cesari, afectează de obicei straturile profunde ale dermului și țesutului pielii. Boala debutează la persoanele cu vârsta peste 25 de ani.
Tabloul de sânge include leucocitoză de severitate diferită, neutropenie, anemie. Limfocitele leucemice au nuclei mari, rotunzi, în formă de fasole, polimorfi, malformați, grosolan, adesea răsuciți, cromatină; în citoplasmă pot fi observate granule azurofile mai mari decât granulele limfocitelor obișnuite. Dimensiunea celulei este diferită.
Citochimic, în aceste celule, poate fi detectată activitate ridicată a fosfatazei acide (de natură lizozomală), α-naftil acetat-esterazei, localizată local în citoplasmă. Din punct de vedere imunologic, limfocitele care alcătuiesc substratul acestei forme de leucemie, după cum arată studiul markerilor lor de suprafață folosind anticorpi monoclonali, pot fi T-helper în unele cazuri, T-supresoare în altele și helpers și supresori în altele.
Împreună cu această formă de leucemie cu celule T rapid progresivă, a fost descrisă o formă benignă cu limfocite T mari, granulare.
Tratament (principii generale)
Indicațiile pentru tratamentul leucemiei limfocitare cronice se înrăutățesc starea generala, apariția citopeniei, o creștere rapidă a ganglionilor limfatici, splina, ficat, apariția infiltrației leucemice a trunchiurilor nervoase și a organelor nehematopoietice, ducând la sindrom de durere sau disfuncție a funcției; o creștere constantă a nivelului de leucocite. Cu rezistență primară la clorbutină, nu este re-prescris. Doza de clorbutină pentru terapia de întreținere este de 10-15 mg de 1-2 ori pe săptămână.
Ciclofosfamida este prescrisă pentru leucemia limfocitară cronică rezistentă la clorbutină, precum și pentru o creștere a leucocitozei, o creștere semnificativă a ganglionilor limfatici sau a splinei și o tendință la trombocitopenie. Doza de ciclofosfamidă este de 2 mg/kg pe zi. Tratamentul intermitent cu doze mari de 600 mg/m2 o dată pe săptămână poate fi eficient. Efectul ciclofosfamidei este instabil, medicamentul suprimă imunogeneza, așa că nu ar trebui utilizat pentru o lungă perioadă de timp.
Hormonii steroizi în tratamentul leucemiei limfocitare cronice ocupă un loc special: duc la o scădere rapidă a ganglionilor limfatici, eliminarea intoxicației, normalizarea temperaturii, îmbunătățirea stării de bine, dar nu este nimic mai periculos decât numirea prednisolonului pentru tratamentul acestor pacienti.
Terapia izolată cu prednisolon sau adăugarea acestuia ca medicament permanent la o altă terapie citostatică intermitentă sau leucafereză este fatală din cauza complicațiilor infecțioase foarte frecvente și severe, pe de o parte, și foarte ineficientă în ceea ce privește, pe de altă parte. Scăderea ganglionilor limfatici este însoțită de o creștere a leucocitozei, normalizarea temperaturii și dispariția altor semne de intoxicație se observă numai cu aportul constant de prednisolon, ele reluând cu și mai multă forță imediat după anularea acestuia.
Datorită sindromului de sevraj specific tumorilor cu celule mature limfoproliferative, chiar și după utilizarea programelor citostatice, care include prednisolon (COP, VAMP), este necesar să se înceapă reducerea dozei până la sfârșitul programului de tratament și să se continue utilizarea, reducând doza, timp de câteva zile după încheierea programului.
În leucemia limfocitară cronică, unul dintre tratamentele eficiente este radioterapia. Cu o creștere a ganglionilor limfatici periferici ai cavității abdominale în condiții de citopenie sau cu nivel inalt leucocite și trombocitopenie, o dimensiune semnificativă a splinei, infiltrare leucemică în regiunea trunchiurilor nervoase sau un proces distructiv în țesut osos radioterapia locală devine necesară.
Cu expunere locală o singura doza este 1,5-2 Gy. Doza totală la focar este determinată de locul de localizare a acestuia. Splina este de obicei iradiată într-o doză totală de 6-9 Gy, deoarece doze mari poate duce la citopenie profundă și, prin urmare, necesită monitorizarea constantă a sângelui periferic în timpul tratamentului. Iradierea splinei duce la o scădere nu numai a acestui organ, ci adesea a ganglionilor limfatici cervicali și axilari. În cazul distrugerii vertebrale, doza totală locală de radiație este de 25 Gy. Radioterapia locală dă adesea un efect de durată: în zona de iradiere, de regulă, infiltrația limfatică nu se agravează.
Iradierea totală fracționată pentru leucemia limfocitară cronică a fost utilizată cu succes în anii 1950 de către Osgood (1951, 1955). Această metodă de radioterapie poate fi eficientă acolo unde chimioterapia este dificil de utilizat sau s-a dovedit ineficientă.
În complex măsuri medicaleîn leucemia limfocitară cronică, îndepărtarea splinei a început să fie utilizată pe scară largă. Dezvoltarea citopeniei profunde, care nu sunt cauzate de citostatice, necesită numirea hormonilor glucocorticosteroizi. Dacă un curs lunar de hormoni nu a dat un efect de durată și, după anularea lor, citopenia a început să crească din nou, atunci este necesară îndepărtarea splinei.
Un alt indiciu important pentru îndepărtarea splinei este dimensiunea splinei. Dacă în cazul limfocitomului splenic, diagnosticul tumorii în sine stă la baza splenectomiei, atunci în leucemia limfocitară cronică cu splenomegalie problema operației nu este atât de clar rezolvată. În leucemia limfocitară cronică după intervenție chirurgicală, poate apărea o creștere destul de rapidă a ficatului ca urmare a proliferării limfocitare progresive în acesta.
De asemenea, indicații pentru extirparea splinei în leucemia limfocitară cronică sunt creșterea rapidă a splinei, necontrolată de citostatice, apariția infarctelor splinei, durerea persistentă în hipocondrul stâng, organele de dimensiuni foarte mari cu proces incontrolabil. medicamentele(creșterea leucocitozei, exacerbarea infecțiilor, epuizare incipientă, mărirea concomitentă a ficatului, febră neinfecțioasă persistentă).
Leucofereza este utilizată în cazurile de leucocitoză severă, în care terapia citostatică cu doze convenționale de medicamente este ineficientă; leucofereza este de obicei eficientă în trombocitopenie și agranulocitoză pe fondul leucocitozei mari.
Plasmafereza în leucemia limfocitară cronică se utilizează în cazurile de sindrom de vâscozitate crescută care se dezvoltă cu forme secretoare ale bolii (boala Waldenström, leucemie limfocitară cronică cu secreție monoclonală de imunoglobuline G); plasmafereza prelungită este indicată pentru polinevrita care complică proliferarea limfatică.
Tratamentul formelor individuale
Cu o formă benignă de leucemie limfocitară cronică, tratamentul cu citostatice nu este început de mult timp. O indicație pentru terapia citostatică este o creștere a subiectivității disconfort(slăbiciune, transpirație) cu creșterea numărului de leucocite; de regulă, ajunge deja la 50 × 10 3 în 1 µl. În acest caz, se începe terapia cu clorbutină (leukeran). doza zilnica 5-10 mg sub controlul sângelui, încercând să nu treacă în reducerea pragului de leucocitoză de 2 × 10 4 - 3 × 10 4 la 1 µl. Tratamentul urmărește să nu obțină nicio îmbunătățire, ci doar o compensare clinică; se efectuează în ambulatoriu și, de obicei, pacienții sunt capabili să lucreze.
Cu o formă progresivă, cel mai potrivit principiu de tratament pentru mulți ani a fost abordarea primară de restrângere, a cărei esență este limitarea procesului leucemic cu doze constante moderate de medicamente citostatice deja în stadiile incipiente, când leucocitoza nu a ajuns încă foarte mult. numere mari. Utilizați următoarele programe.
Clorbutina în doză de 5-10 mg/zi sau ciclofosfamidă în doză de 200 mg/zi (cu o creștere predominantă a numărului de leucocite pe fond de limfadenopatie moderată, este de obicei preferată clorbutina, cu limfadenopatie severă pe fond de cu creștere lent și leucocitoză nu foarte mare, ciclofosfamida este prescrisă mai des). Scopul terapiei citostatice este de a obține compensarea somatică cu stabilitate pe fondul leucocitozei în sânge, de preferință mai mică de 50 × 10 3 în 1 μl.
Programul M-2 ( Kempin şi colab): în prima zi a cursului se administrează intravenos 2 mg vincristină, 600-800 mg ciclofosfamidă (10 mg/kg), BCNU în doză de 0,5 mg/kg; alte medicamente sunt administrate pe cale orală - melfalan (Alkeran) la 0,25 mg / kg (sau sarcolizină la 0,3 mg / kg) 1 dată pe zi timp de 4 zile consecutive, prednisolon în doză de 1 mg / (kg / zi) timp de 7 zile, jumătate din această doză pentru următoarele 7 zile și un sfert din doza inițială pentru 15-35 de zile de tratament. Potrivit autorilor, programul de tratament dezvoltat de ei face posibilă obținerea remisiunii în 17% din cazuri cu o durată medie de viață a pacientului de peste 7 ani. Încetarea tratamentului a dus la recidivă.
Tratamentul formei tumorale a leucemiei limfocitare cronice s-a dovedit a fi, de asemenea, mai de succes atunci când se utilizează programe intensive de polichimioterapie - COP, CHOP, M-2 (BCNU, ciclofosfamidă, sarcolizină, vincristină, prednisolon). Când se utilizează programul M-2, sunt descrise remisiunile ( Kempin şi colab), care persistă numai cu continuarea tratamentului. Primele 2 programe duc relativ rar la remisie, dar pot realiza o reducere semnificativă a ganglionilor, ceea ce este deosebit de important pentru conglomeratele din cavitatea abdominală. Pentru a menține îmbunătățirea obținută, puteți utiliza monoterapia - cure intermitente de ciclofosfamidă.
Repetările multiple ale cursurilor COP și CHOP sunt destul de dificile pentru pacienții cu leucemie limfocitară cronică, deoarece abolirea prednisonului în aceste cursuri duce adesea la creșterea bruscă a temperaturii la 37,5 ° C, o deteriorare bruscă a stării generale, transpirație, slăbiciune și o slăbiciune semnificativă. creșterea infecțiilor. Efectuând aceste cursuri, este necesar să începeți reducerea dozei de prednisolon în a 9-a-10-a zi de tratament, amânând anularea acesteia cu 3-6 zile după terminarea cursului.
După obținerea unei îmbunătățiri stabile cu cursuri COP sau CHOP (de obicei 6 cure), terapia intermitentă cu ciclofosfamidă este prescrisă după 2 săptămâni: 200 mg de ciclofosfamidă pe cale orală zilnic sau o dată la două zile timp de 5 sau, respectiv, 10 zile (doza totală de medicament 1000 mg) , o pauză între cursuri 10-12 zile. Cu o scădere a nivelului de trombocite - mai puțin de 1,5 × 10 3 în 1 μl, sau leucocite - mai puțin de 4-5 × 10 3 în 1 μl, intervalele dintre ciclurile de ciclofosfamidă sunt prelungite până când acești indicatori se îmbunătățesc sau se normalizează.
Durata terapiei intermitente cu ciclofosfamidă este imprevizibilă: se efectuează pentru a obține o stare stabilă compensată a pacienților.
Ca program independent pentru tratamentul formei tumorale a bolii, iradierea totală fracționată este utilizată la 0,03-0,06-0,12 Gy pe sesiune zilnic, doza totală este de 0,5-1,2 Gy ( Johnson, Rubin și colab). Această terapie poate fi periculoasă la niveluri WBC sub 2 x 10 3 în 1 µl.
Cu o eficiență scăzută a programelor, radioterapia locală este utilizată în zona ganglionilor limfatici măriți și a splinei. De obicei, splina este iradiată mai întâi (în cazul unei măriri accentuate a amigdalelor, acestea sunt iradiate mai întâi), este planificat un program de iradiere suplimentar în funcție de scăderea ganglionilor periferici și de leucocitoză după iradierea splinei.
În tratamentul formei splenomegalice, îndepărtarea splinei este adesea folosită ca primă etapă, ceea ce duce adesea la mulți ani de compensare somatică la pacienții cu stabilitate hematologică fără tratament suplimentar. Manifestarea tulburărilor subiective (transpirație, slăbiciune, scăderea capacității de muncă), o creștere a leucocitozei, o mărire progresivă a ficatului după intervenție chirurgicală necesită numirea terapiei citostatice în conformitate cu tabloul clinic și hematologic al bolii în curs de dezvoltare.
Tratamentul formei de măduvă osoasă a leucemiei limfocitare cronice ( limfadeniei osoase) se efectuează cu ajutorul programului VAMP: 8 zile de tratament și 9 zile libere. Tratamentul conform acestui program este prescris la doza completă, în ciuda numărului inițial scăzut de leucocite și trombocite. Se efectuează cel puțin 8-10 cure, deși după 3-4 cure imaginea sângelui și a măduvei osoase arată de obicei deja o îmbunătățire completă.
Programele pentru tratamentul procesului citolitic în leucemia limfocitară încep aproape întotdeauna cu numirea prednisolonului în doză de 60-80-100 mg / zi până la ameliorarea stabilă a citolizei. Dacă în decurs de o lună de la terapia cu prednisolon, citoliza mare nu este oprită, atunci terapia cu steroizi ar trebui abandonată și trebuie efectuată splenectomia.
Procesul citolitic care s-a dezvoltat cu leucocitoză mare poate fi adesea oprit prin leucofereză. De obicei, produc 5-7 leucofereză înainte de a avea un efect pozitiv. Leucofereza s-a dovedit a fi cea mai eficientă în procesul trombocitolitic. Riscul de îndepărtare simultan cu leucocite și o anumită cantitate de trombocite, al căror conținut în sânge este deja scăzut, este mic: de obicei, după prima leucofereză, sângerarea scade, deși nu există încă o creștere a trombocitelor.
După terminarea procesului citolitic, terapia se efectuează conform formei de leucemie limfocitară cronică. În cazul reapariției citolizei pe fondul limfadenopatiei moderate, se recomandă utilizarea schemei VAMP.
În unele cazuri, leucemia limfocitară cronică cu citoliză este însoțită de o creștere pronunțată a temperaturii, dar aceasta în sine nu devine baza pentru modificarea programului obișnuit de tratament. Natura acestei creșteri a temperaturii este necunoscută.
Dispariția parțială a oricărui germen din măduva osoasă sugerează citoliză intramedulară, probabil din cauza anticorpilor la celulele măduvei osoase sau a efectului citotoxic al limfocitelor în sine. Tratamentul acestui sindrom se efectuează în același mod ca cel al citolizei periferice deschise.
Terapia utilizată în mod obișnuit pentru leucemia limfocitară cronică este în general ineficientă pentru forma prolimfocitară. Spre deosebire de forma splenomegalică a leucemiei limfocitare cronice, iradierea și îndepărtarea splinei nu au niciun efect. O combinație de cytosar cu rubomicina poate fi mai eficientă.
Leucemia limfocitară cronică cu producție de paraproteine se tratează după aceleași principii ca și celelalte forme de boală descrise mai sus, dar nu este asociată cu secreția de imunoglobuline. Deoarece forma secretantă a bolii poate evolua atât ca benignă, cât și ca progresivă, tumorală, măduvă osoasă, splenomegalică, se tratează după aceleași programe citostatice ca și formele corespunzătoare. Un plus important la terapia citostatică este plasmafereza, prescrisă pentru sindromul de hipervâscozitate.
Cel mai instrument eficient Tratamentul pentru forma celulelor păroase este splenectomia. Terapie eficientă pe termen lung cu clorbutină în doze mici - 2-4 mg pe zi. Normalizarea compoziției sângelui cu o astfel de terapie are loc după 6-10 luni de la începerea tratamentului. De asemenea, sunt utilizate deoxicoformicina (un inhibitor de adenozin deaminaza foarte activ în celulele T), o combinație de doze mici de vinblastină și clorbutină și interferon.


