21.04.2019
Tipuri de răspuns inflamator. Inflamația - o mare enciclopedie medicală
1. Adecvat caracterizat printr-o relație direct proporțională între puterea factorului dăunător și puterea inflamației.
2. inadecvat caracterizată printr-o discrepanță între puterea factorului dăunător și severitatea inflamației.
Aceasta poate fi o reacție hipoergică \ slăbită \
Reacție hiperergică \ intensificată \
Reacție hipoergică poate
1 \ reacție a forței imunității - atunci când un factor dăunător puternic este reflectat cu pierderi mai puține cu inflamație moderată
2 \ reacție de slăbiciune a imunității - când un factor dăunător slab duce la leziuni severe \ distrofie, necroză \, iar reacția inflamatorie este aproape absentă. Aceasta este o dovadă a lipsei de apărare a corpului și o însoțește boală gravă precum bolile de sânge.
Hiperergic reacţia reflectă întotdeauna o sensibilizare crescută a organismului. Poate fi rezultatul deteriorării imunității umorale și celulare. Și întotdeauna însoțește inflamația imună.
Există 2 tipuri de reacții hiperergice -
1\ Hipersensibilitatea de tip imediat apare imediat după expunerea la un antigen/medicament, polen de plante, Produse alimentareși alți alergeni. Se caracterizează prin inflamație acută cu dezvoltarea unei reacții alterativ-exudative. Inflamația este declanșată de factori umorali - anticorpi, complexe imune, antigeni.
2\ Hipersensibilitate de tip întârziat - observată cu încălcarea imunității celulare\ acțiunea agresivă a limfocitelor T și a macrofagelor\. Reacția inflamatorie are loc la o zi după expunerea la antigen. Un exemplu este inflamația pe piele la o zi după introducerea tuberculinei.
Clasificare.
Cu fluxul distingeți 3 tipuri de inflamații
1\ acută - până la 3 săptămâni
2 \ subacută - până la 3 luni
3\ cronice - mai mult de 3 luni.
Prin factori cauzali aloca:
1\banală\nespecifică\inflamație
2\inflamatie specifica\ inflamatie in tuberculoza, sifilis, lepra, rinosclerom, sapa\.
Software de patologie\ principiu de bază \ distinge 3 tipuri de inflamație, în funcție de predominanța uneia dintre componentele principale ale inflamației -
1\ alternativă
2\exudativ
3\proliferativ\productiv\.
1\ INFLAMAŢIA ALTERATIVA
În acest tip de inflamație predomină afectarea parenchimului organului. Reacția vasculară este slab exprimată. Gradul de deteriorare este foarte divers și variază de la distrofia obișnuită \ grad ușor deteriorare \ la necroză \ deteriorare necrotică \.
Patomorfologia depinde de gradul de deteriorare.
Exod- focarele mici se vindecă complet - la fata locului focare mari au format țesut cicatricial. Valoare - depinde de localizarea și severitatea procesului.
2\ INFLAMAŢIA EXUDATIVĂ
Se caracterizează prin predominanța reacției de exudare în timpul inflamației cu formarea unui revărsat, care determină întreaga imagine a inflamației.
În funcție de caracteristicile exudatului, se disting 7 tipuri de inflamație exsudativă -
A. Seros
B. Fibrinos
V. Purulent
G. putred
D. Hemoragic
E. catarală
J. Mixt.
1) Inflamație seroasă
caracteristici ale inflamației. Exudatul este un lichid care conține 3-8% albumină. Sunt puține celule. Cursul inflamației este acut. Hiperemia este bine exprimată. Porozitatea capilarelor este exprimată moderat. Localizare - cavități seroase \ cardiace, abdominale, pleurale \, meninge, stroma hepatică, miocard, rinichi.
Aspect exudat: lichid ușor tulbure, galben pai.
Motivele- termice, chimice, infectii etc.
Exod- favorabil: resorbtie completa. Rareori - scleroza - mai des în ficat, rinichi, miocard.
2) inflamație fibrinoasă
Exudatul conține multă fibrină. Deteriorarea capilarelor în acest tip de inflamație este semnificativă. Membranele seroase și mucoase sunt afectate mai des, mai rar stroma organelor.
Există 2 tipuri de această inflamație:
1\ crupus
2\ difterie
1\ Inflamație crupoasă. Cuvântul crupă \ corb-corb, croaiat, șuierător ca un corb \ subliniază localizarea predominantă a procesului \ de exemplu, membrana mucoasă a traheei, bronhiilor \. Se caracterizează prin formarea unui film fibrinos gri-galben. Filmul este slab conectat la suprafața mucoasei necrotice sau a membranei seroase. Când filmul este separat, este detectat un defect de suprafață.
2\ Inflamație difterică. Se caracterizează prin modificări necrotice profunde în straturile mucoase și submucoase. Prolapsul fibrinei apare atât în profunzime, cât și la suprafață. Filmul fibrinos de culoare gri-galben este strâns lipit de țesuturile subiacente, iar atunci când este respins, se formează un defect profund.
Difteric \ înseamnă piele \ procesul inflamator este observat nu numai în difterie. Acesta este un concept mai larg, deoarece inflamația difteriei apare în diferite tipuri de patologie.
Cauzele inflamației fibrinoase:
Bacterii: streptococi, stafilococi, bacili - tuberculoză, difterie etc.
uremie \ insuficiență renală\ - intoxicații endogene cu dezvoltarea pericarditei fibrinoase \ inimă păroasă \, pleurezie fibrinoasă etc.
intoxicații exogene.
curgere: 1\acut 2\cronic
Exod: micile defecte ale mucoaselor se vindecă, în locul celor mari, se formează țesut cicatricial cu posibila dezvoltare a stenozei, de exemplu, a traheei și bronhiilor.
Pe membranele seroase se formează întotdeauna aderențe fibroase, ceea ce poate duce la afecțiuni adezive atunci când este localizat în cavitatea abdominală și obstrucție intestinală.
Puroiul este un lichid gros, vâscos, gri-verde. Exudatul purulent conține o mulțime de globuline, fibrină și, cel mai important, neutrofile.
Tipuri de inflamație purulentă.
1\ Flegmon- abces vărsat. Se caracterizează prin răspândirea puroiului în spațiile intermusculare, în țesutul adipos, fascie, tendoane
2\ Abces- Inflamație purulentă delimitată. Există puroi în cavitatea abcesului, peretele abcesului este format dintr-o membrană piogenă.
Localizarea este diferită: piele, cap, rinichi, ficat, plămâni și alte organe interne.
3\ empiem- inflamatie purulenta a cavitatii: pleurala, abdominala, articulatiilor.
4\ Furuncul- inflamația purulentă a foliculului de păr.
5\ Carbuncul- inflamația purulentă a unui grup de foliculi de păr.
6\Paranychius- Inflamatia purulenta a patului periungual.
7\ Infractor- inflamație purulentă a degetului.
Motivele: mai des microorganisme piogene \ toate tipurile de infecție cocică \, bacili de tuberculoză, ciuperci, agenți chimici.
Curs - 1 \ Acut 2 \ Cronic.
Acut se produce sub formă de inflamație difuză sau limitată. În cazurile severe, procesul se extinde pe suprafețe mari și poate provoca moartea prin intoxicație și insuficiență de organe multiple.
Continuă cronică pentru o lungă perioadă de timp cu dezvoltarea fibrozei în jurul procesului purulent. Oferă complicații precum - pasaje fistuloase cronice, dungi extinse de puroi, intoxicație, epuizarea plăgii, amiloidoză.
4. Inflamație putridă
Se dezvoltă atunci când o inflamație a unei infecții putrefactive intră în zonă. Se caracterizează printr-o creștere a proceselor necrobiotice, formarea de gaz fetid.
5. Inflamație hemoragică
Apare atunci când eritrocitele pătrund în exsudat. Acest lucru indică leziuni severe ale microvasculaturii. Se observă în forme severe de gripă, variola neagră naturală, antrax, ciumă.
6. Catar .
Aceasta este o inflamație a membranelor mucoase cu formarea de mucus și acumularea acestuia în exudat. Compoziția exudatului este diferită, dar conține întotdeauna mucus.
Forme de catar \ catar \:
1\ Seros. Exudatul noroios este caracteristic. Mucoasa este umflată, cu sânge. notat în viral infectie respiratorieîn organele respiratorii şi în holeră în mucoasa intestinului subţire.
2\Slimy. Caracterizat prin prezența unei cantități mari de mucus. Exudatul este vâscos, situat pe mucoasa hiperemică. Localizare – organe respiratorii și digestive. În epiteliul mucoasei, sunt adesea observate celule caliciforme sau cricoide. Motivele sunt diferite. Rezultatul este favorabil.
3\ Purulent. Inflamație purulentă severă urmată de procese erozive și ulcerative, precum și de fibroză și deformare.
Cursul catarului este acut și cronic.
Rezultatul inflamației acute depinde de forma catarului - cu membranele seroase și mucoase, are loc recuperarea completă, cu procese purulent-cicatricial-ulcerative cu stenoză și deformare.
Catarul cronic decurge în funcție de tip
1\ catar atrofic cu dezvoltarea atrofiei \ scaderea grosimii mucoasei \.
2\ catar hipertrofic - cu ingrosarea mucoasei datorita proliferarii structurilor parenchimatoase si mezenchimatoase.
În acest caz, există o încălcare a funcției organului cu dezvoltarea gastritei cronice, enteritei, colitei, bronșitei, emfizemului și pneumosclerozei.
7. Inflamație mixtă : seros-purulent, seros-fibrinos, purulent-fibrinos și altele.
De obicei, se dezvoltă atunci când o nouă infecție se alătură în cursul inflamației, forțele reactive, de protecție ale corpului se schimbă semnificativ.
Inflamația seroasă se observă cu leziuni închise, arsuri, după utilizarea abceselor, cu infecție cu microbi slab virulenți.
Inflamația seroasă se caracterizează prin formarea unui exsudat seros lichid, limpede sau ușor tulbure. Conține 3-5% proteine, în principal albumină, produse ale metabolismului și degradarii celulelor tisulare, o cantitate mică de celule vasogenice, precum și celule detașate de țesut local.
Prezența unei cantități semnificative de fibrină în exudatul seros caracterizează inflamația serofibrinoasă. Uneori, inflamația seroasă se transformă în purulentă.
Impregnarea seroasă a țesuturilor din cauza umflării coloizilor țesuturilor deteriorate, observată în răni și leziuni închise, ar trebui să fie distinsă de inflamația seroasă; se numește edem traumatic și apare în primele ore după leziune pe fondul anemiei, și nu hiperemie inflamatorie. Nu există fenomene exudative celulare în edemul traumatic (IV Davydovsky). În absența infecției și a iritației mecanice suplimentare, acest edem este ușor de rezolvat.
Inflamația fibrinoasă se observă cel mai adesea în afecțiunile articulațiilor, tecilor tendonului, burselor și altor structuri anatomice căptușite cu membrane sinoviale, mucoase sau seroase (pleura, peritoneul, uretra, conjunctiva). Exudatul inflamator conține multe elemente formate și fibrinogen, care, sub acțiunea enzimelor celulelor deteriorate, se transformă în fibrină. Acesta din urmă se depune sub formă de fire în crăpăturile și spațiile tisulare, precum și pe suprafața membranelor mucoase, seroase sau sinoviale, unde formează o rețea densă de pâslă sau depozite fibrinoase masive.
Straturile fibrinose servesc adesea ca o sursă de aderență parțială sau completă a membranelor sau a organelor (intestinelor) care sunt în contact unele cu altele. În astfel de cazuri, inflamația fibrinoasă se numește inflamație adezivă sau adezivă. Consecințele acesteia, în funcție de locul de dezvoltare și zona de deteriorare, sunt diferite. De exemplu, fuziunea membranei vaginale comune cu membrana testiculară proprie, chiar și în cazurile de obliterare completă a cayum vaginale, are un efect redus asupra functii fiziologice a gonadei, în timp ce aderențele intraperitoneale servesc ca sursă de durere ireparabilă și tulburări funcționale severe, încălcare a ansei intestinale și alte boli foarte periculoase.
Lucrările studenților lui Girgolav au dovedit că aderențele intraperitoneale organizate (sub formă de corzi și șuvițe) cresc cu vasele „conțin fibre musculare netede și uneori striate, precum și elemente nervoase pulpe și nepulmonice.
Purulent inflamația se caracterizează prin formarea de exudat purulent sau puroi. Este un lichid tulbure de consistență cremoasă sau lichidă, de culoare alb-cenușiu, gri-gălbui sau gri-verde. Puroiul este format din ser purulent și elemente celulare.
În stadiul inițial proces inflamator puroiul conține o cantitate imensă de leucocite segmentate fagocitare și nefagocitare. Alături de leucocitele vii, care au păstrat bine nucleul și protoplasma, există leucocite moarte care se află în diferite stadii de degenerare și dezintegrare. Aceste celule moarte se numesc corpuri purulente.
Pe lângă leucocitele segmentate și corpurile purulente, puroiul conține diferite celule ale sistemului reticuloendotelial și o masă de elemente celulare de țesut local mort. În funcție de localizarea focarului purulent, de intensitatea și durata procesului, este posibil să se detecteze în puroi rămășițele de mănunchiuri de colagen umflate, fibre elastice, nisip osos, fibre de țesut fibros, fibre libere, nuclei de celule musculare etc. Alături de elementele celulare enumerate, în puroi se găsesc limfocite și globule roșii.
Cu cât procesul purulent este mai intens, cu atât elementele celulare ale țesutului local și celulele vasogenice sunt distruse și topite mai repede.
Ser purulent. Partea lichidă a puroiului conține detritus de țesut, care se formează ca urmare a degenerării și degradarii elementelor celulare, țesutului celular și enzimelor microbiene, microbi vii și uciși. Cel mai adesea se găsesc în puroi: enzime proteolitice, care sunt eliberate după descompunerea leucocitelor segmentate sau sunt secretate de microbi și provoacă topirea țesuturilor; enzime trefon secretate de limfocite, favorizand regenerarea tesuturilor si, aparent, apar in cantitati mari odata cu dezvoltarea granulatiei; lipază (o enzimă care dizolvă grăsimile), amilază, tripsină, hialuronidază, precum și diverși anticorpi - bacteriolizine, antitoxine, hemolisine, opsonine, endo- și exotoxine etc.
În plus, serul purulent conține acetonă, glicogen, zahăr de struguri, grăsimi, săruri medii (fosfat de amoniac-magneziu, sare de masă) și corpi proteici rezultate din degradarea celulară: globuline, nucleină, leucină, albumoze, peptone și tirozină. Exudatul purulent are cel mai adesea o reacție neutră și o greutate specifică mare. Proprietăți fiziceși compoziție chimică puroiul sunt diferiti, in functie de cauza supuratiei, reactia locala si generala a animalului (vezi capitolul abcese).
Inflamația putrefactivă va fi descrisă în capitolul despre Infecții putrefactive.
În funcție de cauzele procesului inflamator, există inflamații banale și specifice. Banal poate fi cauzată de diferite microorganisme, factori fizici și chimici. specific provoacă agenți patogeni ai anumitor infecții (tuberculoză, sifilis, lepră). Cursul inflamației poate fi acut, subacut și cronic. În funcție de cauzele procesului inflamator și de condiții, poate predomina una dintre etapele inflamației. Prin urmare, alocați:
1. alternativă
2. exudativ
3. proliferativ
1. Când alternativă In inflamatie predomina procesul de alterare celulara, iar exudatia si proliferarea sunt slab exprimate (inima, ficatul, rinichii, creierul), deci aceasta inflamatie se numeste parenchim. În cazul în care un modificări distrofice duce la moartea celulelor și țesuturilor, o astfel de inflamație este necrotică. Se dezvoltă sub acțiunea unor substanțe toxice foarte active (acide, alcaline) asupra țesuturilor.
2. Când exudativ inflamația este dominată de procesul de exudare. În funcție de compoziția exudatului, există:
Seros
Fibrinos
Purulent
hemoragic
Amestecat
Dacă există mucus în exudatul seros sau purulent, se numește catar. Dacă inflamația este însoțită de degradarea țesuturilor, se numește putrefactiv.
Inflamația seroasă se caracterizează prin prezența exudatului seros, care conține 3% proteine și nu conține celule descuamate. Este transparent, dar dacă leucocite moarte sunt amestecate cu el, atunci devine tulbure. Inflamația seroasă se dezvoltă în organele parenchimatoase, pe membranele seroase ale cavităților și mucoasele organelor (cu pleurezie seroasă, exudatul se acumulează în cavitatea pleurală. Pleura devine tulbure, cu sânge; cu miocardita seroasă, exudatul se acumulează între mușchi. fibre ale inimii, care își pierd striația transversală și se dezintegrează; în rinichi exudatul se acumulează în cavitățile capsulelor glomerulare). Inflamația seroasă a pielii în timpul unei arsuri are loc cu formarea de vezicule, deoarece. exudatul se acumulează sub epidermă și îl exfoliază. Dacă exudatul se acumulează pe membrana mucoasă, atunci mucusul este adesea amestecat - cataral seros. De obicei, inflamația seroasă este acută și se termină bine. După aceasta, țesutul original este restaurat. Rareori, țesutul conjunctiv crește și se dezvoltă scleroza organului, iar în cavități se formează aderențe.
Inflamația fibrinoasă se caracterizează prin conținutul de exudat, care conține proteina fibrinogen. Odată ajuns în țesut, fibrinogenul trece în fibrină, se coagulează în fire subțiri albe. În acest caz, pe organe se formează o peliculă albicioasă. Inflamația fibrinoasă poate fi crupoasă și difterică. Dacă filmul este legat lejer de țesuturile subiacente și este ușor separat de ele - crupus. Dacă filmul aderă strâns la țesuturile subiacente și când este separat, se formează ulcere - difteric. Inflamația fibrinoasă croupoasă se dezvoltă adesea la copiii cu difterie, în timp ce filmul este ușor separat și poate înfunda lumenul traheei, ceea ce duce la asfixie.
Cu inflamația croupoasă a pericardului, apare efectul „inimii păroase”. La sfârșitul inflamației crupuse, țesutul original este de obicei restaurat. În cazul inflamației difterice, apare întotdeauna necroza mucoasei și submucoasei. La sfârșitul unei astfel de inflamații, la marginile ulcerului se formează țesut de granulație, care se maturizează într-o cicatrice. Aceasta determină formarea de aderențe între foile pleurei, între epicard și pericard, între membrana seroasă a intestinului și peritoneul parietal.
Inflamația purulentă se caracterizează prin prezența unei cantități mari de proteine și leucocite, inclusiv cele moarte (corpi purulenti). Puroiul este o masă cremoasă de culoare galben-verde cu miros urât. Necroza țesutului inflamat apare întotdeauna sub acțiunea enzimelor lizozomilor leucocitelor neutrofile în timpul degradarii acestora.
Ca urmare a topirii țesuturilor, se formează o cavitate în el, umplută cu puroi și care conține microorganisme. În jurul cavității se formează un arbore celular de leucocite și macrofage - un abces - o inflamație purulentă limitată. În mușchi, exudatul purulent se poate răspândi difuz - flegmon - inflamație purulentă nelimitată. Odată cu acumularea de puroi, se formează un canal prin care puroiul este îndepărtat periodic spre exterior. Într-un curs cronic, acest canal este căptușit cu țesut de granulație - o fistulă permanentă. Inflamația purulentă poate apărea acut, subacut și cronic. Este cauzată de microorganisme piogene. O astfel de inflamație este periculoasă datorită localizării sale (creierul). În cazul unei pătrunderi a puroiului în fluxul sanguin, microorganismele se răspândesc - sepsis.
Inflamația hemoragică se caracterizează prin prezența celulelor roșii din sânge în exsudat. Se dezvoltă cu microbi și boli virale(gripa virală, antrax, ciuma). Are loc acut și sever, rezultatul depinde de tipul de agent patogen.
Inflamația putrefactivă se caracterizează prin prezența bacteriilor putrefactive. Țesuturile cu această inflamație dobândesc culoare inchisași miros urât. Se derulează foarte greu și se termină cu moartea pacientului.
3. proliferativ (productiv)) se caracterizează prin procesul de reproducere celulară.
intermediar (interstitial)) inflamația se dezvoltă în țesutul interstițial al organelor parenchimatoase. Infiltratul inflamator conține limfocite, monocite și plasmocite. Unele dintre ele trec în fibroblaste, care formează proteina protocollagen. Acesta servește ca bază pentru construirea fibrelor de colagen ale țesutului conjunctiv. În rezultatul inflamației, se dezvoltă scleroza difuză a organului.
Granulomatos inflamația se caracterizează prin acumularea în țesutul inflamat de celule capabile de fagocitoză. Ele formează grupuri sub formă de noduli (granuloame). Sunt vizibile doar la microscop. Apar cu febră tifoidă, tifos, reumatism, tuberculoză, sifilis, lepră. Granuloamele cresc în plămânii oamenilor care lucrează mult timp în industrii periculoase. Adesea, în centrul granulomului se formează centrul necrozei. Maturarea granulomului se termină cu scleroza acestuia. Adesea se depune var în ele, adică. are loc pietrificarea.
specific inflamația se dezvoltă în tuberculoză și sifilis ( curs cronic). Inflamația este de natură specifică cu formarea de granuloame. În cursul inflamației, granuloamele suferă necroză brânză specifică.
Cursul acestor boli este însoțit de o restructurare imunitară semnificativă a organismului. Cu tuberculoza inflamație acutăîncepe cu o reacție alternativă, rezultând în formarea unui focar de necroză brânză. Apoi se formează granuloame tuberculoase - mici, cu un cap de ac, tuberculi albici. Necroza cașului conține Mycobacterium tuberculosis. Odată cu progresia inflamației specifice, tuberculii celulari se îmbină, formând noduri mari închegați - tuberculi solitari. Când procesul încetează, fibroblastele formează o capsulă de țesut conjunctiv în jurul granulomului. Granulomul este sclerozat, varul se depune în focarul de necroză, iar granulomul trece în petrificat.
Cu sifilisul cauzat de treponemul palid, se formează și granuloame în organele interne. Granuloame sifilitice - gume.
Pot fi unice și multiple, cu diametrul de 3–5 cm.Sunt mai des localizate în oase și ficat. Când procesul încetează, guma scleroză într-o cicatrice aspră în formă de stea.
Reacția de inflamație este o reacție universală de protecție a organismului la acțiunea diferiților factori patogeni (mecanici, fizici, chimici, biologici etc.), datorită cărora factorii care au cauzat daune sunt neutralizați și distruși. Pielea deteriorată este cea mai accesibilă poartă pentru agenții infecțioși. Agenții patogeni invadatori induc un răspuns inflamator complex care atrage leucocitele și componentele plasmatice solubile la locul infecției, ducând la localizarea și distrugerea microorganismelor în zona de introducere a acestora (Fig. B.3 și Fig. 22 im Reacție inflamatorie acută ).
Cel mai caracteristici raspuns inflamator:
Flux sanguin crescut
Expansiunea capilarelor și creșterea aportului lor de sânge (hiperemie),
O creștere a permeabilității capilare și, ca urmare,
Astfel, permeabilitatea capilară crescută asigură ieșirea anticorpilor, componentelor complementului și a altor sisteme enzimatice ale plasmei sanguine, diferite tipuri de celule sanguine din capilare în țesutul deteriorat; cel mai mare număr dintre ele se încadrează pe forme de celule fagocitare. Diferite populații de celule apar, de regulă, una câte una (schimbare de fază). Tipul de celule prezente la un moment dat, predominanța anumitor celule și momentul apariției lor - toate acestea depind de natura antigenului și de locul corpului în care se desfășoară reacțiile imunologice.
De obicei, în cea mai timpurie perioadă de inflamație în focarul infecției, mai ales neutrofilele, dar mai târziu și monocitele și limfocitele migrează în ea. Celulele T CD8 și câteva celule B ajung de obicei mai târziu.
Dezvoltarea inversă a unei reacții acute depinde dacă organismul a reușit să se elibereze de antigen sau infecție. Dacă nu reușește, răspunsul inflamator acut devine cronic, în care există puține neutrofile în focalizare, dar celulele T CD4 și fagocitele mononucleare se acumulează în număr semnificativ.
După cum sa menționat deja, un întreg set de mediatori participă la formarea răspunsului inflamator. Printre aceștia se numără mediatorii secretați de microorganisme și țesutul deteriorat, un grup de mediatori ai plasmei sanguine, mediatori vasoactivi secretați de leucocitele cu val timpurie. Aminele vasoactive cu acțiune rapidă și produsele sistemului kinin depind de răspunsul imediat. Recrutarea și activarea ulterioară a leucocitelor are loc sub acțiunea mediatorilor nou sintetizați, cum ar fi leucotrienele. Cu toate acestea, rolul principalului regulator aparține antigenului însuși. Prin urmare, focalizarea infecției cronice sau a reacțiilor autoimune (unde antigenul nu poate fi îndepărtat complet) diferă semnificativ în compoziția celulară a infiltratului din focarele de inflamație, eliberate rapid din antigen.
Un rol semnificativ în reglarea inflamației revine principalelor sisteme enzimatice ale plasmei sanguine: sistemul de coagulare, sistemul de fibrinoliză, sistemul kinin și sistemul complement.
Sistemul complement mediază interacțiuni multiple între răspunsul imun și inflamație. Multe dintre efectele proinflamatorii ale C3a și C5a se datorează capacității lor de a induce eliberarea conținutului de granule din mastocite.
Sistemul kinină include mediatorii bradikinină și lisilbradikinină (kalidină). Bradikinina este o peptidă vasoactivă foarte puternică din punct de vedere funcțional, care provoacă o creștere a lumenului venular și a permeabilității vasculare, precum și contracția mușchilor netezi. Se formează ca urmare a activării factorului Hageman (XII), care este legat de sistemul de coagulare a sângelui, în timp ce formarea kalidinei necesită activarea sistemului plasmină sau participarea enzimelor secretate de țesuturile deteriorate.
Celulele inflamatorii auxiliare joacă, de asemenea, un rol. Acestea includ
INFLAMAŢIE- un tesut vascular local complex, complex (mezenchimal) de protectie si adaptare a intregului organism la actiunea unui stimul patogen. Această reacție se manifestă prin dezvoltarea unor modificări ale circulației sângelui la locul afectarii unui țesut sau organ, în principal în patul microcirculator, o creștere a permeabilității vasculare în combinație cu degenerarea țesuturilor și proliferarea celulară.
Patologia generală
Scurte informații și teorii istorice
Întrebarea semnificației și esenței lui V. a primit întotdeauna un loc important în medicină. Până și Hipocrate credea că V. avea o valoare neutralizantă pentru organism, că începuturile nocive au fost distruse în focarul purulent și, prin urmare, formarea puroiului este utilă, vindecatoare, dacă nu se depășește o anumită limită a intensității procesului inflamator. Opiniile lui Hipocrate asupra naturii inflamației au dominat până în secolul al XVIII-lea, completate de o descriere a „semnelor cardinale” ale inflamației.
A. Celsus a descris patru pene principale, semnul lui V.: roșeață ( rubor), umflătură ( tumora), durere ( dolor), creșterea temperaturii ( calorii). Al cincilea semn este disfuncția ( functio laesa) descris de K. Galen; el a vorbit despre o inflamație ca despre febră locală și a subliniat o varietate de etiol, factori, secara pe care le poate provoca.
Primul aproape de vedere modernă despre V. a fost formulată în limba engleză. chirurgul J. Gunter, to-ry a definit V. ca reacția organismului la orice deteriorare. Gunter a considerat V. un proces de protecție care are loc întotdeauna la locul deteriorării, cu ajutorul căruia este restaurat functia normalațesut sau organ deteriorat.
Doctrina lui V. a început să se dezvolte după îmbunătățirea microscopului optic (mijlocul secolului al XIX-lea), precum și în prima jumătate a secolului al XX-lea. în legătură cu dezvoltarea biochimice, biofizice și histochimice. metode şi metode de studiu microscopic electronic al ţesuturilor. R. Virkhov (1859) a atras atenția asupra afectarii parenchimului organelor (modificări distrofice ale celulelor) în V. și a creat așa-numitul. teoria nutrițională („nutrițională”) B. Această teorie și-a pierdut semnificația în legătură cu studiile lui Samuel (S. Samuel, 1873) și Y. Kongeym (1887), to-ree importanța principală în patogeneza lui V. a fost acordată la reacţia vaselor mici (teoria vasculară B .).
AS Shklyarevsky (1869) a aplicat o metodă experimentală pentru studiul unui șanț de sânge la V. și a dat fizic. explicația fenomenului de „stare marginală a leucocitelor”. A. G. Mamurovsky (1886) a observat tromboza și blocarea limfei, vasele în centrul atenției lui V.
O contribuție deosebit de mare la dezvoltarea problemei lui V. a fost adusă de I. I. Mechnikov, care în 1892 a formulat teoria biologică a lui V., a dezvoltat doctrina fagocitozei (vezi), a pus bazele patologiei comparative a lui V. și teoria imunității celulare și umorale ( cm.). Procesul de absorbție a particulelor străine de către fagocite, inclusiv bacterii, a fost recunoscut de I. I. Mechnikov drept principalul proces central care îl caracterizează pe B. În prelegerile sale despre patologia comparativă a inflamației, I. I. Mechnikov a scris despre procesul de digestie intracelulară desfășurată în citoplasma fagocitelor .
Dezvoltarea ideii lui I. I. Mechnikov privind importanța fagocitozei pentru protejarea organismului de un factor patogen și formarea imunității a fost obținută în lucrările lui H. N. Anichkov, A. D. Ado, Kohn (E. J. Cohn, 1892 - 1953) și multi alti oameni de stiinta. Odată cu descoperirea în 1955 a organitelor citoplasmatice - lizozomi (vezi) - învățăturile lui I. I. Mechnikov despre citaze ca purtători ai funcției digestive a celulei au primit o confirmare suplimentară.
V. V. Voronin a stabilit în 1897 importanța stării țesutului interstițial și a tonusului vascular în V. Atribuind un rol secundar procesului de fagocitoză, a considerat procesele care au loc în substanța interstițială a țesutului conjunctiv drept principalele mecanisme care stau la baza V. ., și a dat o diferență față de interpretarea lui Mechnikov a fenomenului de emigrare, rătăcire celulară și fagocitoză. Teoria lui Voronin nu a dezvăluit biol, esența inflamației. V. V. Podvysotsky în „Fundamentals of General and Experimental Pathology” (1899) a scris că cu V. există o divergență a celulelor endoteliale, ca urmare a căreia se formează găuri între ele, prin care leucocitele pătrund din vas în spațiul perivascular.
În 1923 H. Schade a propus fiz.-chim. Teoria lui V.: în opinia sa, baza lui V. este acidoza tisulară, Crimeea și întregul set de modificări este determinat. Ricker (G. Ricker, 1924) a considerat fenomenele lui V. ca o manifestare a tulburărilor neurovasculare (teoria neurovasculară a lui V.).
Lucrările lui A. A. Maksimov (1916, 1927), A. A. Zavarzin (1950) și alți oameni de știință care au creat modele experimentale ale lui V. și au studiat transformarea formelor celulare în focusul B.
patologia comparativă
Descrierea clasică a patologiei comparative a lui V. a fost dată de I. I. Mechnikov, arătând că V. reprezintă întotdeauna o reacție activă a organismului, în orice stadiu. dezvoltare evolutivă el n-a fost. I. I. Mechnikov trasat diferite etape filogeneza, dezvoltarea tuturor fazelor reacției inflamatorii - alterare, exudare și proliferare, descrisă în detaliu fagocitoza; la animalele înalt organizate, un rol mare în fagocitoză a fost atribuit mecanismelor de neuroreglare. Organismul, subliniază I. I. Mechnikov, este protejat prin mijloacele de care dispune. Chiar și cele mai simple organisme unicelulare nu tratează pasiv stimulii nocivi, ci îi combate prin fagocitoză și acțiunea digestivă a citoplasmei. Cu toate acestea, chiar și la cele mai simple organisme unicelulare, atunci când sunt expuse la un factor patogen, apar modificări care sunt similare cu anumite procese distrofice din organismele multicelulare. La organisme pluricelulare reacția la deteriorare este complicată din cauza proliferării celulare și formate sistem vascular; organismul poate deja „trimite” un număr semnificativ de fagocite la locul rănirii. Pentru mai mult stadii târzii filogeneza în organisme are loc migrarea celulară. Odată cu formarea de endocrine și sistemele nervoase apar factori neuroumorali care reglează răspunsul inflamator.
La animalele foarte organizate, alte procese protectoare și adaptative se alătură fagocitozei: blocarea vaselor venoase și limfatice care drenează sângele din focarul V., exudarea lichidului seros care diluează produsele toxice și formarea de anticorpi prin proliferarea celulelor plasmatice care neutralizează factor patogen.
Datele despre fazele lui V. obținute în timpul studiului răspunsului inflamator în filogenie arată complicația acestuia pe măsură ce organismele evoluează; Fazele lui V. se repetă într-o anumită măsură în perioada prenatală a unei persoane. Yu. V. Gulkevich (1973) a arătat că embrionul are o reactivitate semnificativ mai mică în comparație cu organismul adult și cel mult primele etape dezvoltarea embrionară răspunde la efect nociv numai moartea, cu toate acestea, deja în stadiile incipiente de dezvoltare, se poate observa și proliferarea celulară. Exudația cu prezența leucocitelor a fost găsită în partea fetală a placentei și în membrana fetală la 10-12 săptămâni. și este cea mai recentă componentă ontogenetică a răspunsului inflamator. Fagocitoza la un germen al persoanei este efectuată de hl. arr. macrofage ale țesutului conjunctiv și, ulterior, granulocite segmentate.
Dezvoltarea unei reacții inflamatorii în ontogeneza umană este strâns legată de formarea imunolului, reactivitatea, care este exprimată morfologic prin apariția unui număr mare de celule plasmatice producătoare de imunoglobuline, al căror număr crește semnificativ atunci când apare un focar inflamator în corpul embrionului. Studiile arată că o reacție inflamatorie cu prezența tuturor semnelor de V. se stabilește în luna a 4-5 a vieții intrauterine. În perioada postnatală la V. influența asupra organismului a iritanților antigenici ai mediului și a imunolului se amplifică, procesele în încă Mai mult complica kliniko-morfol. profilul B.
Etiologie și mecanisme patogenetice
Reacția inflamatorie constă din mai multe faze interconectate: a) alterarea țesuturilor și a celulelor lor constitutive; b) eliberarea de substanţe fiziologic active (aşa-numiţii mediatori ai V.), care constituie mecanismele de declanşare ale lui V. şi implică o reacţie a vaselor de microcirculaţie; c) creșterea permeabilității pereților capilarelor și venulelor; d) reacții ale sistemului sanguin la deteriorare, inclusiv modificări ale proprietăților reologice ale sângelui (vezi Sânge, Reologie); e) proliferare - stadiu reparator B.
În scopuri practice, se recomandă împărțirea condiționată a celor trei componente principale interconectate ale lui V., care au un morfol clinic strălucitor. expresie: alterare cu eliberare de mediatori, reacție vasculară cu exudație și proliferare. Clasificarea principalului morfol, formele lui V. se bazează pe predominanța uneia sau alteia dintre aceste componente.
Alterare (deteriorarea țesuturilor și a celulelor) poate fi considerată ca urmare a acțiunii directe a factorului patogen și a tulburărilor metabolice care apar în țesutul afectat. Aceasta este prima fază a V.; caracterizează procesele inițiale și se manifestă morfologic de la tulburări structurale și funcționale abia vizibile până la distrugerea completă și moartea (necrobioză, necroză) țesuturilor și celulelor (vezi Alterarea). Modificările alternative ale V. sunt deosebit de pronunțate în țesuturile foarte diferențiate care îndeplinesc funcții complexe, de exemplu, în neuroni; în țesăturile care se efectuează hl. arr. funcția de susținere și stroma constitutivă a organului, de exemplu, în țesutul conjunctiv, modificările alterative sunt adesea dificil de detectat. În organele parenchimatoase, alterarea se manifestă prin diferite tipuri de degenerescență proteinacee (vezi) și degenerescență grasă (vezi), în stroma acestora, umflarea mucoidei și fibrinoide poate apărea până la necroza fibrinoidă (vezi Transformarea fibrinoidă).
În c. n. Cu. alterarea se exprimă printr-o modificare a celulelor ganglionare (neurocite) sub formă de liză a substanței bazofile (tigroide), împingerea nucleilor la periferie și picnoza (vezi), umflarea sau încrețirea celulelor. În mucoasele, alterarea se exprimă prin afectarea epiteliului, descuamare (vezi) cu expunerea membranei bazale; glandele mucoase secretă intens mucus, se adaugă epiteliu descuamat la tăietură, lumenii glandelor se extind (vezi Degenerarea mucoasă).
Modificări ultrastructurale în V. apar atât în componentele citoplasmei cât și în nucleul celular și membrana acestuia. Mitocondriile cresc în dimensiune, se umflă; unele mitocondrii, dimpotrivă, se micșorează, cristae sunt distruse; se modifică forma şi mărimea cisternelor reticulului endoplasmatic (vezi), apar vezicule, structuri concentrice etc.. Se modifică şi ribozomii (vezi). În nucleul celular, deteriorarea se manifestă prin localizarea marginală a cromatinei, rupturi ale membranei nucleare.
În multe cazuri, alterarea se dezvoltă prin așa-numita. efect lizozomal: atunci când membranele lizozomilor sunt distruse (vezi), se eliberează diverse enzime, în special hidrolitice, care joacă un rol semnificativ în deteriorarea structurilor celulare.
Mediatori inflamatori- o serie de substanțe fiziologic active considerate declanșatoare ale V., sub influența cărora apare principala legătură a V. - reacția vaselor patului microcirculator și sângele care curge cu o încălcare a proprietăților reologice ale sângelui, care constituie faza iniţială a reacţiei inflamatorii. Mediatorii lui V. contribuie la creșterea permeabilității vaselor sistemului microcirculator, în special a secțiunii venulare a acestuia, cu exudarea ulterioară a proteinelor plasmatice, emigrarea tuturor tipurilor de leucocite, precum și a eritrocitelor prin pereții acestor vase. Aceste substanțe active fiziologic joacă un rol important în manifestările lui V., iar unii cercetători le numesc „motoare interne” ale lui V.
Spector și Willoughby (W. G. Spector, D. A. Willoughby, 1968) dau 25 de nume de substanțe fiziologic active (mediatori chimici) cu un spectru diferit de acțiune care apar după lezarea țesuturilor. În special, multă muncă asupra mediatorilor lui V. a apărut după descoperirea histaminei și a leucotaxinei. Deși leucotaxina s-a dovedit a fi o substanță de natură eterogenă în lucrările de verificare ulterioare, studiul său a servit ca stimul pentru studii ulterioare ale chimiei endogene. Mediatorii V., dintre care cei mai importanți sunt considerați a fi histamina, serotonina, kininele plasmatice, produșii de degradare ai ARN și ADN-ului, hialuronidază, prostaglandine etc.
Una dintre principalele surse de chimie. Mediatorii lui V. sunt mastocite (vezi), în granule se găsesc to-rykh histamina, serotonina, heparina etc.; în citoplasma mastocitelor, citocrom oxidază, acidă și fosfataza alcalină, enzime pentru sinteza nucleotidelor, proteaza, exteraza, leucina-aminopeptidaza, plasmina.
Spector și Willoughby au arătat cel mai convingător rolul deosebit de important al histaminei (vezi) în declanșatorii B. Histamina este prima substanță vasoactivă care apare imediat după afectarea tisulară; cu el se asociază etapele inițiale de vasodilatație, permeabilitate vasculară crescută și exudație; histamina are un efect predominant asupra venulelor. Serotonina este, de asemenea, de mare importanță (vezi).
Dintre mediatorii lui V. este necesar de remarcat factorul de permeabilitate la globulină (PF/dil.), descoperit în plasma sanguină a cobaiului de Miles (A. A. Miles) et al. (1953, 1955) și T. S. Paskhina (1953, 1955) în exudatul inflamator aseptic, serul sanguin de iepuri, câini și oameni; acest factor favorizează eliberarea bradikininei cu ajutorul kalikreinei. Spector consideră că factorul de permeabilitate a globulinei are o relație strânsă cu mecanismul de coagulare a sângelui, și în special cu factorul Hageman (vezi Sistemul de coagulare a sângelui). Potrivit lui Miles, factorul Hageman activează precursorul globulinei PF/dil., se formează un PF/dil activ, iar apoi este pornit un lanț de reacții succesive: prekininogenază - kininogenază - kalikreină - kininogen - kinin.
Nucleozidele Nek-ry participă la reacția inflamatorie; adenozina poate provoca o creștere a permeabilității pereților microvaselor și acumularea locală de leucocite; nucleozidele nek-ry sunt eliberatoare (eliberând) o histamină.
Reacție vasculară cu exsudație joacă un rol foarte important în mecanismele lui V. O serie de autori susțin că întregul „aspect al inflamației”, toate caracteristicile sale, întreaga gamă de modificări tisulare sunt determinate de reacția vasculară, permeabilitatea vaselor microcirculatorii. pat și gravitatea daunelor acestuia.
În fazele timpurii ale V. se constată activarea funcțiilor endoteliului capilarelor. În citoplasma endoteliului, numărul de microvezicule crește, apar acumulări de citogranule, se formează poliribozomi, mitocondriile se umflă, iar cavitățile reticulului endoplasmatic se extind. Celulele endoteliale își schimbă oarecum configurația, se umflă, membranele lor devin libere (vezi Permeabilitate).
Mecanismele de trecere a substanțelor cu diferite greutăți moleculare și a celulelor sanguine prin căptușeala endotelială și membrana bazală a capilarelor și venulelor au rămas neclare mult timp. Prin utilizarea metodelor de microscopie electronică, s-a constatat că celulele endoteliale din capilarele cu endoteliu continuu, strâns adiacente între ele, sunt doar în unele locuri legate între ele cu ajutorul desmozomilor (joncțiuni strânse). Celula este fixată pe membrana bazală și fixată de celulele vecine cu o masă coloidală, cum ar fi proteinatul de calciu în combinație cu mucopolizaharide. În patol, condițiile corpului celular poate fi redus, schimba forma și se poate muta. Complexul de celule endoteliale care căptușește suprafața interioară a vaselor de microcirculație este un sistem mobil, în timpul funcționării unei tăieturi, pot apărea goluri în golurile dintre celulele endoteliale și chiar canale din corpul celulelor. Lacunele interendoteliale ar trebui atribuite așa-numitelor. pori mici, iar canalele din corpul celulei endoteliale (transport microvezicular) - la așa-numita. pori mari, prin care se realizează transportul transcapilar. Observații cu microscopul electronic dinamic
A. M. Chernukha și colab. a arătat că, de exemplu, în pneumonie, microvezicularea endoteliului capilar și formarea de microbule endoteliale mai mari sunt semnificativ crescute, indicând o creștere a metabolismului tisular.
În atenția lui V. apar tulburări pronunțate ale fluxului sanguin și circulației limfatice. După afectarea țesuturilor, cea mai timpurie modificare a unei reacții inflamatorii acute este o reducere rapidă (de la 10-20 de secunde la câteva minute) a arteriolelor. Majoritatea cercetătorilor nu acordă prea multă importanță acestui fenomen, dar Spector și Willoughby îl consideră o reacție de protecție cauzată de catecolamine. În curând se dezvoltă două faze de vasodilatație. Prima fază (vasodilatație imediată), însoțită de creșterea permeabilității la proteinele din sânge, atinge un maxim după o medie de 10 minute; a doua fază, mult mai lungă, se măsoară în câteva ore. Din cauza celei de-a doua faze de expansiune a vaselor, există o infiltrare a țesăturilor de către leucocite, o hiperemie inflamatorie (vezi), proprietățile reologice ale modificării sângelui, apar staze, hemoragii locale, tromboze ale vaselor mici; în atenția lui V., metabolismul crește, to-ry este exprimat printr-o creștere a concentrației de ioni de hidrogen, acidoză, hiperosmie. În limf, microvasele se dezvoltă limfostaza și o limfotromboză.
Schimbările în proprietățile reologice ale sângelui încep cu o modificare a vitezei fluxului sanguin, o încălcare a curentului axial, eliberarea globulelor albe din acesta și localizarea acestora de-a lungul pereților venulelor postcapilare (așa-numita poziție marginală a leucocite); se formează agregate de trombocite și eritrocite, stază și tromboză de venule și capilare. Tromboza apare din cauza activării factorului Hageman, o componentă importantă a sistemului de coagulare a sângelui. Apoi există exudația (vezi), adică ieșirea din vase în țesuturi părțile constitutive sânge - apă, proteine, săruri și celule sanguine. În focusul lui V. se găsesc produse metabolice, toxine eliberate din fluxul sanguin, adică focusul lui V. îndeplinește, parcă, o funcție eliminativă de drenaj. Substanțele (de exemplu, vopsele) care au fost exudate sau introduse direct în focarul lui V. sunt slab excretate din cauza trombozei vaselor venoase și limfatice din țesuturile inflamate.
Exudarea proteinelor are loc în secvență, ceea ce se explică prin dimensiunea moleculelor (cea mai mică moleculă de albumină, cea mai mare dintre fibrinogen): cu o ușoară creștere a permeabilității, se eliberează albumine, pe măsură ce permeabilitatea crește, globuline și fibrinogen. Exudarea moleculelor proteice are loc hl. arr. prin canalele din corpul celulelor endoteliale (pori mari) și, într-o măsură mai mică, prin goluri dintre celulele endoteliale (pori mici).
La o ieșire dintr-un curent de sânge printr-un perete de venule și capilare ale elementelor celulare ale sângelui, hl. arr. leucocite (granulocite și monocite segmentonucleare), precedate de poziționarea marginală a leucocitelor, lipindu-le de peretele vasului. AS Shklyarevsky (1869) a arătat că eliberarea de leucocite din curentul axial este în deplină concordanță cu fizicul. legea comportamentului particulelor suspendate într-un fluid care curge atunci când viteza acestuia scade. După lipirea de celulele endoteliale, granulocitele segmentate formează pseudopodi care pătrund prin peretele vasului, conținutul celulei se revarsă spre tulpină extins dincolo de vas, iar leucocitul este în afara vasului. În țesutul perivascular, granulocitele segmentate continuă să se miște și sunt amestecate cu exudatul.
Procesul de emigrare a leucocitelor se numește leucodiapedeză. S-a stabilit că emigrarea granulocitelor segmentate și a celulelor mononucleare este oarecum diferită. Deci, granulocitele segmentate (neutrofile, eozinofile și bazofile) emigrează între celulele endoteliale (interendoteliale), și agranulocite (limfocite mari și mici și monocite) - prin citoplasma celulei endoteliale (transendoteliale).
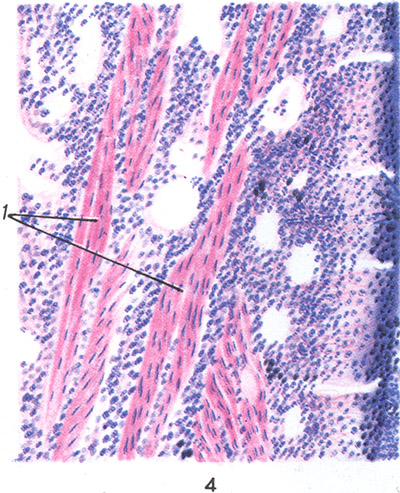
Orez. 1. Emigrarea interendotelială a leucocitelor prin peretele vasului în timpul inflamației: a - granulocitele segmentate (1) au pătruns în spațiul de sub celula endotelială și sunt situate între endoteliu (2) și membrana bazală (3). Sunt vizibile articulațiile celulelor endoteliale (4), fibrele de colagen (5), nucleii granulocitelor (6); x 20.000; b - două granulocite segmentate (1) sunt localizate în țesutul conjunctiv perivascular (membrana bazală s-a recuperat într-un gel dens). Endoteliul (2) nu este modificat, articulațiile (4) ale celulelor sale și fibrele de colagen ale țesutului conjunctiv perivascular (5) sunt vizibile; lumenul vasului (7); x 12.000.
Emigrarea interendotelială are loc după cum urmează. În faza inițială a B., granulocitul segmentat aderă la celula endotelială și, parcă, fire sunt întinse între aceasta și leucocit. Urmează apoi contracția celulei endoteliale și pseudopodiile se repezi în golul format între cele două celule; cu ajutorul lor, granulocitul segmentat pătrunde rapid în spațiul de sub celula endotelială, se exfoliază, așa cum ar fi, iar orificiul de deasupra acestuia este închis prin reconectarea celulelor endoteliale - granulocitul segmentat se află între endoteliu și membrana bazală (Fig. 1). , A). Următoarea barieră - membrana bazală - este depășită de granulocitul segmentat, aparent, prin mecanismul tixotropiei (scăderea izotermă reversibilă a vâscozității soluției coloidale), adică tranziția gelului membranei într-un sol cu o ușoară atingere. a granulocitelor către membrană. Granulocitul învinge cu ușurință solul, se găsește în țesutul din afara vasului (Fig. 1b), iar membrana bazală este din nou restaurată într-un gel dens.
La emigrarea transendotelială, agranulocitele se lipesc inițial de celula endotelială, activitatea o tăietură în același timp crește brusc; procesele sub formă de degete care apar la membrana celulei endoteliale, așa cum spune, captează celula mononucleară din toate părțile, o absorb formând o vacuola mare și o aruncă pe membrana bazală. Apoi prin mecanismul de tixotropie celule mononucleare pătrunde prin membrana bazală în spațiul perivascular și se amestecă cu exudatul.
Cu V., din vase ies și eritrocitele în țesut (vezi Diapedeză). Trec pasiv de peretele vasului creștere bruscă permeabilitatea vasculară, care se observă cu infecții foarte toxice (ciumă, antrax), deteriorarea pereților vaselor de sânge de către o tumoare, boala de radiatii si etc.
I. I. Mechnikov a explicat ieșirea din vas a granulocitelor segmentate și mișcarea către focarul de deteriorare prin chemotaxie, adică efectul asupra leucocitelor al substanțelor care au cauzat V. sau s-au format în focarul lui V. (vezi Taxiuri). Menkin (V. Menkin, 1937) a scos în evidență așa-numitul țesut inflamator. leucotaxina, care provoacă chemotaxia pozitivă a granulocitelor segmentate; chimiotaxia pozitivă este mai pronunțată la granulocitele segmentate, mai puțin la agranulocite.
Cel mai important fenomen al lui V. este fagocitoza (vezi), realizată de celule - fagocite; acestea includ granulocite segmentate - microfage și agranulocite - macrofage (vezi), în citoplasmă to-rykh, se realizează procesul de digestie intracelulară. A dezvăluit un rol pozitiv în procesele de fagocitoză a ionilor de aluminiu, crom, fier și calciu, opsonine (vezi).
S-a stabilit că diverse particule și bacterii invaginează membrana fagocitară; în citoplasma fagocitei, partea invaginată a membranei cu materialul închis în ea este desprinsă, formând o vacuolă sau fagozom. Când fagozomul se contopește cu lizozomul, se formează un fagolizozom (lizozom secundar), care, cu ajutorul hidrolazelor acide, realizează digestia intracelulară. În momentul fagocitozei, activitatea enzimelor proteolitice lizozomale crește brusc, în special fosfataza acidă, colagenaza, catepsinele, arilsulfataza A și B etc. Datorită acelorași enzime, țesuturile moarte sunt scindate; îndepărtarea produselor de degradare din focarul lui V. are loc prin fagocitoză.
Cu ajutorul fenomenelor de pinocitoză, picăturile lichide și macromoleculele sunt absorbite, de exemplu, feritina, proteina, antigenul (vezi Pinocitoză). Nossel (G. Nossal, 1966) a arătat că antigenul Salmonella este marcat iod radioactivși introdus în corpul unui iepure, este absorbit de macrofage în ordinea micropinocitozei. Moleculele de antigen din citoplasma macrofagelor sunt expuse la hidrolaze lizozomale, ceea ce duce la eliberarea de determinanți antigenici. Acestea din urmă sunt complexate cu ARN-ul macrofagului, iar apoi informațiile despre antigen sunt transmise limfocitelor, care sunt transformate în celule plasmatice care formează anticorpi. Deci, digestia intracelulară a antigenului se termină cu procesul imunogen (vezi. Imunomorfologie) și se realizează funcția de protecție și imunogenă a reacției inflamatorii, în cursul unei tăieturi există o imunitate celulară și umorală.
Cu toate acestea, împreună cu fagocitoza completă la macrofage, de exemplu, cu anumite infecții, fagocitoza este incompletă sau endocitobioza, atunci când bacteriile sau virusurile fagocitate nu sunt complet digerate și uneori chiar încep să se înmulțească în citoplasma celulei. Endocitobioza se explică prin lipsa sau chiar absența proteinelor cationice antibacteriene din lizozomii macrofagilor, ceea ce reduce capacitatea digestivă a enzimelor lizozomale.
Ca urmare a modificărilor microcirculației, a creșterii permeabilității vasculare și a exsudației ulterioare a proteinelor plasmatice, a apei, a sărurilor și a emigrării celulelor sanguine, în țesuturi se formează un lichid tulbure, bogat în proteine (de la 3 la 8%) - exudat (vezi). Exudatul se poate acumula în cavitățile seroase, între structurile fibroase ale stromei de organ, în țesut subcutanat, ceea ce duce la o creștere a volumului țesutului inflamat. Exudatul constă dintr-o parte lichidă și o masă celulară, conține produse de descompunere tisulară. Natura exudatului nu este omogenă: cu un grad mic de permeabilitate vasculară, albuminele predomină în exudat, puține celule, cu permeabilitate semnificativă - globulină, fibrină, multe celule.
Dinamica modificărilor celulare în exudat arată că, sub influența tratamentului, numărul de neutrofile scade inițial, iar numărul de monocite crește și apar un număr mare de macrofage. Modificarea exudatului granulocitelor segmentate în agranulocite este considerată un semn de prognostic favorabil.
Proliferarea (multiplicarea) celulelor este faza finală, reparatorie B. Reproducerea celulelor are loc hl. arr. datorită elementelor mezenchimatoase ale stromei, precum și elementelor parenchimului organelor. Celulele stem din țesut conjunctiv se înmulțesc - poliblaste sau celule limfoide, celule adventițiale și endoteliale ale vaselor mici, celule reticulare ale ganglionilor limfatici, limfoblasti mici și mari (vezi Țesutul de granulație, Țesutul conjunctiv). Odată cu diferențierea lor, în focusul lui V. apar celule mature și specializate: fibroblaste, fibrocite, mastocite și celule plasmatice, to-secară se diferențiază de predecesorii lor - plasmablaste și limfocitele mari și mici; apar capilare noi. Odată cu proliferarea (vezi), se observă și exudarea leucocitelor și limfocitelor neutrofile, eozinofile, bazofile etc.; în acest sens se disting infiltrate limfoide, plasmocite, eozinofile și alte infiltrate.
Elementele celulare din focarul inflamator suferă procese de transformare. Granulocitele segmentonucleare care și-au încheiat funcția fagocitară mor destul de repede. Limfocitele mor parțial, parțial se transformă în celule plasmatice, care mor treptat, lăsând produsul secreției lor - bile hialine. Mastocitele mor, monocitele din sânge care au intrat în țesuturi devin macrofage, curățând focarul lui V de detritus celular și sunt transportate de fluxul limfatic către ganglionii limfatici regionali, unde mor și ei. Cele mai persistente forme celulare din focarul inflamator sunt poliblastele și produsele diferențierii lor - celule epitelioide, fibroblaste și fibrocite. Ocazional, apar celule gigantice multinucleate, care provin din celulele endoteliale epitelioide și proliferante. Cu participarea fibroblastelor, există o sinteză activă de colagen. Citoplasma fibroblastelor devine pironinofilă, adică este îmbogățită cu ribonucleoproteine care formează o matrice pentru colagen. V. se termină cu formarea de ţesut conjunctiv fibros matur.
Tulburările de schimb care apar în centrul lui V., după Lindner (J. Lindner, 1966), pot fi subîmpărțite în procese catabolice și anabolice.
Procesele catabolice se manifestă prin încălcări ale fiziolului, echilibrul substanței principale a țesutului conjunctiv: există procese de depolimerizare a complexelor proteine-mucopolizaharide, formarea produselor de degradare, apariția aminoacizilor liberi, acizilor uronici (care duce la acidoză), aminozaharuri, polipeptide, polizaharide cu greutate moleculară mică. O astfel de dezorganizare a substanței interstițiale crește permeabilitatea țesutului vascular, exudația; aceasta este însoțită de depunerea proteinelor din sânge, inclusiv fibrinogenul, între fibrilele de colagen și protofibrile, care, la rândul lor, contribuie la modificarea proprietăților colagenului.
Reacții de apărare organismul sunt determinate în mare măsură de procesele anabolice și de gradul de intensitate a acestora. Aceste procese în V. sunt exprimate printr-o creștere a sintezei de ARN și ADN, sinteza substanței intermediare principale și enzime celulare, inclusiv hidrolitice. Histochim. studiile efectuate de Lindner cu privire la studiul enzimelor din celulele în focarul lui V. au arătat că monocitele, macrofagele, celulele gigantice și granulocitele segmentate prezintă o activitate enzimatică deosebit de mare din momentul în care apar în focalizarea lui V.. Activitatea enzimelor hidrolaze, care sunt markeri ai lizozomilor, crește, ceea ce sugerează o creștere a activității lizozomilor în focarul B. În fibroblaste și granulocite, activitatea enzimelor redox crește, sporind astfel procesul asociat de respirație tisulară și fosforilare oxidativă. .
Apariția timpurie a celulelor bogate în hidrolaze (lizozomi), și în primul rând a granulocitelor segmentate, poate fi considerată ca una dintre manifestările proceselor catabolice din cauza necesității procesării crescute a produselor de degradare; cu toate acestea, promovează procesele anabolice.
Factori de reglementare și curs
V. este considerată ca o reacție tisulară locală, totuși, apariția și cursul ei sunt în mare măsură determinate de starea generala organism. Principiu general autoreglarea cu informații de feedback este deja prezentată la nivel de celule. Cu toate acestea, reacțiile adaptive din interiorul celulei au o semnificație independentă atât timp cât sisteme functionale a întregului organism, reflectând un complex complex de autoreglare a celulelor și organelor, își păstrează starea relativ stabilă. Când această stare este perturbată, sunt activate mecanisme adaptative și compensatorii, reprezentând reacții neuroumorale complexe. Acest lucru ar trebui să fie reținut atunci când se analizează caracteristicile locale ale dezvoltării B.
Atât factorii hormonali cât și cei nervoși pot influența caracterul lui V.. Hormonii Nek-ry, hl sunt de mare importanță pentru reacțiile inflamatorii. arr. hormoni ai cortexului suprarenal și ai glandei pituitare, care a fost demonstrat în mod convingător în experiment și în clinică de către patologul canadian G. Selye. S-a stabilit că hormonul somatotrop hipofizar deoxicorticosteron acetat și aldosteron sunt capabili să crească „potențialul” inflamator al organismului, adică să întărească V., deși nu îl pot provoca singuri. Mineralocorticoizii, care afectează compoziția electrolitică a țesuturilor, au un efect proinflamator (activează V.). Alături de aceasta, glucocorticoizii (hidrocortizonul și alții), hormonul adrenocorticotrop, fără proprietăți bactericide, au un efect antiinflamator, reducând răspunsul inflamator. Cortizonul, întârzierea dezvoltării celor mai multe semne timpurii B. (hiperemie, exsudație, emigrare celulară), previne apariția edemului; Această proprietate a cortizonului este utilizată pe scară largă în medicina practică. Cortizonul privează țesutul conjunctiv de precursori ai mastocitelor (limfocite mari și poliblaste), în legătură cu aceasta, țesutul conjunctiv este epuizat de mastocite. Este posibil ca efectul antiinflamator al cortizonului să se bazeze pe aceasta, deoarece în absența mastocitelor, activitatea factorilor declanșatori V., de exemplu, histamina, care se formează din granule de mastocite, este semnificativ redusă.
Influenţa factorilor nervoşi asupra V. nu a fost suficient studiată. Cu toate acestea, se știe că în caz de încălcare a inervației periferice, mai ales sensibilă, V. devine lent, prelungit. De exemplu, ulcere trofice membrelor rezultate din leziuni măduva spinării sau nervul sciatic, durează foarte mult timp să se vindece. Acest lucru se datorează faptului că, în țesuturile lipsite de inervație sensibilă, procesele metabolice sunt perturbate, modificările alterative se intensifică, permeabilitatea vasculară crește și edemul.
Wedge, curentul lui V. depinde de setul de factori. Starea de pregătire reactivă a organismului, gradul de sensibilizare a acestuia, este de o importanță deosebită pentru cursul lui V. În unele cazuri, mai ales cu hipersensibilitate, V. este acută, în altele are un curs prelungit, dobândind caracterul de subacut sau cronic. Se observă, de asemenea, un curs ondulat al V., când perioadele de remisie a procesului alternează cu exacerbări; focarele procesului inflamator sunt posibile de-a lungul unui număr de ani, de exemplu, cu bruceloză, tuberculoză, boli de colagen. În aceste cazuri, în cursul bolii, perioada (faza) de hipersensibilitate de tip imediat este înlocuită cu o perioadă de hipersensibilitate de tip întârziat. În fazele de hipersensibilitate predomină modificările exudative și chiar necrotice cu o reacție pronunțată a sistemului de microcirculație. În procesul de remisiune a lui V. sau de trecere a procesului la o formă subacută, fenomenele vasculare scad, iar fenomenele de proliferare dominantă la hron ies în prim-plan. B. La hron, abcesul, de exemplu, odată cu formarea puroiului apar fenomene proliferative exprimate până la dezvoltarea țesăturii mature de legătură. În același timp, nodulii proliferativi cu o reacție vascular-exudativă foarte ușoară apar în primul rând cu unele boli infecțioase cu un curs acut (tifoid și tifos, malarie, tularemie).
La hron, o inflamație cu un curent ondulat o pană, imaginea poate fi foarte pestriță în funcție de predominanța uneia sau aceleia faze a V., iar în țesăturile atât vechi, cât și morfoli proaspete, sunt posibile modificări.
Principalele semne clinice
Cinci clasice o pană, semnele caracteristice V. acute ale acoperirilor exterioare păstrează valoarea, după ce a trecut testul timpului și a primit patofiziol modern. si morfol, caracteristic: roseata, umflatura, durere, febra, disfunctie. La hron. V. și V. organe interne unele dintre aceste semne pot fi absente.
Roşeaţă- o pană foarte strălucitoare, semn de V., cauzată de hiperemie inflamatorie, extinderea arteriolelor, venulelor, capilarelor, încetinirea fluxului sanguin; pe măsură ce fluxul de sânge încetinește, culoarea roșu stacojiu a țesutului inflamat devine cianotică. Hiperemia inflamatorie este combinată cu alterarea țesuturilor, creșterea permeabilității țesutului vascular, exudația și proliferarea celulară, adică cu întregul complex de modificări tisulare caracteristice B.
Umflătură la V. este cauzată în perioada inițială de consecințele unei reacții vasculare și formarea unui infiltrat și edem perifocal, care se dezvoltă mai ales ușor în jurul centrului V., înconjurat de țesut lax; în perioadele ulterioare ale lui V. contează şi proliferarea.
Durere- un însoțitor constant al lui V., rezultat din iritația cu exudat a terminațiilor nervilor senzoriali sau a anumitor substanțe active fiziologic, de exemplu, kinine.
Cresterea temperaturii se dezvoltă cu un aflux crescut sânge arterial, precum și ca urmare a creșterii metabolismului în centrul atenției B.
Funcție afectată pe baza lui V. apare, de regulă, întotdeauna; uneori aceasta poate fi limitată la o tulburare a funcțiilor țesutului afectat, dar mai des suferă întregul organism, mai ales când V. apare în organele vitale.
Principalele forme de inflamație
Pe morfol, la semne se disting trei forme de V.: alternativă, exudativă, productivă (proliferativă).
Inflamație alterativă
Inflamația alterativă se caracterizează printr-o predominanță a leziunilor tisulare, deși apar și exsudația și proliferarea. Acest tip de V. se mai numește și parenchim, deoarece se observă cel mai adesea în organele parenchimoase (miocard, ficat, rinichi, mușchi scheletici).
Modificarea este exprimată alt fel degenerarea celulelor parenchimului organului și stromei, variind de la umflarea tulbure a citoplasmei și terminând cu modificări necrobiotice și necrotice, secara poate apărea în parenchimul organului și în țesutul interstițial sub formă de umflare fibrinoid și necroza fibrinoidă.
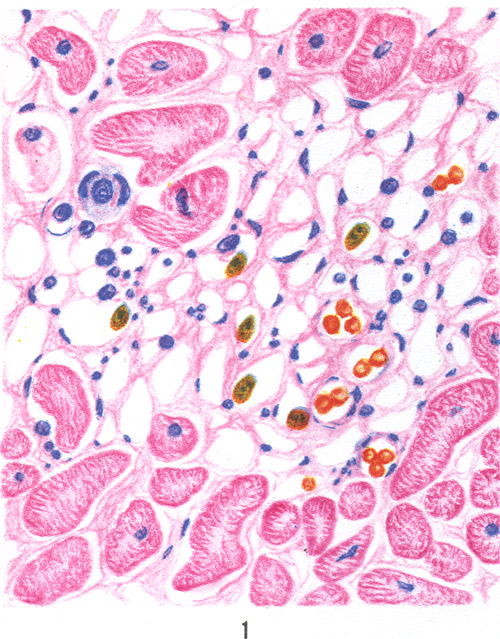
Alternativa V. cu predominanța modificărilor necrobiotice se numește V necrotică. Acest tip de V. se observă cu o reacție alergică imediată (vezi Alergie), precum și atunci când este expus la substanțe foarte toxice. Când este expus organismului toxinelor bacteriilor, de exemplu, difterie, există o alternativă V. a miocardului, o tăietură este exprimată prin apariția în diferite straturi ale miocardului, în special în zona subendocardică, focare de degenerare grasă, dezintegrarea aglomerată a miofibrilelor până la apariția în cazurile severe de focare de necroză; același lucru se observă în miocardita alergică (tsvetn. fig. 1). Reacțiile vascular-mezenchimale și proliferative sunt slab exprimate.
În ficat, alternativa V. se observă cu hepatită infecțioasă, atunci când este expusă, de exemplu, la cloroform, tetraclorură de carbon și se exprimă prin umflarea tulbure și degenerarea grasă a hepatocitelor, o creștere a dimensiunii lor și a dimensiunii ficatului în ansamblu. .
La rinichi, alternativa V. se exprimă prin degenerarea granulară a epiteliului părților proximale și distale ale nefronului până la necroză epitelială cu o reacție vascular-mezenchimală ușoară.
Rezultatele alternativei V. sunt determinate de intensitatea și profunzimea leziunii tisulare. La grad ușor distrofie după eliminarea cauzei care a provocat V., există o restaurare completă a țesuturilor; zonele de afectare ireversibilă a parenchimului sunt înlocuite cu țesut conjunctiv (de exemplu, cardioscleroza se dezvoltă după miocardita difterică).
Inflamație exudativă
Inflamația exudativă se caracterizează prin predominanța reacției sistemului de microcirculație, hl. arr. departamentul său venular, peste procesele de alterare și proliferare. Exudarea părților lichide ale plasmei, emigrarea celulelor sanguine, adică formarea exudatului, vine în prim-plan. Pentru exudativ V., o varietate de morfol și o pană, manifestările sunt tipice, deoarece, în funcție de gradul de încălcare a permeabilității vasculare, natura exudatului poate fi diferită. În acest sens, exudativul V. poate fi seros, cataral, fibrinos (crupus și difteric), purulent, putrefactiv, hemoragic, mixt.
Inflamație seroasă caracterizată prin acumularea în țesuturi, mai des în cavitățile seroase, a unui exsudat ușor tulbure, aproape transparent, care conține de la 3 la 8% proteine serice, iar în sediment - granulocite unice segmentate și celule descuamate ale membranelor seroase.
V. seroasă poate fi cauzată de agenți termici (arsuri), chimici, infecțioși (în special viruși), endocrini și alergici. Această formă de V. se dezvoltă mai des în cavitățile seroase (pleurezie seroasă, peritonită, pericardită, artrită etc.), mai rar în organele parenchimatoase - miocard, ficat și rinichi.
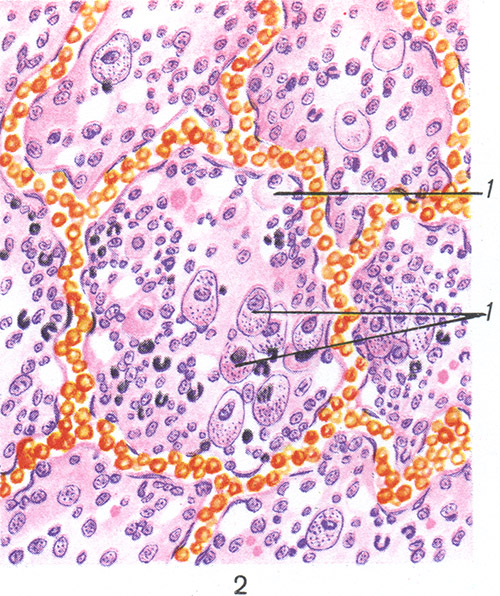
V. seroasă a miocardului se exprimă prin acumularea de exudat între fasciculele de fibre musculare, în jurul capilarelor; în ficat - în spațiile inconjurătoare-sinusoidale (spații Disse); în rinichi (cu glomerulită seroasă) - în lumenul capsulei glomerulare (capsula Shumlyansky-Bowman). În plămân, revărsatul seros se acumulează în lumenul alveolelor (tsvetn. Fig. 2). Când pielea arde, efuziunea seroasă se acumulează sub epidermă, ceea ce duce la formarea de vezicule mari. În membranele seroase se observă hiperemia, acestea devin plictisitoare, își pierd luciul caracteristic.
O efuziune seroasă poate apărea în jurul focarelor de V. purulentă (de exemplu, cu periostita a maxilarului) sau în jurul focarului tuberculos, crescând zona leziunii, așa-numita. perifocal B.
Seros V. de obicei procedează brusc. Cu o cantitate mare de efuzie, activitatea cardiacă devine dificilă, există insuficiență respiratorie mobilitate articulară limitată etc.
Rezultatul V. seros, dacă nu s-a transformat în purulent sau hemoragic, este în mare parte favorabil. Exudatul seros se absoarbe usor si nu lasa urme sau se formeaza o usoara ingrosare a membranelor seroase. În miocard și ficat, pot apărea zone mici de scleroză din cauza proliferării fibroblastelor și formării fibrelor de colagen.
catar (catar) se dezvoltă pe membranele mucoase și se caracterizează prin formarea unui exsudat lichid, adesea transparent, cu un amestec de o cantitate mare de mucus, to-ruyu secretă glandele mucoase într-o cantitate crescută. Exudatul conține leucocite, limfocite și celule epiteliale descuamate și curge de obicei pe mucoasă. Acestea sunt rinita catarală, rinosinuzita, gastrita, enterocolita. Prin natura exsudatului, adică prin predominanța anumitor elemente în exsudat, se vorbește despre cataruri seroase, mucoase sau purulente. Secolul mucoasei începe destul de des cu catar seros, to-ry trece în muc, apoi purulent.
Motivele sunt foarte variate. De mare importanță sunt microbii, termici și chimici. iritanți etc. Catarurile pot apărea atunci când apărarea organismului este slăbită, când bacteriile saprofite care vegeta pe mucoasele devin patogene.
Catarhal V. poate proceda acut și cronic. La curs acut membrana mucoasă pare plină de sânge, umflată, acoperită cu exsudat lichid. Catarul acut seros și mucos durează două-trei săptămâni și de obicei trece fără a lăsa consecințe. Cu catarul purulent, pot apărea eroziuni și ulcere pe membrana mucoasă. Cu hron, catar, în unele cazuri, membrana mucoasă poate rămâne umflată mult timp și se poate îngroșa, pe ea pot apărea polipi de diferite dimensiuni (catar hipertrofic), în alte cazuri, membrana mucoasă devine foarte subțire (catar atrofic) .
inflamație fibrinoasă se caracterizează printr-un exudat lichid, în care fibrinogenul se acumulează în scurt timp, trecând în fibrină la contactul cu țesuturile deteriorate, în urma căruia exudatul se îngroașă. Etiologia V. fibroasă este diversă: poate fi cauzată de microbi (bacil difteric, microbi de dizenterie, micobacterium tuberculosis etc.), virusuri, otrăvuri de origine endogenă (de exemplu, cu uremie) și exogenă (de exemplu, sublimată). V. fibrinos este localizat pe membranele seroase si mucoase, mai rar in profunzimile organului. Fibrinos V. se întâmplă de obicei acut, dar în cazuri nek-ry poate accepta hron, un curent sau proceda în valuri.
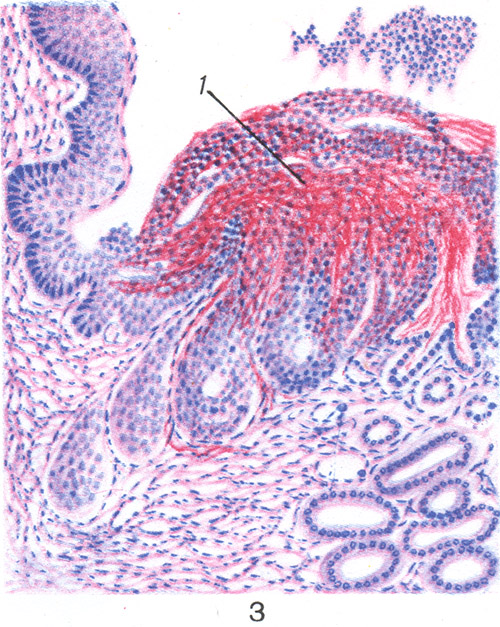
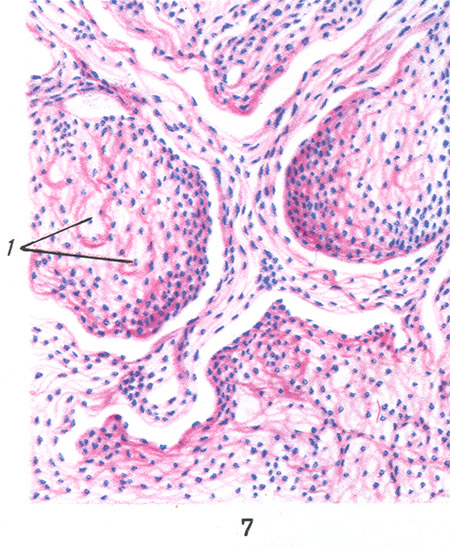
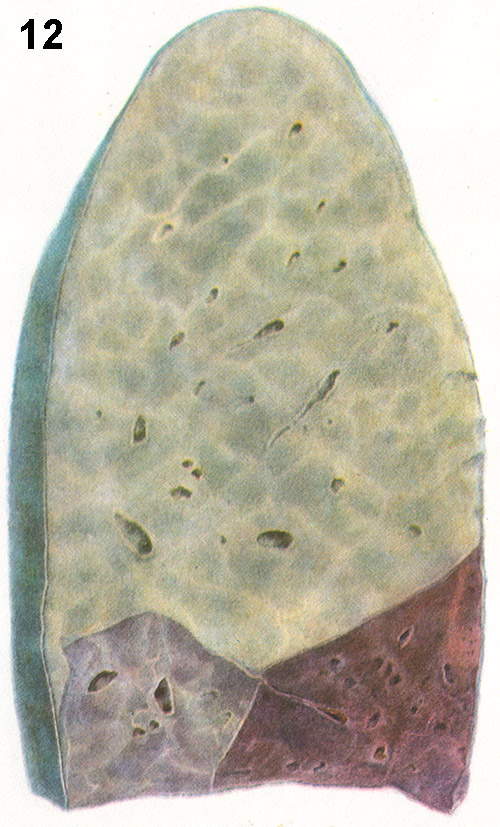
Orez. 12. Crupus inflamație a plămânuluiîn stadiul gri.
Fibrina cade pe suprafața membranelor seroase sub formă de mase viloase, iar pe suprafața mucoaselor - sub forma unui film continuu (imprimare. Fig. 3). În lumenul alveolelor pulmonare, fibrina cade sub formă de dopuri fibrinoase, de exemplu, cu pneumonie croupoasă (imprimare. Fig. 7), în urma căreia țesut pulmonar devine dens și seamănă cu un ficat în consistență (tsvetn. fig. 12).
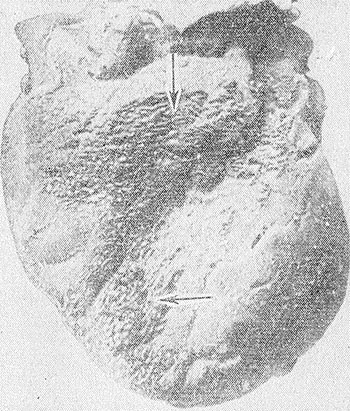
Membranele seroase capătă un aspect plictisitor, pe ele se formează suprapuneri viloase de fibrină, lipite de membrana seroasă (de exemplu, pericardită fibrinoasă - Fig. 2). Pe membranele mucoase, depozitele fibrinoase, în unele cazuri, sunt situate liber, superficial, ușor de separat, în altele sunt strâns lipite de țesutul de bază, ceea ce depinde de adâncimea leziunii și de natura epiteliului membranei mucoase. Da, conexiune epiteliul prismatic cu țesutul dedesubt este slab și fibrina, chiar a căzut în adâncurile stratului submucos, formează o peliculă liber (de exemplu, pe membrana mucoasă a stomacului, intestine, trahee, bronhii).

Orez. 10. Amigdalita difterică și traheita croupoasă. Suprafața amigdalelor și a membranei mucoase sunt acoperite cu suprapuneri membranoase.
Epiteliul scuamos este strâns legat de țesutul conjunctiv subiacent și, prin urmare, pelicula de fibrină este strâns lipită de membrana mucoasă, deși fibrina cade în stratul de suprafață al epiteliului scuamos (între celulele conservate în timpul leziunii), ceea ce se observă, pentru de exemplu, pe membrana mucoasă a amigdalelor, cavitatea bucală, esofag. În legătură cu aceste trăsături, V. fibrinos (tsvetn. Fig. 10) este împărțit în difterie (filme cu așezare strânsă) și croupus (filme cu șezut liber).
difteria B. procedează mai sever: microbii se înmulțesc sub pelicule strânse, eliberând o cantitate mare de toxină; filmele pot închide căile respiratorii, de exemplu, cu difterie a faringelui, care poate provoca asfixie. Cu crupus V., filmele sunt ușor separate, intoxicația este mai puțin pronunțată, dar riscul de blocare tractului respirator de asemenea, nu sunt excluse.
V. fibrinos este una dintre formele severe de V.; prognosticul său este în mare măsură determinat de localizarea procesului și de profunzimea leziunii tisulare, iar rezultatul V. fibrinos al membranelor seroase și mucoase este diferit. Pe membranele seroase, masele de fibrină sunt parțial supuse topirii enzimatice, majoritatea- procese de organizare, adică germinare prin țesut conjunctiv tânăr din partea laterală a straturilor cambiale ale membranelor seroase viscerale și parietale, în legătură cu care se formează aderențe (aderențe) de țesut conjunctiv, care pot perturba funcția organului.
Pe membranele mucoase, filmele fibrinoase sunt de obicei respinse din cauza autolizei (vezi), care se dezvoltă în jurul focarului și a demarcației V. În locul peliculei rupte, se formează un defect al mucoasei, un ulcer, a cărui adâncime este determinată de adâncimea prolapsului de fibrină. Vindecarea ulcerelor are loc uneori rapid, dar în unele cazuri (în special în intestinul gros cu dizenterie) este întârziată mult timp. În alveolele pulmonare, exudatul fibrinos, cu o evoluție favorabilă a pneumoniei croupoase, suferă dezintegrare litică și se rezolvă, în cazuri rare, exudatul germinează cu celule de țesut conjunctiv tânăr, se maturizează treptat și apar câmpuri de scleroză, care se numește carnificarea plămânului.
Inflamație purulentă caracterizat printr-un exudat lichid care conține albumine și globuline și uneori fire de fibrină; în sediment - neutrofile, în mare parte degradate (corpi purulenti). Un astfel de produs al lui V. - un lichid tulbure cu o nuanță verzuie - se numește puroi (vezi). Etiologia V. purulentă este diversă: poate fi cauzată de bacterii (stafilococi, streptococi, gonococi, meningococi, mai rar salmonella tifoidă, micobacterii tuberculoase etc.), ciuperci patogene, sau poate fi aseptică, cauzată de substanțe chimice. substante. V. purulentă poate apărea în orice țesut și organ, cavități seroase, în piele (Fig. 3). Curentul său poate fi acut și cronic, în cazuri nec-ry foarte greu.
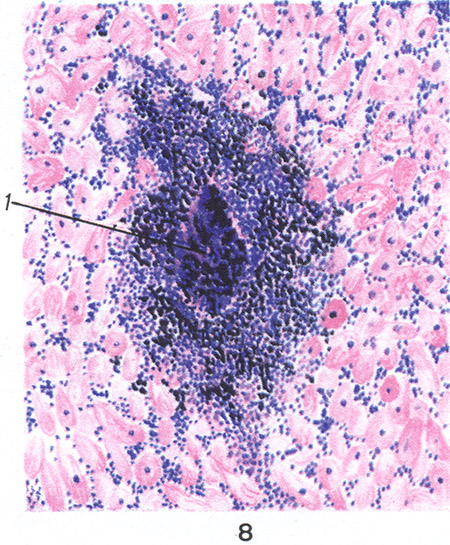
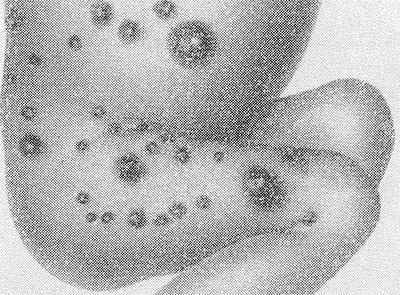
Din punct de vedere morfologic, V. purulentă poate avea două forme - un abces (vezi) și flegmon (vezi) și să fie însoțit de histoliză (topirea țesuturilor). Un abces poate apărea în primul rând (cavitatea sa se formează ca urmare a topirii țesuturilor), precum și prin embolie cu septicopiemie, de exemplu, B. purulentă focală a miocardului cu formarea unui abces (tsvetn. Fig. 8).
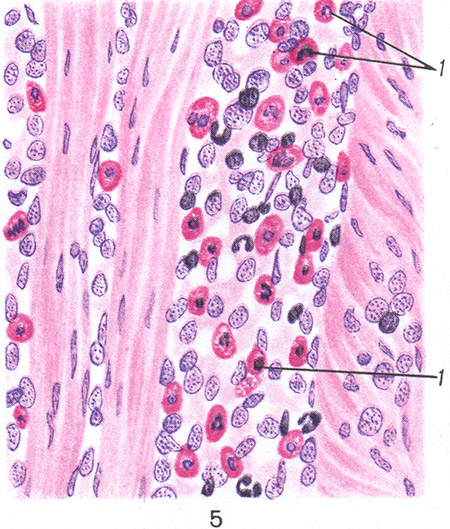
Acut difuz purulent V. (flegmon) are tendința de a se răspândi de-a lungul straturilor interfasciale, fisuri interstițiale (tsvetn. Fig. 4); la flegmonul corpurilor s-a dus.- kish. o cale în infiltrat este o mulțime de eozinofile (tsvetn. fig. 5).
La hron, forma lui V. centrul purulent este înconjurat de o capsulă fibroasă densă; în exudat, împreună cu corpurile purulente, există un număr mic de limfocite, macrofage și celule plasmatice. Pot exista perioade de exacerbare a V., formarea unei fistule cu expirarea puroiului. Acumularea de exsudat purulent în cavitățile nek-ry ale unui organism este denumită empiem (vezi).
În rezultatul V. purulentă acută, în cazuri favorabile, procesul este delimitat, este posibil să se vindece chiar și abcesele mari prin înlocuirea cavității lor cu țesut de granulație, maturându-se treptat într-o cicatrice, care rămâne la locul abcesului. Hron, purulent V. poate continua foarte mult timp și poate duce la amiloidoză (vezi). În cazurile adverse, focalizarea purulentă nu este limitată, procesul purulent trece la limfă, vase și vene, ceea ce duce la o generalizare a procesului, uneori până la sepsis (vezi).
Inflamație putridă(gangrenos, ichorus) se dezvoltă ca urmare a participării bacteriilor putrefactive (anaerobii patogeni) într-o formă sau alta de exudativ V.. Putrid V. prezintă un mare pericol pentru organism și poate apărea în acele organe care vin în contact cu mediu inconjurator(vezi Gangrena, angina lui Ludwig). Țesuturile inflamate suferă descompunere putrefactivă, capătă o culoare verde murdară, devin flăcătoare, ca și cum s-ar fi îndepărtat cu formarea de gaze urât mirositoare (vezi Infecția anaerobă).
Inflamație hemoragică caracterizată prin prezenţa în exudat a unui număr diferit de eritrocite. Caracterul hemoragic poate lua orice tip de V. (seros, fibrinos, purulent), care depinde de grad înalt creșterea permeabilității, până la distrugerea vaselor de microcirculație. Acest tip de V. apare atunci când este expus la microbi foarte virulenți; cu ciumă, antrax, gripă toxică, focarul hemoragic al lui V. seamănă cu o hemoragie. În cavitățile seroase se observă exudat hemoragic cu tumori maligne. Acest tip de V. este semnul unei boli foarte grave; rezultatul său depinde de boala de bază.
Se observă forme mixte de inflamație cu o slăbire a apărării organismului, adăugarea unei infecții secundare, de exemplu. stafilococi. In aceste cazuri exsudatul seros se poate alatura purulent sau fibrinos, apoi V. se numeste seros-purulent, seros-fibrinos etc.Exudatul cataral poate avea si un caracter mixt.Un semn de prognostic deosebit de nefavorabil este transformarea exudatului seros in hemoragic. , care indică întotdeauna asupra atașării unei infecții severe sau progresia unei tumori maligne.
Inflamație productivă
Această formă se mai numește și inflamație proliferativă, deoarece se caracterizează prin predominanța reproducerii (proliferării) elementelor celulare ale țesutului afectat. Alterarea și exudația sunt prost exprimate, greu recunoscute; granulocitele segmentate sunt rare.
V. productiv poate fi cauzat în primul rând de biol., fizic. si chimic. factori sau observaţi în timpul trecerii V. acută la cronică.
V. productivă decurge, de regulă, cronic, dar poate fi acut, de exemplu, V. granulomatos cu tifos și tifos, cu vasculită de diverse etiologii etc.
V. productivă se bazează pe reproducerea celulelor tinere ale țesutului conjunctiv local, precum și a celulelor cambiale ale capilarelor sanguine, care formează noi capilare în timpul diferențierii. Toate celulele care se înmulțesc în timpul V. productivă au atât origine locală, histiogenă, cât și hematogenă. De exemplu, în centrul V. se pot vedea limfocitele mari și mici, monocitele și, de asemenea, în cantitate mică, eozinofilele și bazofilele care provin din fluxul sanguin. Pe măsură ce celulele se maturizează, macrofagele, fibroblastele, fibrocitele, celulele limfoide, plasmatice unice și mastocite rămân în centrul atenției V. V. productivă, parcă, este completată de fibroblaste; ei secretă tropocolagen, un precursor de colagen al țesutului conjunctiv fibros, care rămâne la locul focarului B productiv.
Rezultatele inflamației productive sunt diferite. Poate apărea resorbția completă a infiltratului celular; totusi, mai des la locul infiltratului, ca urmare a maturarii celulelor mezenchimale incluse in infiltrat, se formeaza fibre de tesut conjunctiv si apar cicatrici.
Există două tipuri de V. productive: nespecifice și specifice. Cu V. productiv nespecific, celulele proliferante sunt localizate difuz în țesutul inflamat; morfol, nu există o imagine specifică caracteristică agentului cauzal care a cauzat V.. Cu V. productivă specifică, compoziția celulară a exudatului, gruparea celulelor și ciclul procesului sunt caracteristice agentului patogen V. V. specifică în cea mai mare parte are caracterul așa-numitului. granuloame infectioase - noduli formati din elemente de tesut de granulatie.
Inflamație interstițială, sau interstițial, are de obicei un hron, un curs și se caracterizează prin faptul că infiltratul inflamator se formează în stroma organului din jurul vaselor (miocard, ficat, rinichi, plămâni, mușchi striați, uter, glande endocrine). Infiltratul, constând dintr-o varietate de celule, este situat difuz, captând întregul organ, sau în focare separate în principal în jurul vaselor (tsvetn. Fig. 9). În unele cazuri, predomină orice tip de celule; uneori infiltratul este format din limfocite şi macrofage şi seamănă cu B. pe bază imunitară. La tipurile nek-ry de V. interstițială se colectează numărul mare de plasmocite care secretă gammaglobuline. Odată cu moartea celulelor plasmatice, produsele activității lor vitale rămân în țesuturi sub formă de formațiuni sferice fuchsinofile libere - așa-numitele. bile hialine sau corpuri Roussel. În rezultatul producției interstițiale V. dezvoltă scleroză (vezi) sau ciroză (vezi).
Formarea granuloamelor(noduli) apare ca urmare a proliferării celulare în țesutul interstițial al organului sub influența unui factor patogen. Acești noduli pot fi compuși dintr-o varietate de celule mezenchimale sau dintr-un singur tip de celulă; uneori sunt situate în strânsă legătură cu vase mici și chiar se formează în peretele arterei. Diametrul granulomului nu depășește de obicei 1-2 mm, dar poate ajunge la 2 cm.În centrul granulomului se găsesc uneori detritus celular sau tisular, în Krom este uneori posibil să se identifice agentul cauzal al bolii, iar la periferia detritusului, macrofagele limfoide, epitelioide și plasmatice sunt localizate în proporții diferite.și mastocite, printre care se găsesc celule gigantice multinucleate. De obicei, granuloamele sunt sărace în capilare.
Formarea granuloamelor în țesuturi reflectă protectoare și procese imunitare, secara se dezvoltă în boli infecțioase și, într-o anumită măsură, determină dinamica imunolului, procesul de la debutul leziunilor tisulare până la stadiul final al bolii, care se exprimă prin cicatrizarea granuloamelor.
Formarea granuloamelor se observă într-o serie de boli infecțioase acute (tifoid și tifos, tularemie, encefalită virală, rabie) și anumite boli hron (reumatism, bruceloză, micoză, sarcoidoză, tuberculoză, sifilis etc.).
La nek-ry hron, bolile infecțioase granuloamele devin morfol, o structură și o dinamică de dezvoltare, caracteristice acestei boli, într-o anumită măsură. În acest sens, ele sunt desemnate după cum urmează: tuberculoză - cu tuberculoză, gumă - cu sifilis, lepromă - cu lepră, noduli - cu mufă și rinosclerom. Cu bolile enumerate, V. procedează într-un mod specific, adică este caracteristic numai acestei boli; în granuloamele specifice B. compoziţia celulară este destul de asemănătoare, cele mai caracteristice sunt celulele gigantice epitelioide şi multinucleate: celulele Pirogov-Langhans - în granulomul tuberculos; celule, sau bile, Virchow - în lepră; Celulele Mikulich - cu sclerom etc.
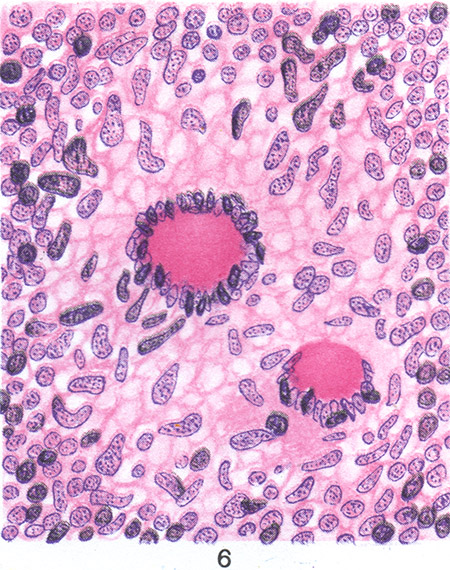
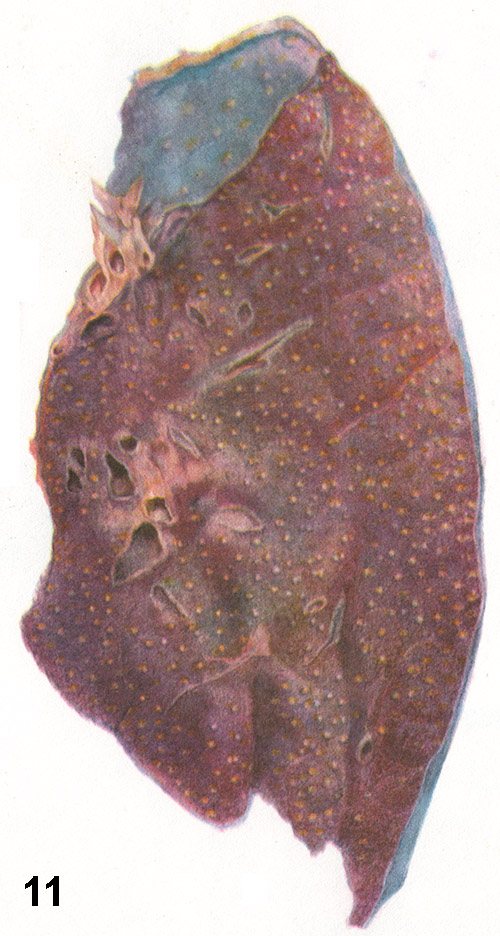
Orez. 11. Granuloame tuberculoase miliare ale plămânului.
Specificitatea granuloamelor este definită nu numai de morfolul lor, o structură (tsvetn. fig. 6), ci are și o pană. curenții și manifestările patoanatomice ale V. (tsvetn. fig. 11). În cazurile nec-ry, granuloamele la tuberculoză, sifilisul și lepra au atât de multe în comun într-o structură încât, fără o colorare specială a agentului cauzal, diagnosticul poate fi dificil; de aceea la morfol, diagnosticul specific V. este foarte importantă analiza kliniko-anatomică a unei boli în ansamblu.
Cu febra tifoidă, granuloamele se formează în grup de limf, foliculi (petice Peyer), în limf ileocecal, ganglioni, ficat, splină, măduvă osoasă. Ele apar din celulele reticulare în proliferare capabile să fagocitize salmonelele tifoide; aceste acumulări nodulare suferă apoi necroză. Procesul de formare a granulomului, inclusiv formarea cicatricilor, durează 4-5 săptămâni. (vezi febra tifoidă).
Granuloamele cu tifos apar în c. n. N de pagină, în special într-o medulă oblongata la nivelul măslinelor, în strânsă legătură cu vasele mici, se observă în to-rykh endotrombovaskulit productiv și distructiv, caracteristic unui sapropyra (vezi. Tifus epidemic). Granuloamele asemănătoare ca structură, dar cu o leziune vasculară mai puțin pronunțată, apar în c. n. Cu. cu encefalită virală și rabie.
Cu reumatism, granuloamele apar în țesutul conjunctiv al miocardului, valvele cardiace, în țesutul periarticular, în capsula amigdalelor; sunt construite din celule mari cu citoplasmă bazofilă de tip macrofag, a căror acumulare este considerată ca o reacție la procesele de dezorganizare a țesutului conjunctiv (vezi Reumatism).
La tularemie, granulomul se dezvoltă la nivel regional până în centrul înfrângerii pielii limfului, nodurilor. În centrul granulomului există un focar de necroză, de-a lungul periferiei există un arbore de celule epitelioide și limfoide și un număr mare de granulocite segmentate; uneori există celule gigantice multinucleare (vezi Tularemia).
În bruceloză, granuloamele sunt structură diferită. În unele cazuri, în centrul granulomului și în jurul circumferinței, există o acumulare de celule epitelioide și gigant multinucleate, în altele - în centrul granulomului, necroză și celule epitelioide și gigant de-a lungul periferiei (vezi Bruceloza); morfol, imaginea este foarte asemănătoare cu granulomul tuberculos.
Sarcoidoza se caracterizează prin formarea de granuloame în ganglionii limfatici, construite din celule epitelioide și gigantice fără semne de necroză în centru (vezi Sarcoidoza).
La vindecarea granuloamelor, se formează cicatrici mici, abia vizibile (vezi Granulomul).
Formarea de polipi și veruci genitale- V. productivă a mucoaselor. În același timp, cresc celulele stromei și epiteliului prismatic, se formează polipi de origine inflamatorie (catar hipertrofic); astfel sunt, de exemplu, rinita polipoa, colita etc. Pe membranele mucoase, la marginea epiteliului prismatic și scuamos, de exemplu, în anus, pe organele genitale, verucile genitale se formează din excrescențe ale epiteliului scuamos (vezi Negi). Membranele mucoase detașabile irită și macerează epiteliul scuamos, provoacă hron în stromă. V., o tăietură stimulează stroma și epiteliul să crească în continuare (vezi Papilom, Polip, polipoză).
Evoluția favorabilă a V. este determinată de perfecțiunea proceselor de fagocitoză, formarea de anticorpi, proliferarea celulelor țesutului conjunctiv și delimitarea focarului inflamator. Acest răspuns adecvat este corp sanatos si se numeste norrergic. Cu toate acestea, dezvoltarea tuturor componentelor V., cursul și rezultatul depind și de starea organismului: de boli anterioare, vârstă, rata metabolică etc.
Wedge, observațiile arată că de multe ori același agent patogen la o persoană nu provoacă nicio reacție, iar la alta - o reacție locală și generală foarte violentă, uneori chiar ducând la moarte.
De exemplu, au fost descrise cazuri de difterie, când o persoană dintr-o familie a murit din cauza unei manifestări toxice severe a bolii, în timp ce alți membri ai familiei fie nu s-au îmbolnăvit deloc, fie infecția lor s-a manifestat într-o formă ștearsă a bolii. , deși toți aveau o singură sursă de infecție.
S-a stabilit că, în funcție de reactivitatea organismului, V. poate fi hiperergic, apărut într-un organism sensibilizat (vezi Alergie), sau hipoergic, se observă o tăietură în prezența imunității la agentul V.
Există multe observații când imaginea lui V. nu corespunde tipului obișnuit, norrergic și depinde nu atât de toxicitatea agentului patogen, cât de reacția necorespunzător de violentă a organismului afectat, care poate fi cauzată de o sensibilizare preliminară ( vedea). Acest tip de V. se numește inflamație alergică.
În experiment, la animalele infectate cu bacil difteric după sensibilizarea cu ser de cal, boala se desfășoară foarte rapid și într-un mod deosebit în comparație cu animalele nesensibilizate. Faptul că o evoluție atât de diferită de normală a bolii este asociată cu sensibilizarea organismului a fost remarcat în lucrările de anafilaxie ale lui G. P. Saharov (1905), despre reacția tuberculină a lui K. Pirke (1907), în studiile asupra morfologiei. a reacțiilor alergice de A. I. Abrikosov (1938) și R. Ressle (1935), în lucrările despre dezvoltarea V. în ontogeneză de H. N. Sirotinin (1940).
Inflamație pe bază imună
Studiile lui F. Burnet (1962), R. V. Petrov (1968) au constatat că rata V. poate crește sau încetini în funcție de starea imunității celulare și umorale, adică cu o reactivitate alterată a organismului, V. dobândește trăsături care îl deosebesc de B norrergic. Astfel, introducerea unei substanțe proteice în organism ca antigen duce la dezvoltarea hipersensibilității și, cu administrarea repetată chiar și a unei doze nesemnificative din aceeași substanță, la o reacție generală sau locală inadecvată. se dezvoltă cu o diferență pronunțată față de reacția norrergică - o discrepanță între o doză mică de antigen și o reacție foarte violentă a organismului (vezi Anafilaxia, fenomenul Arthus).
O astfel de reacție se numește hiperergică, V. - hiperergică, sau o reacție de hipersensibilitate imediată: se dezvoltă în țesut la 1-2 ore după reintroducerea antigenului. Motivul V. la hipersensibilitate de tip imediat sunt complexele imune, to-secara consta din anticorpul care circulă în sânge pe antigenul introdus mai devreme, antigenul a intrat din nou în țesătură și complementul activat. Kokrin (Ch. Cochrane, 1963) a arătat că complexele imune au efect citopatic și leucotactic: se fixează în peretele vasului, în special venulele postcapilare, îl deteriorează, crescând permeabilitatea și leucodiapedeza.
Cu V. alergică, care se desfășoară în funcție de tipul de reacție de hipersensibilitate imediată, așa-numita. proteaza inflamatorie (bogată în grupări sulfhidril), care mărește brusc permeabilitatea vasculară și stimulează emigrarea granulocitelor segmentate. Cu acest tip de V., atât în experiment, cât și în patologie, o persoană suferă leziuni tisulare semnificative, o reacție foarte pronunțată a microvasculaturii, emigrarea abundentă a granulocitelor segmentate, impregnarea cu plasmă și necroza fibrinoidă a pereților vaselor mici și a țesuturilor din jur. vasele, edem, hemoragii, adică se dezvoltă un tablou caracteristic al necrozatului V.. Natura imună a acestui V. este confirmată de detectarea complexelor imune în focar, determinate prin metoda Koons (vezi Imunofluorescență).
Microscopie electronică și imunochimie. Studiile lui Shirasawa (H. Schirasawa, 1965) arată următoarea succesiune de modificări tisulare în focarul V. ischerergic de tip imediat: 1) formarea precipitatelor imune (complexe antigen-anticorp) în lumenul venulelor; 2) legarea de complement; 3) efectul chemotactic al precipitatelor asupra granulocitelor segmentate și acumularea lor în apropierea venelor și capilarelor; 4) fagocitoza si digestia complexelor imune de catre granulocite segmentate cu ajutorul enzimelor lizozomale; 5) eliberarea enzimelor lizozomale și formarea de substanțe vasoactive; 6) daune de către acestea peretele vascular urmate de hemoragie, edem si necroza.
Inflamația hiperergică, adică V., care se desfășoară pe bază imunitară, este observată la pacienții predispuși la reactii alergice, nair, cu intoleranta la medicamente, in faza acuta a cursului bolilor de colagen, cu febra fanului etc.
Există un alt tip de sensibilitate crescută a corpului - hipersensibilitate de tip întârziat; se bazează pe manifestări ale imunității nu umorale, ci celulare. În acest caz, o reacție locală în țesuturile organismului sensibilizat are loc la 12 sau mai multe ore după administrarea repetată a antigenului corespunzător. O astfel de reacție este de obicei observată la copiii infectați cu micobacterium tuberculosis după administrarea intradermică de tuberculină, prin urmare, o reacție de hipersensibilitate de tip întârziat este numită și reacție de tip tuberculină. Rolul principal în focalizarea unui astfel de V. aparține limfocitelor T și macrofagelor. Limfocitele sunt reprezentanți ai populației de limfocite timusului, migrează din organele limfoide în sânge și înapoi (limfocite recirculare), ca și cum ar găsi un antigen în țesuturi și au un efect patogen asupra țesuturilor. Limfocitele intră în contact cu macrofagele bogate în fosfatază acidă și, parcă, se informează reciproc despre natura antigenului. Modificările patului microcirculator în focarul lui V. cu acest tip de reacție sunt foarte slab exprimate, granulocitele segmentate sunt absente, semnele V. nu sunt exprimate clar. Între timp, V., care decurge în funcție de tipul de hipersensibilitate întârziată, este observată într-o serie de boli autoimune severe (la piele, ficat, rinichi etc.). având prost exprimate wedge, și morfol, dinamică și se termină cu o scleroză.
Destul de des gistol, o imagine la hron, interstițial V. la persoană amintește de reacția de tip întârziat (predominanță în infiltrat de limfocite și macrofage); V. are un curs prelungit, reflectând procesele autoimune care au loc în organism. Același tip de V. se observă în timpul formării granuloamelor. În unele cazuri, granuloamele îndeplinesc funcția macrofagelor în raport cu antigenul, în altele, granulomul este, așa cum ar fi, destinat resorbției produselor de degradare tisulară în centrul leziunilor imune (de exemplu, granulomul reumatic).
V., dezvoltându-se pe bază imunitară, se poate manifesta într-o formă mixtă, atunci când este dificil de stabilit granițele dintre două tipuri de V. hiperergice.
Diferențierea inflamației și a proceselor similare morfologic
În forma dezvoltată V. nu reprezintă dificultăți mari pentru un diagnostic de pană și morfol. Oricum numai morfol, este imposibil să ne limităm la criteriu la recunoașterea lui V., în special la formele sale separate; este necesar să se țină seama de întregul complex de manifestări, inclusiv pană, date. În organism, se observă astfel de reacții tisulare și vascular-celulare, cum ar fi, de exemplu, cu hipersensibilitate de tip întârziat, atunci când este dificil de detectat toate semnele de V. în țesuturi: de exemplu, nu există o reacție pronunțată de vasele de microcirculație, nu există granulocite segmentate sau, așa cum se observă în peretele stomacului în mijlocul digestiei, o mulțime de granulocite segmentate ca manifestare a leucocitozei distributive. Se știe că în timpul involuției postpartum a uterului în organele glandulare este posibil să se detecteze infiltrate din celulele limfoide ca expresie a modificărilor metabolice. Proliferarea exprimată a plasmoblastelor și plasmocitelor în organele imunogenezei (măduvă osoasă, limf, noduri, splină, timus) ca expresie a unei reacții de protecție, manifestată prin producerea de anticorpi. În țesutul peripelvin sunt descrise focare de hematopoieza extramedulară, asemănătoare cu un infiltrat inflamator.
Apar mari dificultăți în a face distincția între procesele inflamatorii și distrofice, proliferarea celulelor inflamatorii și proliferarea celulelor neinflamatorii, în special tumora.
Rezultatele și semnificația inflamației pentru organism
Rezultatele lui V. sunt diferite și depind de cauză, starea organismului și structura organului. Moartea țesuturilor vitale este posibilă cu cele mai grave consecințe pentru organism. Cu toate acestea, de obicei țesutul inflamat este delimitat treptat de țesutul sănătos din jur, produsele degradării țesuturilor suferă clivaj enzimatic și sunt resorbite prin fagocitoză, absorbite de capilarele limfei nou formate. retelelor. Mulțumită proliferarea celulară Focalizarea lui V. este înlocuită treptat de țesut de granulație (vezi). Dacă nu au existat leziuni tisulare semnificative, poate avea loc recuperarea completă a acestora. Cu un defect semnificativ la locul focalizării lui V., se formează o cicatrice ca urmare a maturării țesutului de granulație (vezi). Unele patol, modificări (îngroșarea și aderența membranelor seroase, creșterea excesivă a cavităților seroase, cicatrici în organe) pot rămâne în organe și țesuturi, încălcând funcția unui organ regional în cazuri severe, uneori întregul organism. Deci, de exemplu, un exudat fibrinos de pe suprafața membranelor seroase, în lumenul alveolelor, se poate dizolva sau, odată cu acumularea sa semnificativă, suferă organizare și transformare a țesutului conjunctiv. V. productivă interstițială difuză se termină de obicei cu scleroza difuză a organului (de exemplu, cardioscleroza). Odată cu vindecarea unui număr mare de granuloame, de exemplu, în miocard cu reumatism, se formează câmpuri semnificative de cardioscleroză, care afectează negativ activitatea inimii. În cazurile în care țesutul conjunctiv emergent se micșorează și comprimă parenchimul, organul este deformat, care este de obicei însoțit de o restructurare a structurii sale și de fenomene de regenerare (vezi). Un astfel de proces este denumit ciroză de organ, de exemplu, ciroză hepatică, nefrociroză, pneumociroză.
Inflamația este o reacție importantă protectoare și adaptativă și, în termeni biologici generali, destul de oportună dezvoltată în procesul de filogeneză; această reacție a devenit treptat mai complicată în procesul de evoluție a organismelor vii (vezi Reacții de protecție ale corpului, Reacții de adaptare). V. poartă protecție împotriva influenței unui factor patogen sub forma unui biol deosebit, o barieră care se exprimă prin fenomenul de fagocitoză și dezvoltarea imunității celulare și umorale. Cu toate acestea, această reacție este automată, se realizează prin mecanismele de autoreglare cu ajutorul influențelor reflexe și umorale. Apărând ca reacție adaptativă, V. în anumite condiții poate dobândi uneori o valoare dăunătoare pentru organism: cu V. se produce leziuni tisulare, cu unele forme până la necroză.
Datorita reactiei inflamatorii se delimiteaza focarul de afectare de intregul organism, emigrarea globulelor albe in focarul de V. si fagocitoza, eliminarea principiilor nocive. Proliferarea limfocitelor și a celulelor plasmatice contribuie la producerea de anticorpi și la creșterea imunității locale și generale. În același timp, este bine cunoscut faptul că acumularea de exudat în V. poate fi foarte periculoasă. Deci, de exemplu, exudatul în alveole cu pneumonie de la începutul apariției sale are influenta negativa asupra corpului, deoarece schimbul de gaze este perturbat, formarea unui revărsat fibrinos pe membrana mucoasă a laringelui provoacă o îngustare a lumenului, irită receptorii laringelui, care este însoțită de un spasm al mușchilor laringelui și poate duce la asfixie (vezi). Fagocitoza poate fi incompletă: un fagocit care a absorbit o bacterie, dar nu o poate digera, devine un purtător de infecție în întregul organism.
Încălcări la V. nu numai local; apare de obicei și reacție generală organism, exprimat prin febră, leucocitoză, VSH accelerat, modificări ale metabolismului proteinelor și carbohidraților, fenomene de intoxicație generală a organismului, care la rândul său modifică reactivitatea organismului.
I. I. Mechnikov scria în 1892: „... puterea de vindecare a naturii, al cărei element principal sunt reacțiile inflamatorii, nu este deloc o adaptare care a ajuns la perfecțiune. Bolile private și cazurile de moarte prematură dovedesc suficient acest lucru. Și mai departe: „Această imperfecțiune a făcut necesară intervenția activă a unui om nemulțumit de funcția puterii sale naturale de vindecare”. Imperfecțiunea „puterii vindecătoare” a naturii o face necesară intervenție chirurgicalăși utilizarea agenților terapeutici care vizează îmbunătățirea reacțiilor de protecție și compensare ale organismului și eliminarea V.
Secolul este piatra de temelie a multor boli, prin urmare este una dintre cele mai importante probleme experimentale și o pană, medicina. Este studiat la toate nivelurile de biol, structuri, începând de la molecular, subcelular, celular și terminând. întreg organismul. Se cercetează etiol, factori, biochimici, modificări, morfofiziol. caracteristicile, reactivitatea țesuturilor și a organismului în ansamblu, pană, imaginea B. O secțiune specială a apărut în dezvoltarea problemei V. - V. farmacologie - studiul mecanismelor de acțiune a mediatorilor lui V., cu participarea căreia se realizează diferite etape ale reacției inflamatorii; Se caută medicamente antiinflamatoare active care inhibă eliberarea acestor mediatori și, prin urmare, contribuie la scăderea B.
Bibliografie: Ado A. D. Fiziopatologia fagocitelor, M., 1961, bibliogr.; Alekseev O. V. și Chernukh A. M. Conexiuni neuro-capilare în miocardul șobolanilor, Bull. Experiment, biol, and medical, t. 74, No. 12, p. 96, 1972, bibliogr.; Alpern D. E. Inflamaţie (Probleme de patogeneză), M., 1959, bibliogr.; Voronin VV Inflamaţie, Tbilisi, 1959, bibliogr.; Inflamație, imunitate și hipersensibilitate, trans. din engleză, ed. G. 3. Moveta, M., 1975; Kongeim I. Patologia generală, per. din germană, vol. 1, Sankt Petersburg, 1887; M e n-to în V. Dinamica inflamaţiei, trad. din engleză, M., 1948, bibliografie; Mechnikov II Eseu despre starea actuală a problemei inflamației, SPb., 1897; el, Prelegeri despre patologia comparată a inflamației, M., 1947; Paskhina T. S. Rolul factorilor umorali de natură peptidică și proteică în reglarea permeabilității capilare, Vestn. Academia de Științe Medicale a URSS, nr. 9, p. 21, 1962; Pigarevsky VE Citochimia proteinelor cationice antibacteriene ale leucocitelor în fagocitoză și inflamație, Arkh. patol., t. 37, nr. 9, p. 3, 1975, bibliogr.; G1 despre l şi car A. Reacţiile inflamatorii şi dinamica lor, trad. din franceză, Novosibirsk, 1969, bibliografie; Strukov AI Probleme controversate în doctrina inflamației, Arkh. patol., t. 34, nr. 10, p. 73, 1972, bibliogr.; Chernukh A. M. Focalizarea infecțioasă a inflamației, M., 1965, bibliogr.; Chernukh A. M., Alexandrov P. N. și Alekseev O. V. M! microcirculation, M., 1975, bibliogr.; C o t r a n R. S. Structura fină a microvasculaturii în raport cu permeabilitatea normală şi alterată, în: Bazele fizice ale transportului circulator, ed. de E. B. Reeve a. A. C. Guyton, p. 249, Philadelphia-L., 1967, bibliogr.; H i r s c h J. G. Fagocitoza, Ann. Rev. Microbiol., v. 19, p. 339, 1965, bibliogr.; Procesul inflamator, ed. de B. W. Zweifach a. o., v. 1 - 3, N. Y.--L., 1974; Mediatori ai inflamației, ed. de G. Weissmann, N. Y., 1974; M i 1 e s A. A. Substanţe moleculare mari ca mediatori ai reacţiei inflamatorii, Ann. N. Y. Acad. Sc., v. 116, p. 855, 1964; M i 1 es A. A. a. Wilhelm D. L. Globuline care afectează permeabilitatea capilară, în: Polipeptide care efectuează mușchii netezi a. vasele de sânge, ed. de M. Schachter, p. 309, Oxford a. o., 1960, bibliogr.; Rocha e Silva M. Mediatori chimici ai reacției inflamatorii acute, Ann. N. Y. Acad. Sc., v. 116, p. 899, 1964; Selye H. The mast cells, Washington, 1965, bibliogr.; Spector W. G. Activarea unui sistem de globulină care controlează permeabilitatea capilară în inflamație, J. Path. Bact., v. 74, p. 67, 1957, bibliogr.; alias, Substanțe care afectează permeabilitatea capilară, Pharmacol. Apoc., v. 10, p. 475, 1958, bibliogr.; Spectorul W. G. a. Willoughby D. A. Răspunsul inflamator, Bact. Apoc., v. 27, p. 117,1963; ei, The pharmacology of inflammation, L., 1968; Willoughby D. A. a. Walters M. N. Efectul acidului ribonucleic (ARN) asupra permeabilității vasculare și posibila relație cu LNPF, J. Path. Bact., v. 90, p. 193, 1965.
A. I. Strukov, A. M. Cernukh.


